Clear Sky Science · nl
De rol van genen gerelateerd aan cellulaire veroudering bij ischemie‑reperfusie‑letsel en de identificatie van hun biomarkers
Waarom hartschade kan verergeren wanneer de bloedtoevoer terugkeert
Als iemand een hartaanval heeft of een hartoperatie ondergaat, proberen artsen zo snel mogelijk de bloedtoevoer naar het verhongerde hartweefsel te herstellen. Paradoxaal genoeg kan die levensreddende stap zelf extra schade veroorzaken — een probleem dat bekendstaat als ischemie‑reperfusie‑letsel. Deze studie onderzoekt waarom sommige hartcellen zo slecht reageren wanneer het bloed terugkeert, met de nadruk op de biologie van cellulaire veroudering en het identificeren van een kleine set genen die artsen kunnen helpen deze verborgen schade preciezer te detecteren en mogelijk te behandelen.
Wanneer redding verandert in nieuwe schade
Ischemie‑reperfusie‑letsel verloopt in twee fasen. Eerst raakt een kransslagader geblokkeerd en wordt het hartweefsel van zuurstof beroofd (ischemie). Vervolgens, wanneer de blokkade wordt opgeheven en het bloed terugstroomt (reperfusie), kan een wolk van reactieve moleculen en ontsteking reeds kwetsbare cellen verder beschadigen. Huidige hulpmiddelen — zoals ECG’s, beeldvorming en bloedtests voor eiwitten als troponine — missen vaak vroegtijdige of subtiele schade en kunnen niet gemakkelijk voorspellen wie op lange termijn problemen zal ondervinden. Dat gat heeft onderzoekers ertoe aangezet dieper te kijken, naar de moleculaire gebeurtenissen binnen de hartcellen zelf.
Cellulaire veroudering als verborgen motor
De auteurs concentreren zich op cellulaire senescentie, een toestand waarin cellen permanent stoppen met delen en een soort "alarm" afgeven. Gesenesenteerde hartcellen scheiden een mengsel van ontstekingsbevorderende moleculen en enzymen uit, bekend als het senescence‑associated secretory phenotype. Deze chemische wolk kan littekenvorming verergeren, immuuncellen aantrekken en weefselherstel verstoren, waardoor een vicieuze cirkel van schade en chronische disfunctie ontstaat. Door publieke genexpressie‑datasets van muizenharten die aan ischemie‑reperfusie blootgesteld waren te doorzoeken en deze te kruisen met honderden genen die met cellulaire veroudering zijn geassocieerd, verkleinde het team de set tot 26 genen die duidelijk veranderen na letsel.
Zes genen die een diagnostische vingerafdruk vormen
Om de meest informatieve signalen uit die 26 genen te vinden, gebruikten de onderzoekers verschillende machine‑learningmethoden. Deze algoritmen zoeken naar combinaties van genen die het beste beschadigde harten van gezonde harten onderscheiden. Na logistieke regressie, LASSO en support vector machine‑analyses kwamen zes genen naar voren als een krachtig diagnostisch panel: CDKN2B, ID1, STAT3, TERF2, TP53 en ZNF277. Gezamenlijk konden hun activiteitspatronen ischemie‑reperfusie‑letsel in de samengestelde datasets met zeer hoge nauwkeurigheid identificeren, en deden ze het in interne tests beter dan veel traditionele bloedmarkers. Gen‑padanalyses verbonden deze markers met stressresponscircuits die te maken hebben met oxidatieve schade, cel‑doodprogramma’s en bekende signaalroutes zoals MAPK en PI3K–AKT, die allemaal bepalen of een cel herstelt of in permanente senescentie belandt.
Hoe het immuunsysteem in het verhaal past
Schade door herstelde bloedstroom gebeurt niet geïsoleerd; immuuncellen stromen snel het hart binnen. Door de activiteit van immuuncellen te schatten uit dezelfde genexpressiegegevens, vond de studie duidelijke tekenen van verhoogde immuunbetrokkenheid in beschadigde harten, waaronder verschillende typen T‑cellen, B‑cellen, macrofagen en mestcellen. Eén verouderingsgerelateerd gen, CDKN2B, correleerde sterk met "central memory" CD4‑T‑cellen, terwijl TP53 verband hield met geactiveerde mestcellen. Deze verbanden suggereren dat verouderingsroutes in hartcellen en veranderingen in het immuunsysteem elkaar versterken: ouder wordende cellen roepen immuunhulp in, en die immuunreacties kunnen op hun beurt schade en littekenvorming verdiepen.
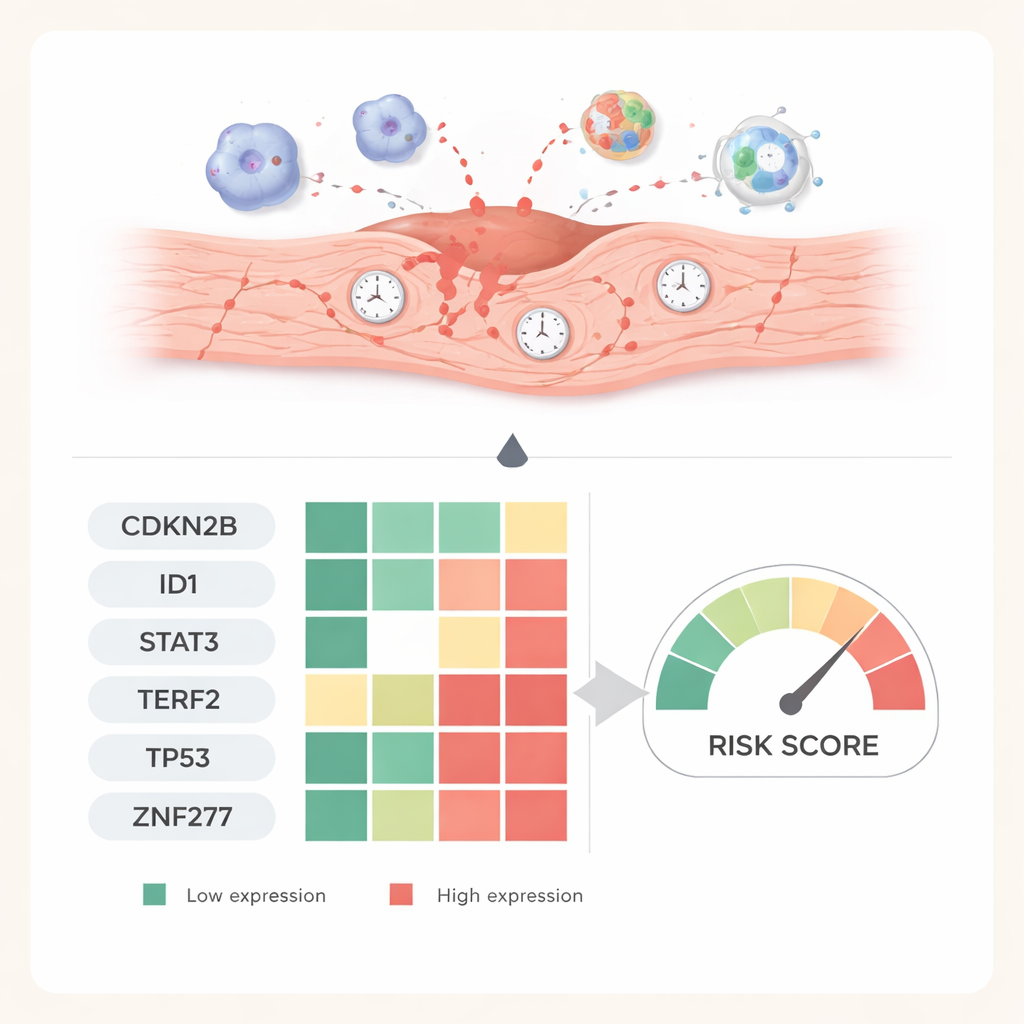
Van computer‑voorspellingen naar levende harten
Om te testen of deze zes genen verder tellen dan computermodellen, creëerden de onderzoekers een muismodel van ischemie‑reperfusie‑letsel. Ze maten genactiviteit op verschillende momenten nadat de bloedstroom was hersteld en gebruikten weefselkleuring om de bijbehorende eiwitten in hartdoorsneden te visualiseren. Eén gen, CDKN2B, nam gestaag toe over een week, wat suggereert dat het helpt beschadigde cellen in een langdurige senescente staat te verankeren. Andere genen, waaronder ID1, STAT3, TP53, TERF2 en ZNF277, vielen vroeg scherp terug en herstelden zich vervolgens geleidelijk, een patroon dat de verschuivingen tussen acute stress, actieve schade en later herstel weerspiegelt. Deze tijdsafhankelijke patronen ondersteunen het idee dat elk gen een andere fase van de reactie van het hart vastlegt.
Wat dit voor patiënten kan betekenen
Voor een niet‑specialist is de kernboodschap dat de studie hartaanval‑gerelateerde schade koppelt aan de biologie van cellulaire veroudering en een zesgenige "vingerafdruk" identificeert die deze schade in experimentele modellen aangeeft. Hoewel het werk nog preklinisch is en voornamelijk gebaseerd op muisgegevens en openbare databanken, biedt het een routekaart voor nieuwe bloed- of weefseltests die ischemie‑reperfusie‑letsel eerder en specifieker kunnen opsporen dan de huidige hulpmiddelen. Op de lange termijn kan begrip van hoe deze verouderingsgerelateerde genen ontsteking, littekenvorming en herstel sturen, de weg openen naar behandelingen die niet alleen geblokkeerde slagaders herstellen, maar ook helpen dat herstelde hart vollediger te laten genezen.
Bronvermelding: Sun, L., Liu, H., Jia, T. et al. The role of cellular senescence-related genes in ischemia–reperfusion injury and the identification of their biomarkers. Sci Rep 16, 5211 (2026). https://doi.org/10.1038/s41598-026-36076-2
Trefwoorden: ischemie reperfusie letsel, cellulaire veroudering, hartaanval, biomarkers, immuunontsteking