Clear Sky Science · nl
Proteomische analyse van het secretoom van endotheliale progenitorcellen identificeert Serpine 1 als een krachtige regulator van osteogenese
Het helen van gebroken bot zonder donorgraft
Wanneer een bot ernstig gebroken is of een deel ontbreekt, hebben chirurgen vaak moeite om zowel de stevigheid als de vorm te herstellen. De huidige opties — bot wegnemen uit een ander deel van het lichaam of synthetische grafts gebruiken — kunnen pijnlijk en riskant zijn en werken niet altijd. Deze studie onderzoekt een ander idee: in plaats van cellen te transplanteren, kunnen we precies de juiste natuurlijke eiwitten toedienen om het eigen botopbouwende mechanisme van het lichaam aan te zetten?
Waarom sommige botletsels niet genezen
De meeste fracturen genezen vanzelf, maar grote bottekorten — zoals die door trauma, tumoren of sterke kaakatrofie ontstaan — genezen vaak niet. In zulke gevallen heeft het lichaam simpelweg niet genoeg lokale bloedvatcellen en botvormende stamcellen om het ontbrekende deel te herbouwen. Onderzoekers in weefseltechniek proberen dit op te lossen door drie ingrediënten te combineren: levende cellen die nieuw bot kunnen vormen, een scaffold die ze iets biedt om op te groeien, en signalen die hen vertellen wat ze moeten doen. Celtransplantaties kunnen werken, maar zijn duur, sterk gereguleerd en niet altijd praktisch voor routinekliniek. Dat heeft wetenschappers gedreven naar “celvrije” oplossingen rond slimme biomaterialen en zorgvuldig gekozen eiwitten.
Geheime signalen van vaatopbouwende cellen
Endotheliale progenitorcellen zijn zeldzame cellen in het bloed die helpen nieuwe bloedvaten te vormen. Eerder werk liet zien dat wanneer deze cellen nabij bot worden geplaatst, ze de genezing bevorderen — voornamelijk door oplosbare signalen uit te zenden in plaats van zelf in bot te veranderen. In de nieuwe studie verzamelden de auteurs het vloeibare kweekmedium waarin deze cellen hadden gegroeid en gebruikten geavanceerde proteïne-analyse om honderden uitgescheiden moleculen in kaart te brengen. Ze concentreerden zich op acht eiwitten die sterk gekoppeld zijn aan vaatgroei en botvorming. Met menselijke beenmergstamcellen en menselijke microvasculaire endotheelcellen in het laboratorium testten ze systematisch welke van deze eiwitten het beste celgroei stimuleerden, migratie dirigeerden en botachtige mineraalafzetting uitlokten.
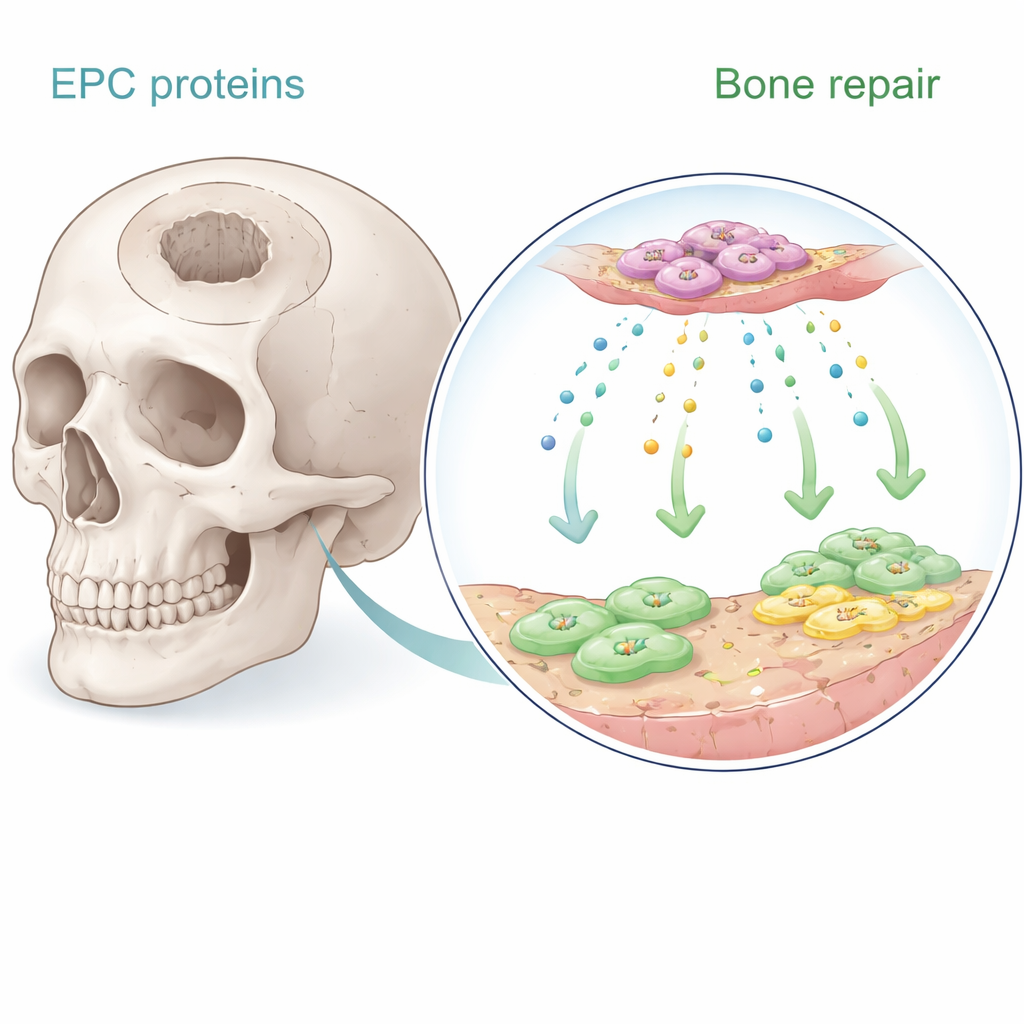
Een verrassend eiwit komt bovendrijven
Onder de kandidaten stak één eiwit er bovenuit: Serpine-1, beter bekend om zijn rol bij bloedstollingsregulatie en wondgenezing. In kweekschalen verhoogde Serpine-1 significant de proliferatie van zowel beenmergstamcellen als endotheelcellen op een dosisafhankelijke manier, en deed het in dit opzicht beter dan bekende groeifactoren zoals BMP-2 en SDF-1. Het bevorderde ook de rijping van stamcellen tot botvormende cellen, aangetoond met klassieke kleuringen die alkalische fosfatase-activiteit en calciumrijke mineraalafzettingen laten zien. Andere eiwitten, zoals plaatjesafgeleide groeifactor en BMP-2, waren effectiever in het aanmoedigen van cellen om in een "wond"-gebied te kruipen in migratieproeven, maar Serpine-1 bood een zeldzame combinatie van zowel celtoename als botopbouwend gedrag.
Een eiwit omzetten in een praktisch implantaat
Het vinden van een veelbelovend eiwit is slechts de helft van de uitdaging; het moet ook op een gecontroleerde manier naar een letselplaats worden gebracht. Het team kapselde Serpine-1 in kleine biologisch afbreekbare bolletjes van een medische polymeer genaamd PLGA, en mengde deze microsferen vervolgens door een zachte collageengel. Dit creëerde een scaffold die het eiwit langzaam vrijgaf over tijd. Ze testten het in muizen door een cirkelvormig gat van 4 millimeter in de schedel te boren — een defectgrootte die niet vanzelf geneest. Sommige defecten werden gevuld met alleen collageen, sommige met collageen plus lege microsferen, en sommige met het Serpine-1–geladen scaffold. Na acht weken toonden hoogresolutie micro-CT-scans aan dat de Serpine-1-groep significant meer botvolume, dichtheid en dikte binnen het defect had. Opmerkelijk was dat alleen deze dieren nieuw bot in het midden van de opening ontwikkelden, in plaats van alleen langs de randen.
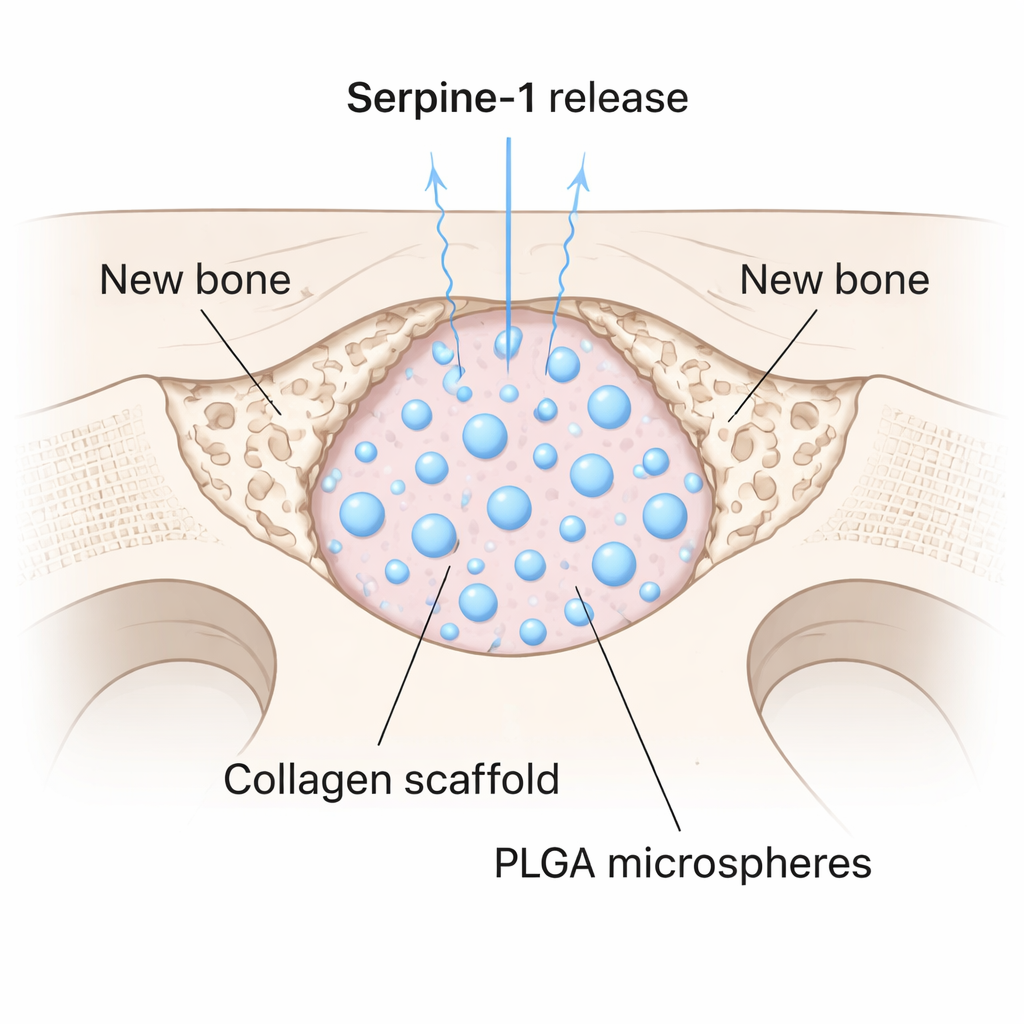
Wat dit kan betekenen voor toekomstige botzorg
De studie introduceert Serpine-1 als een krachtig en eerder ondergewaardeerd signaal voor botvorming. Door dit eiwit te combineren met een langzaam vrijkomend scaffold bereikten de onderzoekers betekenisvolle bothergroei in een defect dat normaal leeg zou blijven. Hoewel Serpine-1 cellen niet zo sterk aantrok naar het defect als sommige andere factoren, suggereert het vermogen om bestaande cellen te laten vermenigvuldigen en rijpen dat het gecombineerd kan worden met migratiebevorderende eiwitten voor nog betere resultaten. Voor patiënten zouden dergelijke celvrije, op eiwitten gebaseerde materialen mogelijk ooit de noodzaak kunnen verkleinen om bot uit het eigen lichaam te oogsten of te vertrouwen op complexe celtherapieën, en zo een eenvoudiger manier bieden om hardnekkige botletsels toch te laten genezen.
Bronvermelding: Asbi, T., Tamari, T., Doppelt-Flikshtain, O. et al. Proteomic analysis of endothelial progenitor cells secretome identifies Serpine 1 as a potent regulator of osteogenesis. Sci Rep 16, 5165 (2026). https://doi.org/10.1038/s41598-026-36048-6
Trefwoorden: botregeneratie, Serpine-1, weefseltechniek, endotheliale progenitorcellen, collageen scaffold