Clear Sky Science · nl
Classificatie van de ernst van dementie gerelateerd aan Alzheimer met magnetische resonantiebeeldvorming met afgeleide-vrije optimalisatie van een convolutioneel neuraal netwerk
Artsen helpen dementie eerder te zien
Naarmate bevolkingen verouderen, maken veel gezinnen zich zorgen over geheugenverlies en dementie. Hersenscans kunnen vroege veranderingen laten zien die verband houden met de ziekte van Alzheimer, maar het doorvragen van duizenden beelden met het blote oog is traag en moeilijk, zelfs voor deskundigen. Deze studie presenteert een slim computergereedschap dat MRI-hersenscans analyseert en mensen indeelt in vier niveaus van dementie: van geen dementie tot matige stoornis. Het systeem is ontworpen om zowel buitengewoon nauwkeurig als licht genoeg te zijn om op gewone ziekenhuiscomputers te draaien, waardoor geavanceerde beeldanalyse breder toegankelijk wordt.
Een nieuwe slimme hulp voor hersenscans
De onderzoekers richten zich op een type kunstmatige intelligentie genaamd convolutioneel neuraal netwerk, of CNN, dat uitblinkt in het herkennen van patronen in beelden. In plaats van alleen te beslissen of iemand de ziekte van Alzheimer heeft, onderscheidt hun hulpmiddel vier stadia: geen dementie, zeer mild, mild en matige dementie. Hiervoor trainde het team hun model op grote openbare verzamelingen van MRI-scans die al door experts waren gelabeld. Het doel was tweeledig: bijna perfecte nauwkeurigheid bereiken en het model compact en snel houden, zodat het praktisch is voor dagelijks klinisch gebruik in plaats van alleen voor goed gefinancierde laboratoria.
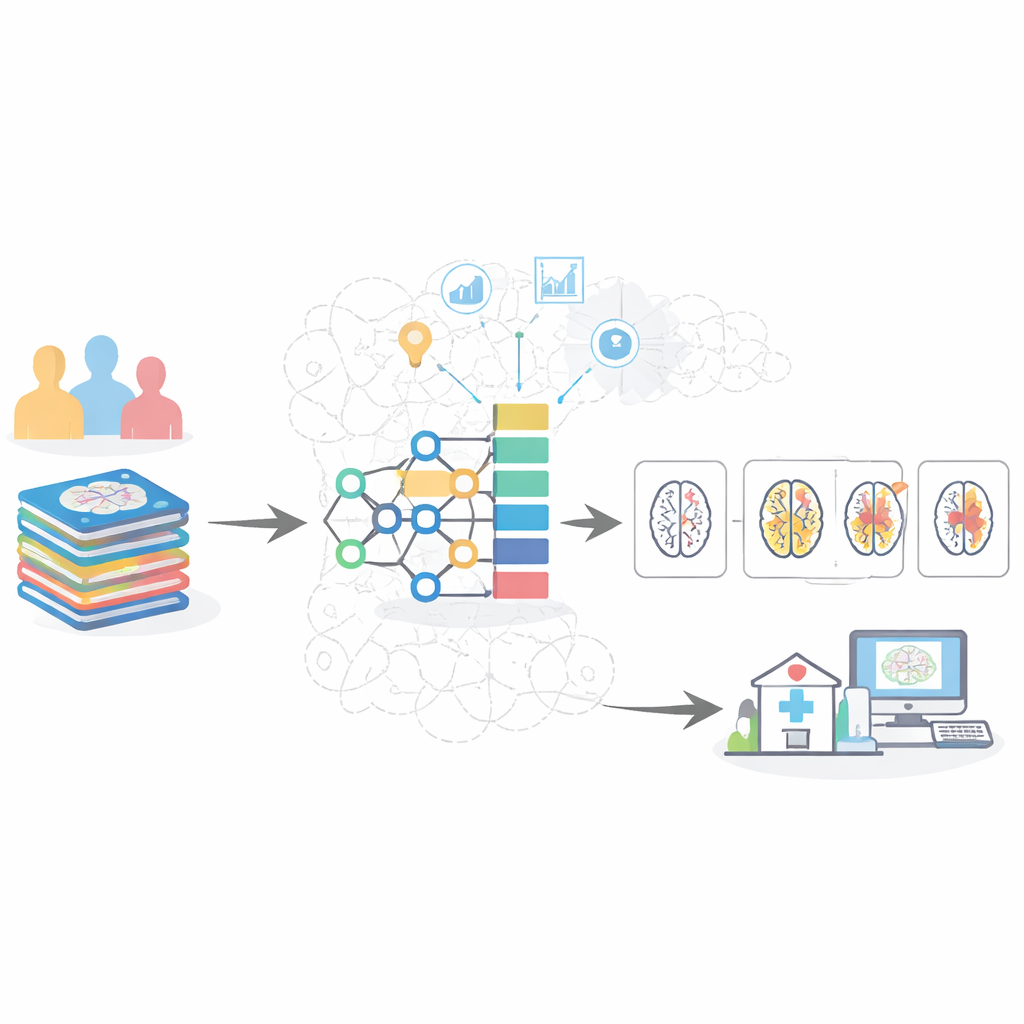
De data balanceren en de beelden opschonen
Een belangrijke uitdaging in medische data is dat niet alle ziektestadia evenveel vertegenwoordigd zijn. In deze hersenscanverzamelingen komen gezonde en zeer milde gevallen veel voor, terwijl scans met matige dementie veel zeldzamer zijn. Standaard AI-systemen neigen er dan toe het veilige pad te kiezen door de veelvoorkomende klassen te overspelen en vroeg of matig zieke gevallen te missen. Om dit tegen te gaan gebruikten de auteurs een tweestapsstrategie: ze verwijderden eerst verwarrende grensgevallen en creëerden vervolgens realistische synthetische voorbeelden van de ondervertegenwoordigde stadia. Daarnaast bereidden ze elke MRI-slice zorgvuldig voor door te filteren, de hersenen te isoleren van omliggend weefsel en helderheid en contrast te normaliseren, zodat het model zich kon concentreren op medisch relevante kenmerken zoals krimp van diepe geheugenstructuren en verwijding van met vocht gevulde ruimtes.
Ontwerp van een kleiner, slimmer netwerk
In plaats van te vertrouwen op traditionele trainingsmethoden die parameters bijstellen via wiskundige gradiënten, gebruikte het team een familie van zogenaamde afgeleide-vrije optimalisatietechnieken. Ze begonnen met een groter, conventioneel CNN en gebruikten vervolgens evolutionair zoeken en neural architecture search om een eenvoudiger ontwerp te laten ontstaan met slechts drie convolutionele lagen en veel minder filters. Bayesian optimalisatie verfijnde vervolgens hoe het netwerk getraind moest worden, terwijl gesimuleerde annealing en pruning overbodige verbindingen na de training verwijderden. Het eindresultaat, DAPA-CNN genoemd, heeft ongeveer 85% minder aanpasbare parameters dan het beginnende model, gebruikt ongeveer een kwart van het geheugen en traint in minder dan twee derde van de tijd, terwijl het toch de cruciale patronen in de scans vastlegt.
Bijna perfecte prestaties en duidelijke visuele verklaringen
Ondanks zijn kleinere omvang bleek DAPA-CNN opmerkelijk nauwkeurig. Op een grote Alzheimer-dataset bepaalde het in bijna alle gevallen correct het dementiestadium, met nauwkeurigheid en andere prestatiemaatstaven die rond de 99% lagen. Het model generaliseerde ook goed naar een aparte multicenter-dataset die op verschillende scanners was verzameld, wat suggereert dat het robuust is tegen variaties in reële beeldvorming. Om het systeem transparanter te maken voor clinici genereerden de auteurs class activation maps—heet-achtige overlays die laten zien welke hersengebieden een beslissing beïnvloedden. In vroege stadia benadrukken deze kaarten gebieden die betrokken zijn bij geheugen en waarvan bekend is dat ze als eerste verslechteren bij de ziekte van Alzheimer; in latere stadia verspreiden ze zich naar bredere corticale regio’s, wat overeenkomt met de klinische kennis over ziekteprogressie.
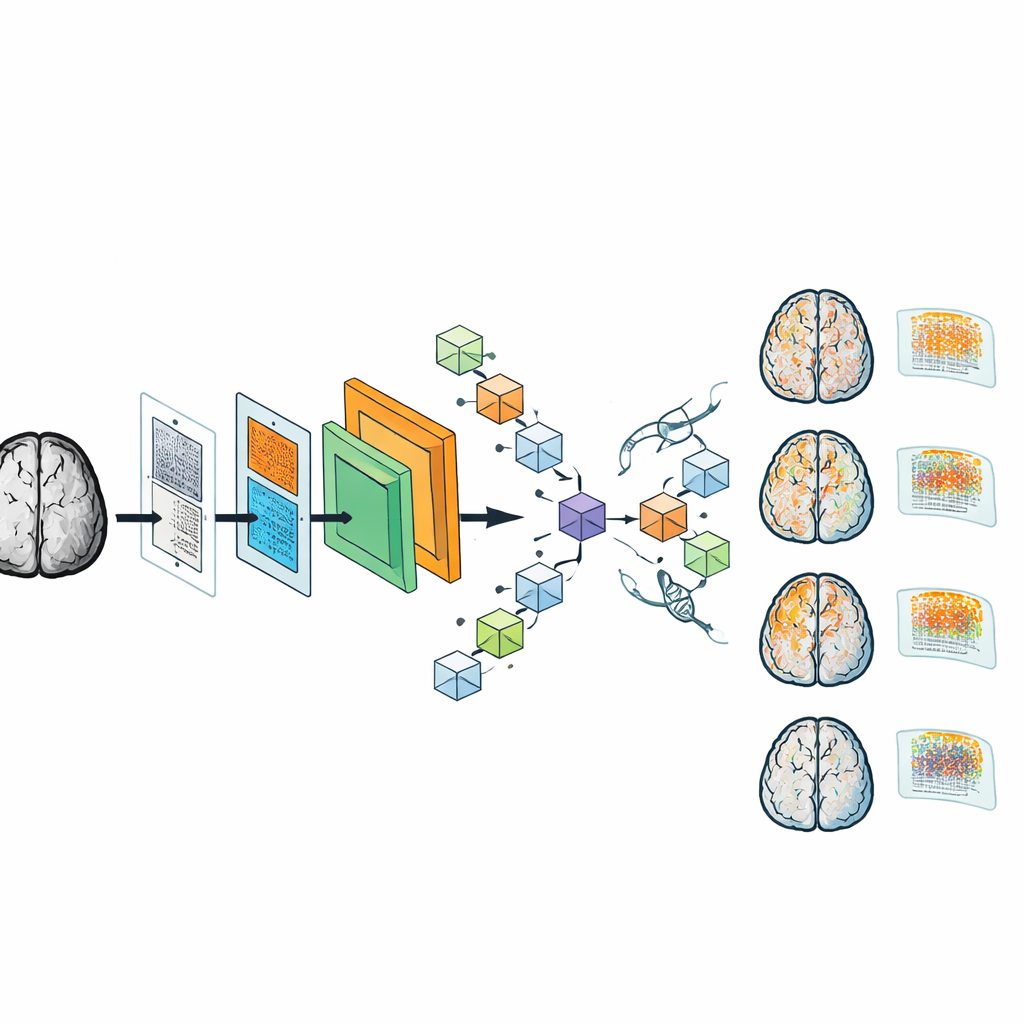
Wat dit betekent voor patiënten en klinieken
Voor niet-specialisten is de kernboodschap dat de studie een snel, compact en interpreteerbaar hulpmiddel biedt om de ernst van dementie te classificeren op basis van routinematige MRI-scans. Door de trainingsdata te balanceren en het netwerk zorgvuldig vorm te geven met afgeleide-vrije optimalisatie, creëerden de auteurs een model dat op bescheiden hardware kan draaien en toch bijna perfecte nauwkeurigheid levert en de hersengebieden belicht die aan zijn beslissingen ten grondslag liggen. Als dit bevestigd wordt in toekomstige prospectieve klinische studies, zou dergelijke technologie kunnen bijdragen aan eerdere diagnoses, consistentere staging tussen ziekenhuizen en beter volgen van hoe de ziekte van Alzheimer de hersenen in de loop van de tijd verandert.
Bronvermelding: Ganesan, S.K., Velusamy, P., Parthsarathy, P. et al. Alzheimer’s related dementia severity classification from magnetic resonance imaging using derivative-free optimization of convolutional neural network. Sci Rep 16, 10077 (2026). https://doi.org/10.1038/s41598-026-36037-9
Trefwoorden: Ziekte van Alzheimer, hersenen MRI, dementie-indeling, deep learning, AI in medische beeldvorming