Clear Sky Science · nl
Moleculaire congestie-effecten op eiwitstabiliteit in een bacterieel proteoom
Waarom het drukke leven van eiwitten ertoe doet
Binnen elke levende cel vervullen eiwitten hun taken in een omgeving zo vol met andere moleculen dat bijna de helft van het volume ingenomen kan worden. Toch bestuderen de meeste laboratoriumexperimenten eiwitten in verdunde, vrijwel lege oplossingen. Dit artikel stelt een eenvoudige maar belangrijke vraag: hoe verandert deze drukke realiteit de stabiliteit en het gedrag van eiwitten, en wat betekent dat voor hoe het leven op moleculair niveau functioneert?
Een blik in een dicht opeengepakt cellulaire wereld
Om dit te onderzoeken werkten de onderzoekers met een bacterie genaamd Cupriavidus necator, een microbe van belang voor groene technologieën zoals koolstofafvang en bioplastiekproductie. Ze openden de cellen voorzichtig, zodat honderden verschillende eiwitten dicht bij hun natuurlijke vorm bleven. Vervolgens voegden ze hoge concentraties van grote, waterminnende polymeren toe—gebruikelijke “congestie-agents” genaamd PEG, dextran en Ficoll—die vaak worden gebruikt om het dichte inwendige van cellen na te bootsen.
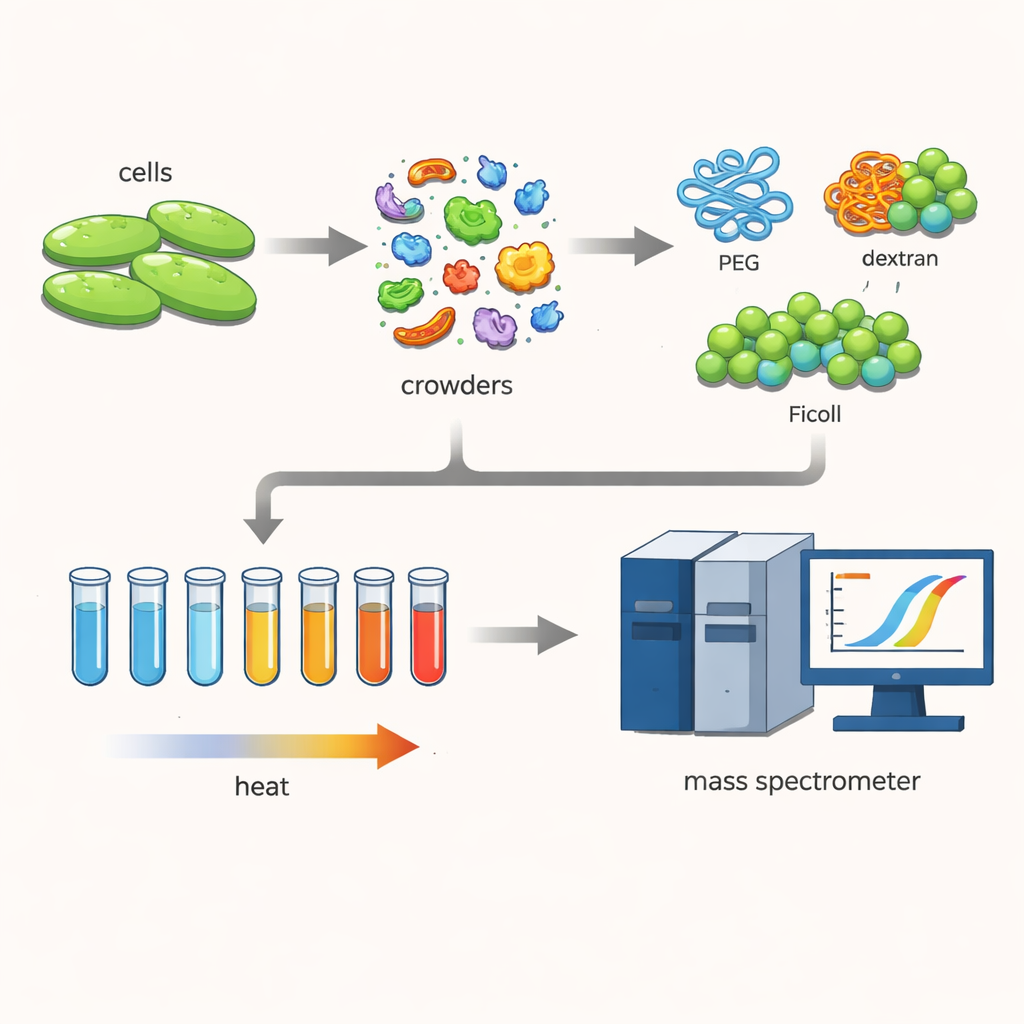
Eiwitten zien smelten
Het team gebruikte een techniek bekend als thermische proteoomprofilering. Ze verwarmden vele kleine monsters van het eiwitmengsel stapsgewijs van 30 tot 70 graden Celsius. Naarmate de temperatuur steeg, vouwden minder stabiele eiwitten zich uit en klonterden samen, waardoor ze uit de oplossing verdwenen. Door de overgebleven oplosbare eiwitten te labelen en te meten met een gevoelige massaspectrometer, konden de wetenschappers smeltcurven voor elk eiwit reconstrueren en de smelttemperatuur bepalen—het punt waarop de helft ervan de oplosbare, werkzame staat heeft verlaten. Vergelijking van deze temperaturen met en zonder congestie-agents toonde aan hoe de drukke omgeving de eiwitstabiliteit verschuift.
Een gemengd beeld: sommige eiwitten stabieler, andere kwetsbaarder
Gemiddeld verlaagde toevoeging van een van de zes polymeer-congestiemiddelen de smelttemperaturen over het bacteriële proteoom, wat wijst op een lichte algehele destabiliserende werking. Maar deze globale trend verborg een veel genuanceerder verhaal. Voor tientallen individuele eiwitten verhoogden of verlaagden de congestiemiddelen de stabiliteit duidelijk, soms met meerdere graden. De meeste eiwitten werden door slechts één van de zes reagentia beïnvloed, maar een handvol reageerde op meerdere middelen, en bijna al deze eiwitten werden ofwel consequent gestabiliseerd ofwel consequent gedestabiliseerd, wat wijst op gedeelde onderliggende eigenschappen in hun interactie met de congestiemiddelen.
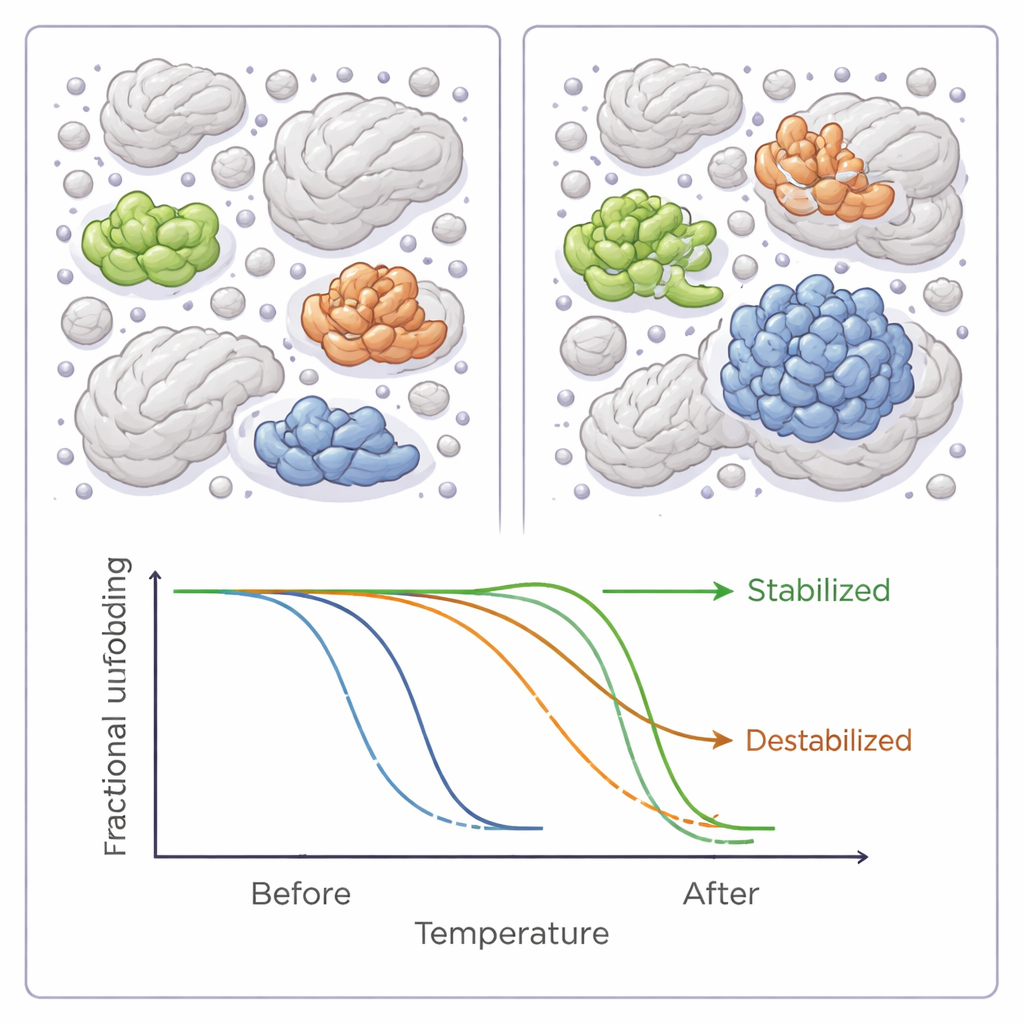
Wat een eiwit doet winnen of verliezen in een menigte
Wanneer de auteurs dichter naar de eigenschappen van deze gevoelige eiwitten keken, kwamen er patronen naar voren. Eiwitten die in drukke omstandigheden stabieler werden, neigden meer hydrofoob te zijn—dat wil zeggen, ze hebben meer waterafstotende oppervlakken—en waren vaker klassieke enzymen met goed gedefinieerde actieve centra. Ze waren ook vaker betrokken bij eiwit‑eiwitinteracties of droegen chemische modificaties die hun functie bijsturen. Gedestabiliseerde eiwitten waren daarentegen gemiddeld kleiner en minder versierd met dergelijke modificaties. Deze bevindingen sluiten aan bij computermodellen en andere experimenten die suggereren dat congestie sommige eiwitten kan bevoordelen terwijl het anderen kwetsbaarder maakt, afhankelijk van grootte, vorm en hoe ze normaal gesproken met partners interageren.
Voorbij simpele compressie: hoe congestiemiddelen echt werken
Traditionele verklaringen voor moleculaire congestie richten zich op “uitsloten volume”, het idee dat grote moleculen simpelweg minder ruimte overlaten en eiwitten aansporen om gevouwen te blijven. Als dat het hele verhaal was, zou men verwachten dat congestiemiddelen vooral eiwitten stabiliseren en sterke verbanden zien met hoe log of viskeus de middelen zijn. In plaats daarvan zagen de auteurs slechts zwakke verbanden met de grootte en stroperigheid van de polymeren. Hun gegevens pasten beter bij een beeld van “preferentiële uitsluiting”: congestiemiddelen en eiwitten vermijden elkaar chemisch, wat indirect bepaalde gevouwen toestanden bevoordeelt maar ook delicate interacties kan verstoren die andere eiwitten stabiel houden. Kortom, het is niet alleen fysieke compressie, maar subtiele chemische duw‑en‑trek die het eiwitgedrag vormt.
Wat dit betekent voor het begrijpen van de chemie van het leven
Voor niet‑specialisten is de kernboodschap dat eiwitten in cellen niet volledig begrepen kunnen worden in isolatie, zwemmend in helder buffer. De dichte moleculaire jungle om hen heen kan sommige eiwitten robuuster maken en andere kwetsbaarder, waardoor de werking van hele reactienetwerken verandert. Deze studie, door stabiliteitsveranderingen voor honderden eiwitten tegelijk te meten, laat zien dat congestie-effecten complex en eiwit‑specifiek zijn, en waarschijnlijk evenzeer door directe interacties als door eenvoudige verpakking worden gedreven. Wanneer onderzoekers medicijnen, industriële enzymen of ontworpen microben ontwikkelen, zal het erkennen van deze drukke realiteit cruciaal zijn om te voorspellen hoe eiwitten zich daadwerkelijk gedragen in levende systemen.
Bronvermelding: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
Trefwoorden: moleculaire congestie, eiwitstabiliteit, thermische proteoomprofilering, bacterieel proteoom, cellulaire omgeving