Clear Sky Science · nl
NEGR1‑tekort verandert glutamaatsignalering en kynurenine‑pad in een muismodel voor psychiatrische aandoeningen
Waarom deze hersenstudie ertoe doet
Veel voorkomende psychische ziekten, van depressie tot schizofrenie, hangen samen met subtiele veranderingen in hoe zenuwcellen met elkaar communiceren. Deze studie onderzoekt één risicogen, genaamd NEGR1, bij muizen om te zien hoe het ontbreken daarvan hersenchemie en gedrag verandert. Door te volgen hoe deze muizen bewegen na een middel dat kortstondig een belangrijke hersenreceptor verstoort, en door gerelateerde hersenchemicaliën te meten, onthullen de onderzoekers hoe genetica, sekse en hersenstofwisseling samen kwetsbaarheid voor psychiatrische aandoeningen kunnen vormen.
Een gen dat hersensignalen in balans houdt
Het NEGR1-gen maakt een celmembraaneiwit dat zenuwcellen helpt verbindingen te vormen en te stabiliseren. Eerder werk toonde aan dat het verwijderen van dit gen bij muizen de hersenstructuur verandert, bepaalde remmende (GABA) verbindingen vermindert en de respons op dopamine‑gerelateerde middelen zoals amfetamine verandert. Omdat deze veranderingen wijzen op een verschuiving naar sterkere exciterende signalen, richtte het team zich op een ander belangrijk exciterend systeem: glutamaat en zijn NMDA‑receptoren, die centraal staan bij leren, geheugen en flexibel gedrag. Ze onderzochten ook het “kynurenine‑pad”, een stofwisselingsroute die het aminozuur tryptofaan afbreekt tot verbindingen die NMDA‑receptoren kunnen versterken of remmen.
Gedragstesten met een bewustzijnsveranderend middel
Om de functie van NMDA‑receptoren te onderzoeken, gebruikten de onderzoekers MK‑801, een bekend middel dat deze receptoren kort blokkeert en aspecten van glutamaatonevenwicht kan nabootsen die gezien worden bij psychiatrische aandoeningen. Mannelijke en vrouwelijke muizen droegen ofwel het normale Negr1-gen of misten het volledig. De dieren kregen dagelijkse injecties MK‑801 en werden getest in een open veld‑arena, waar hun totale beweging, tijd in de hoeken en ronddraaiende bewegingen automatisch werden geregistreerd. Bij drug‑naïeve mannetjes veroorzaakte een enkele dosis MK‑801 een sterkere activiteitspiek bij Negr1-deficiënte muizen dan bij normale muizen, wat suggereert dat hun hersenen ongewoon gevoelig waren voor deze verstoring van glutamaatsignalering.
Een verrassend patroon van snelle tolerantie
Bij herhaalde toediening veranderde het patroon. Bij mannetjes steeg de activiteit op sommige dagen maar daalde op elke tweede dag, wat een zigzagpatroon vormde dat wijst op snelle, gedeeltelijke tolerantie voor de effecten van het middel. Over negen dagen lieten normale mannetjes een toenemende respons zien die past bij sensibilisatie, terwijl Negr1-deficiënte mannetjes een afgezwakte opbouw van activiteit en mildere dag‑tot‑dag veranderingen toonden, wat wijst op veranderde gevoeligheid van NMDA‑receptoren. Vrouwtjes van beide genotypen pasten zich nog sneller aan: rond dag vijf produceerde MK‑801 geen sterke gedragsveranderingen meer, waarna de behandeling werd gestopt. Over alle metingen had sekse een grote invloed, en duidelijke genotypeffecten traden vooral bij mannetjes op.
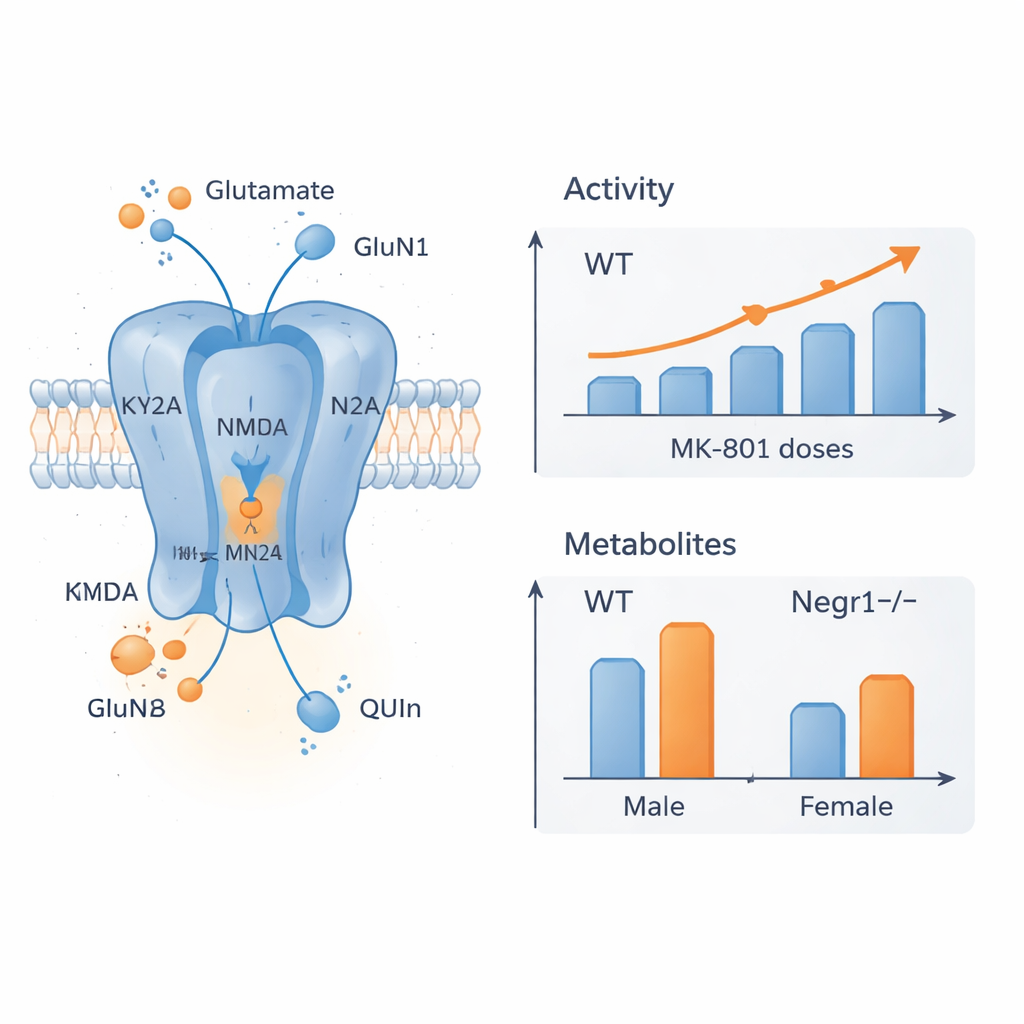
Verschuivingen in receptoren en hersenchemicaliën
Om te achterhalen wat deze gedragsverschillen verklaarde, mat het team de genactiviteit van belangrijke NMDA‑receptorondereenheden en van een enzym dat D‑serine produceert, een co‑signaal voor deze receptoren. Ze concentreerden zich op hersengebieden die cruciaal zijn voor stemming en cognitie: de frontale cortex en de hippocampus. In de frontale cortex toonden vrouwelijke Negr1-deficiënte muizen behandeld met MK‑801 verlaagde expressie van kernreceptorondereenheden, wat suggereert dat hun hersenen de receptor‑samenstelling aanpassen als reactie op zowel de mutatie als het middel. In de hippocampus van mannetjes vertoonden Negr1-deficiënte muizen een hogere basale expressie van bepaalde NMDA‑ondereenheden, in lijn met eerder bewijs voor meer beschikbare receptoren; MK‑801‑behandeling bracht deze niveaus vervolgens terug richting normaal. Parallel daaraan toonden gedetailleerde chemische analyses van bloed en meerdere hersengebieden dat verschillende metabolieten van het kynurenine‑pad en glutamaat zelf op een seks‑ en regiogebaseerde manier waren veranderd, waarbij de frontale cortex het meest werd getroffen en sommige veranderingen met de leeftijd sterker werden.
Wat dit betekent voor het begrijpen van geestelijke ziekten
Gezamenlijk portretteren deze bevindingen NEGR1 als een moleculair organisator die helpt exciterende en inhiberende hersensignalen in balans te houden, deels door de functie van NMDA‑receptoren en tryptofaanmetabolisme te beïnvloeden. Wanneer Negr1 ontbreekt, reageren muizen anders op NMDA‑receptorblokkade, vertonen ze sekseafhankelijke verschuivingen in hersenchemicaliën en ontwikkelen ze geleidelijk tolerantie op eigenaardige manieren. Voor een niet‑specialistische lezer is de kernboodschap dat één risicogen niet op zichzelf werkt: de effecten hangen af van sekse, hersengebied en metabolische staat. Dit werk versterkt het idee dat het richten op paden die met NEGR1 verband houden — in plaats van alleen op individuele receptoren — mogelijk uiteindelijk kan helpen behandelingen op maat te maken voor psychische aandoeningen die worden gekenmerkt door glutamaatonevenwicht.
Bronvermelding: Kuuskmäe, C., Mikheim, K., Mohammadrahimi, N. et al. Negr1 deficiency alters glutamate signalling and kynurenine pathway in a mouse model of psychiatric disorders. Sci Rep 16, 5317 (2026). https://doi.org/10.1038/s41598-026-35968-7
Trefwoorden: NEGR1‑gen, NMDA‑receptor, glutamaatsignalering, kynurenine‑pad, psychiatrische aandoeningen