Clear Sky Science · nl
APOBEC3B verbetert de doeltreffendheid van PARP-remmers bij het uitroeien van ovariumkankerstamcellen
Waarom dit onderzoek van belang is voor patiënten met eierstokkanker
Veel vrouwen met gevorderde eierstokkanker reageren aanvankelijk goed op moderne middelen genaamd PARP-remmers, die inspelen op zwaktes in het DNA-herstel van de tumor. Na verloop van tijd keert de ziekte echter vaak terug, omdat kankercellen leren deze behandelingen te overleven. Deze studie onderzoekt een onverwachte bondgenoot in de kankercellen zelf — een DNA-bewerkend enzym genaamd APOBEC3B — en toont aan dat het, onder de juiste omstandigheden, eierstokkankerstamcellen juist gevoeliger kan maken voor eliminatie met PARP-remmers.
Een dodelijke kanker die steeds terugkeert
High-grade serous eierstokkanker is de meest voorkomende en meest dodelijke vorm van eierstokkanker. Meestal wordt ze laat ontdekt, wanneer de ziekte zich al in de buikholte heeft verspreid, en meer dan 80% van de patiënten met gevorderde ziekte krijgt binnen vijf jaar een recidief. Een belangrijke verdachte achter die terugkeer is een kleine populatie van "kankerstamcellen." Deze cellen kunnen zichzelf vernieuwen, chemotherapie overleven en tumoren na behandeling opnieuw opbouwen. Begrijpen wat deze stamachtige cellen resistent maakt — en hoe ze te bestrijden — is essentieel om de lange termijn overleving te verbeteren.
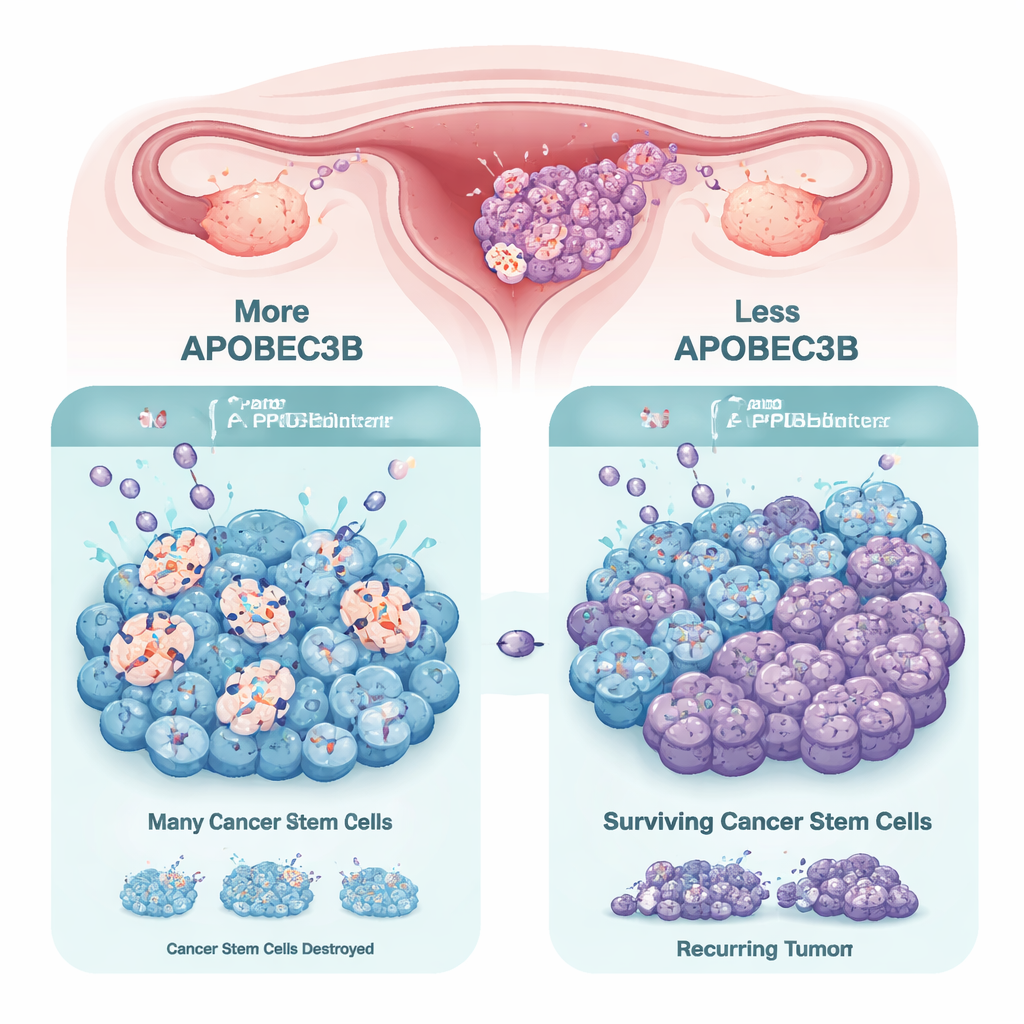
Een muterend enzym met een dubbelrol
De APOBEC3-familie van enzymen helpt normaal gesproken onze cellen te beschermen tegen virussen door specifieke DNA-letters te wijzigen, wat mutaties kan invoeren. In veel kankers is één lid, APOBEC3B, overactief en draagt het bij aan DNA-schade en genetische chaos, wat tumorevolutie en therapieresistentie kan stimuleren. In eierstoktumoren en patiënt-derived modellen bevestigden de onderzoekers dat APOBEC3B gewoonlijk het meest voorkomende APOBEC3-enzym is. Echter, bij vergelijking van gewone tumorcellen met kankerstamcelachtige "tumorsferen" gekweekt in 3D, ontdekten ze dat de stamachtige cellen consequent APOBEC3B naar beneden bijstellen. Dit suggereert dat kankerstamcellen hun mutatielast kunnen verminderen om hun overleving en zelfvernieuwingsvermogen te behouden.
APOBEC3B minder actief maakt stamcellen taaier
Om te testen of APOBEC3B daadwerkelijk invloed heeft op stamachtigheid, gebruikte het team genetische hulpmiddelen om de expressie ervan te onderdrukken in eierstokkanker modellen afkomstig van patiënten en in gevestigde cellijnen. Wanneer APOBEC3B-niveaus werden verlaagd, vormden kankercellen efficiënter tumorsferen en vertoonden ze hogere niveaus van klassieke stammerkers zoals SOX2, OCT4 en NANOG. Het aandeel cellen met stamcelachtige eigenschappen nam toe, wat aangeeft dat verlies van APOBEC3B kankercellen helpt schakelen naar een veerkrachtiger, stamachtig stadium. In muizen groeiden tumoren zonder APOBEC3B op zichzelf niet sneller, maar ze gedroegen zich wel anders wanneer behandeld met PARP-remmers.
Meer APOBEC3B, meer schade — en betere medicijnrespons
De onderzoekers vroegen zich vervolgens af hoe APOBEC3B de werking van PARP-remmers zoals Olaparib beïnvloedt, die werken door DNA-herstel te blokkeren en kankercellen te dwingen te vervallen door dodelijke DNA-schade. In meerdere eierstokkankercellijnen maakte vermindering van APOBEC3B de cellen resistenter tegen PARP-remmers, vooral in 3D-tumorsferen die verrijkt waren voor stamachtige cellen. Omgekeerd maakte verhoogde APOBEC3B sommige cellen gevoeliger voor PARP-remmers, waardoor hun overleving sterk daalde. In muismodellen krompen of vertraagden tumoren met normale APOBEC3B dramatisch onder Olaparib, terwijl APOBEC3B-deficiënte tumoren doorgroeiden ondanks behandeling. Moleculaire analyses toonden waarom: hoge APOBEC3B-niveaus verhoogden replicatiestress en dubbelstrengsbreuken in het DNA, en activeerden DNA-schade signaleringspaden. Wanneer APOBEC3B werd onderdrukt, namen door PARP-remmers geïnduceerde DNA-schade, checkpointactivatie en replicatiestress allemaal af, en hadden cellen meer kans om veilig in de celcyclus vast te lopen in plaats van te sterven.
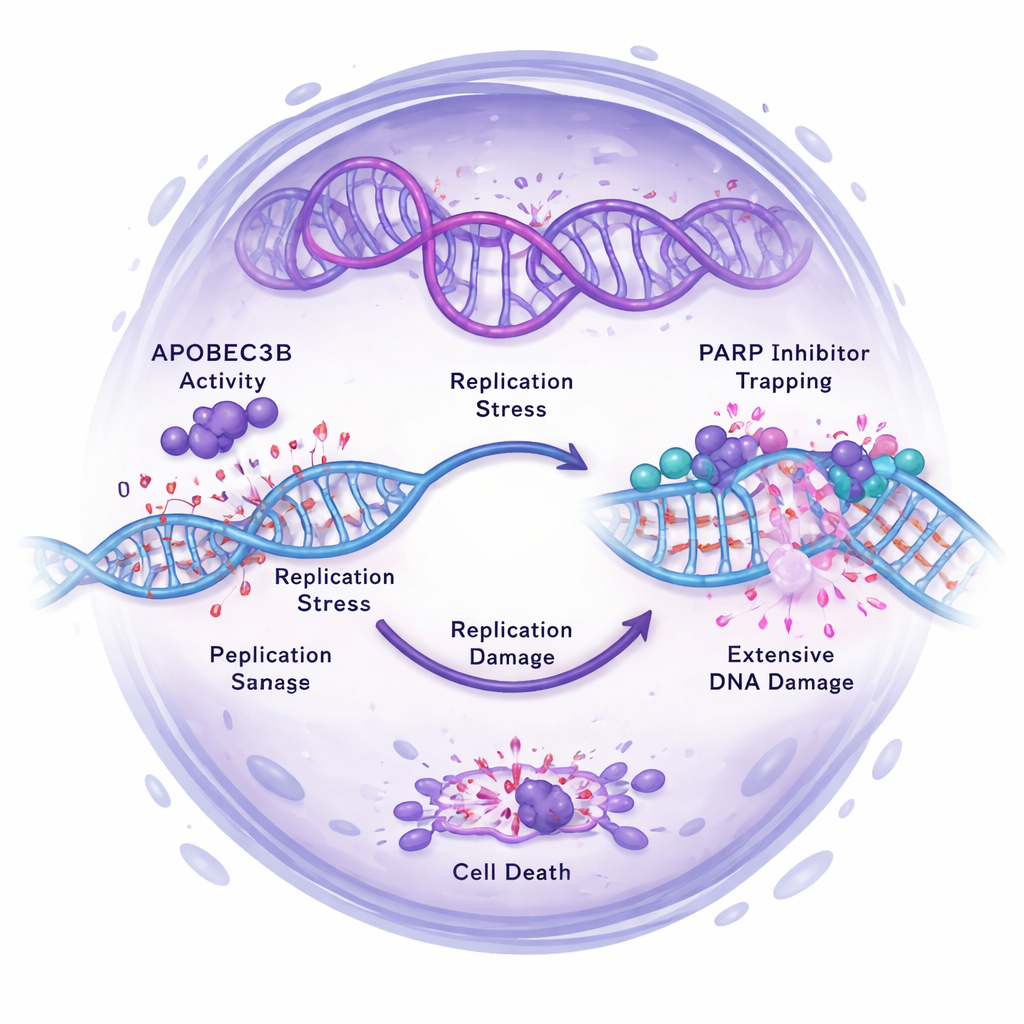
Een nieuwe manier om over resistentie en behandelontwerp na te denken
Dieper gravend met RNA-sequencing vonden de onderzoekers dat de combinatie van verlies van APOBEC3B en PARP-remming veel genen herbedrade die betrokken zijn bij DNA-replicatie en herstel, wat het idee ondersteunt dat APOBEC3B de schadelijke effecten van PARP-remmers op het genoom van kankercellen versterkt. Ze testten ook of een ander herstelenzym, UNG, noodzakelijk was voor dit effect en vonden dat de gevoeligheid voor PARP-remmers in cellen met hoge APOBEC3B grotendeels onafhankelijk was van UNG. Over het geheel genomen wijzen de gegevens op door APOBEC3B aangedreven replicatiestress — niet alleen de mutagene activiteit — als de belangrijkste partner die PARP-remmers helpt eierstokkankerstamcellen te doden.
Wat dit betekent voor patiënten en toekomstige therapieën
Voor een leek is de boodschap dat niet alle genetische chaos in een tumor slecht nieuws is. In deze studie maakten hogere niveaus van het muterende enzym APOBEC3B eierstokkankerstamcellen juist kwetsbaarder voor PARP-remmers door hun DNA-herstelcapaciteit te overbelasten. Wanneer APOBEC3B werd teruggeschroefd, werden kankerstamcellen meer stamachtig en beter in staat een behandeling te doorstaan. Deze bevindingen suggereren dat het meten van APOBEC3B-niveaus kan helpen voorspellen welke patiënten het meest profiteren van PARP-remmers, en dat het timen of combineren van toekomstige APOBEC3B-gerichte middelen met PARP-remmers voorzichtig moet gebeuren. Het benutten van het "zelfsabotage"-effect van APOBEC3B op kankercellen kan nieuwe strategieën openen om terugkeer te voorkomen en de wortels van eierstoktumoren effectiever uit te roeien.
Bronvermelding: Rivera, M., Liu, L., Enlund, S. et al. APOBEC3B enhances the efficacy of PARP inhibitors in elimination of ovarian cancer stem cell. Sci Rep 16, 5194 (2026). https://doi.org/10.1038/s41598-026-35939-y
Trefwoorden: eierstokkanker, PARP-remmers, kankerstamcellen, APOBEC3B, medicatieresistentie