Clear Sky Science · nl
Isolatie, karakterisering en potentiële toepassingen van een nieuw bacteriofaag gericht op beta-lactamresistente Staphylococcus saprophyticus
Waarom piepkleine virussen kunnen helpen bij hardnekkige infecties
Urineweginfecties behoren tot de meest voorkomende bacteriële aandoeningen wereldwijd, en veel gevallen worden nu veroorzaakt door ziekteverwekkers die standaardantibiotica negeren. Een van die daders, Staphylococcus saprophyticus, leeft onschadelijk op onze huid en in de genitale streek maar kan in de urinewegen terechtkomen en pijnlijke, terugkerende infecties veroorzaken, vooral bij vrouwen. Deze studie onderzoekt een ongewone bondgenoot tegen deze microbe: een nieuw ontdekte virus dat bacteriën infecteert, een bacteriofaag genoemd, dat drugresistente S. saprophyticus kan doden en zijn beschermende slijmlaag en geurveroorzakende kolonies op huid en textiel kan verwijderen.
Een verborgen boosdoener in het dagelijks leven
Staphylococcus saprophyticus is een normale bewoner van het menselijk lichaam en koloniseert de darm, urethra, cervix en huid. Toch is het ook de op één na meest voorkomende oorzaak van urineweginfecties bij vrouwen en kan het oudere mannen aantasten. Het vormt kleverige biofilms—dichte bacteriegemeenschappen die aan oppervlakken vastgeplakt zitten—wat het moeilijker maakt voor antibiotica om te werken en de microbe helpt zich aan blaas- en urethracellen te hechten. Veel stammen zijn nu resistent tegen meerdere belangrijke beta-lactamantibiotica, waaronder sommige die zijn ontwikkeld om bestand te zijn tegen bacteriële penicilline-afbrekende enzymen. Buiten urineweginfecties is deze soort in verband gebracht met bederf van voedsel, huid- en ooginfecties, lichaamsgeur en zelfs vruchtbaarheidsproblemen bij mannen, wat het tot een breder hygiëne- en gezondheidsprobleem maakt.
Een virus vinden dat resistente bacteriën besluipt
Om een natuurlijke vijand van deze bacterie te vinden is de onderzoeksgroep eerst een hardnekkige, beta-lactamresistente S. saprophyticus-stam geïsoleerd uit stinkende sokken. Vervolgens screenden ze rioolmonsters—een rijke bron van bacteriële virussen—en identificeerden een faag die ze ØPh_SS01 noemden en die specifiek deze stam aanvalt. Onder de elektronenmicroscoop toonde de faag een klassiek kop-en-staart-structuur die typerend is voor veel bacteriële virussen. Laboratoriumtests lieten zien dat ØPh_SS01 ook meerdere verwante staphylokokken en één Bacillus-soort kan infecteren, wat het een matig breed gastbereik geeft dat nuttig kan zijn om meerdere lastige huid- en omgevingsbacteriën aan te pakken terwijl het veel gerichter blijft dan standaardantibiotica.
Een duurzame en doeltreffende bacteriedoder
ØPh_SS01 bleek verrassend taai. Hij bleef actief over een breed bereik van zuurgraad, temperaturen van koelkastkoud tot lichaamstemperatuur en hoge zoutconcentraties, en verdroeg behandeling met organische oplosmiddelen die werden gebruikt om hem te zuiveren. In vloeibare cultuur leidde toevoeging van de faag aan S. saprophyticus tot ongeveer een zeven-log (tien-miljoenvoudige) afname van het aantal bacteriën binnen 24 uur. Hij werkte ook goed bij het voorkomen en afbreken van biofilms: bij een royale faagodose voorkwam hij ruwweg driekwart van de biofilmvorming en verwijderde hij ongeveer tweederde van reeds gevormde biofilm. Tests op huidachtige humane cellen en cellen afgeleid van de blaas toonden aan dat de faag de zoogdiercellen niet merkbaar schaadde, wat zijn veiligheid ondersteunt voor mogelijk gebruik op of in het lichaam.
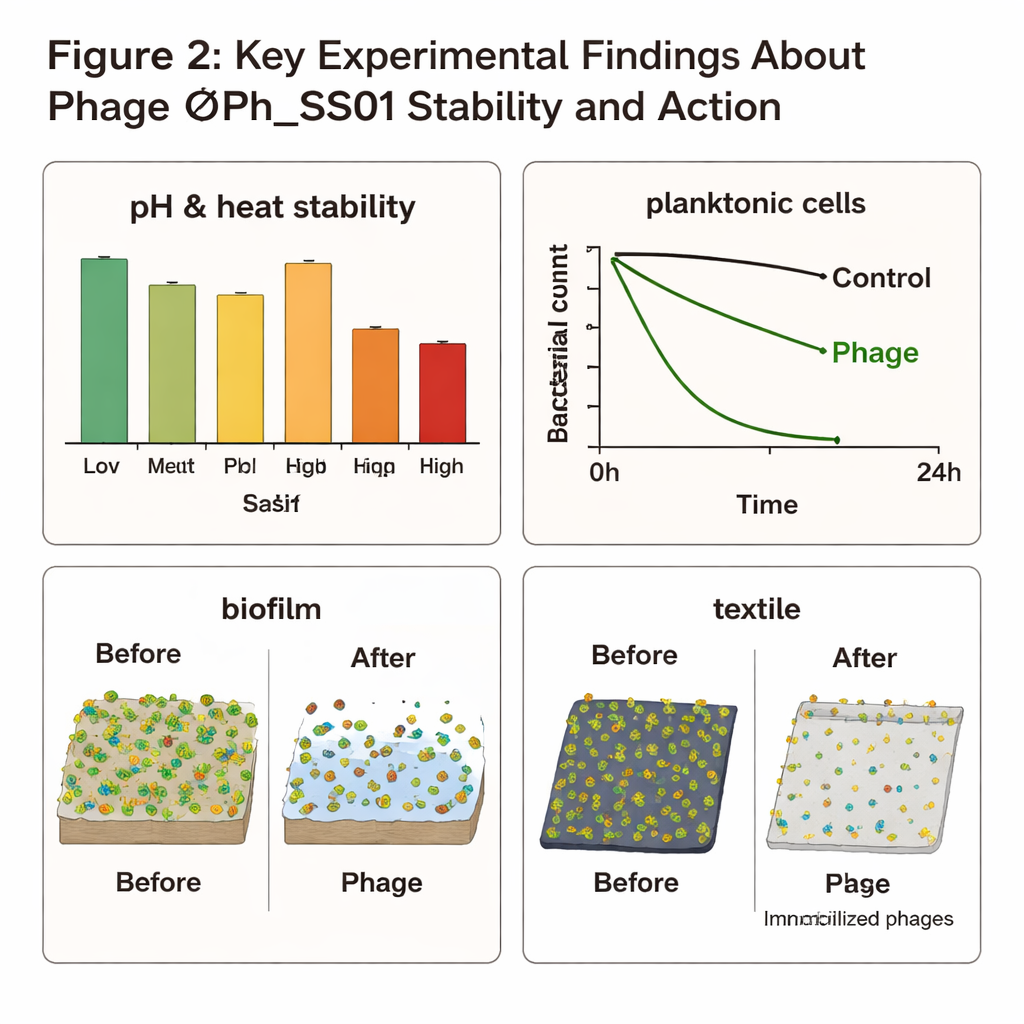
Van laboratoriumbank naar textiel en hygiëne
Het team onderzocht ook hoe deze faag in de praktijk gebruikt zou kunnen worden. Toen ØPh_SS01 op stukjes katoentextiel werd vastgezet en vervolgens werd blootgesteld aan S. saprophyticus, nam het aantal levende bacteriën op de stof in de loop van de tijd met ongeveer zeven ordes van grootte af, en in veel monsters werden de bacteriën niet meer detecteerbaar. Dit proof-of-concept suggereert dat faag-gecoate materialen—zoals sokken, ondergoed, maandverband of verbandmiddelen—actief de bacteriële belasting en bijbehorende geur of infectierisico zouden kunnen verminderen, in plaats van alleen vocht te absorberen. Genomanalyse toonde aan dat ØPh_SS01 een eerder niet-gerapporteerd lid is van de klasse Caudoviricetes met een dubbelstrengs DNA-genoom van 47 kilobasen en genen die passen bij een temperaat levenspatroon, wat betekent dat hij ofwel bacteriën vernietigt of zich stilletjes in hun DNA kan integreren.
Wat dit betekent voor alledaagse gezondheid
Voor niet-specialisten is de kernboodschap dat zorgvuldig gekozen “goede” virussen kunnen worden gebruikt als precisie-instrumenten tegen “slechte” bacteriën die niet langer reageren op gangbare antibiotica. Deze nieuwe faag, ØPh_SS01, kan in laboratoriumtesten een UWI-geassocieerde, drugresistente bacterie drastisch verminderen, zijn biofilms aantasten en functioneren wanneer hij aan textiel is gebonden zonder menselijke cellen te schaden. Hoewel meer werk nodig is om een temperate faag om te zetten in een puur bacteriedodend middel en om het in dieren en mensen te testen, wijst de studie op toekomstige zepen, sprays, verbanden en kleding die actief zelfdesinfecterend zijn—wat kan helpen infecties te voorkomen en onze afhankelijkheid van steeds minder betrouwbare antibiotica te verminderen.
Bronvermelding: Gopika, O., Sarat, N., Manikandan, M. et al. Isolation, characterisation and potential applications of a novel bacteriophage targeting beta-lactam-resistant Staphylococcus saprophyticus. Sci Rep 16, 7460 (2026). https://doi.org/10.1038/s41598-026-35899-3
Trefwoorden: urineweginfecties, bacteriofaagtherapie, Staphylococcus saprophyticus, antibioticaresistentie, biofilmcontrole