Clear Sky Science · nl
KIN17 bevordert het ontstaan en de voortgang van nierkankertumoren via de PI3K-AKT-mTOR-route
Waarom deze nierkankerstudie ertoe doet
Nierkanker wordt steeds vaker opgespoord, maar voor veel patiënten blijft de ziekte moeilijk te beheersen zodra ze is uitgezaaid. Deze studie kijkt tot op moleculair niveau in kankercellen om te begrijpen wat niertumoren doet groeien en binnendringen, en of een experimenteel geneesmiddel dat proces kan remmen. De bevindingen wijzen op een weinig bekend eiwit, KIN17, als nieuwe aanjager van nierkanker en suggereren een manier om het indirect aan te pakken met een orale behandeling.
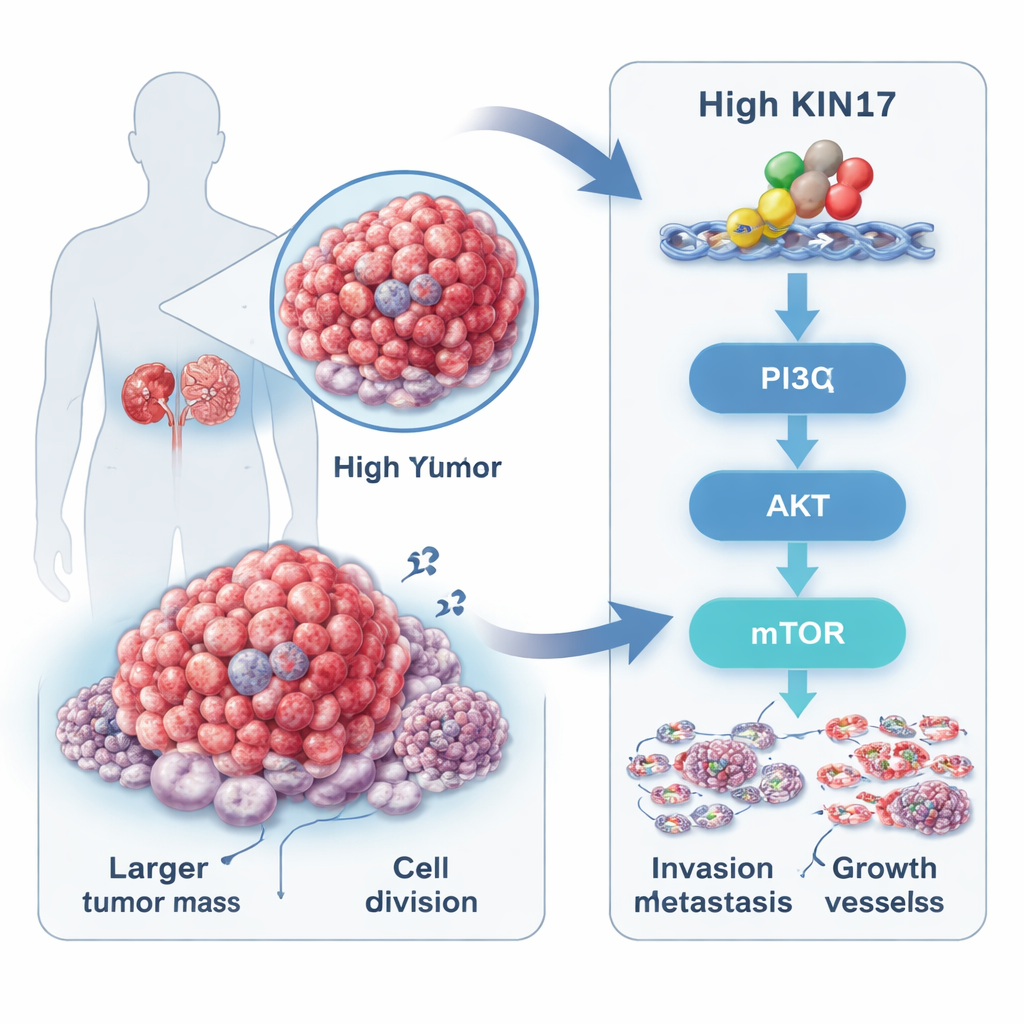
Een verborgen drijfveer in niertumoren
Niercelcarcinoom, de meest voorkomende vorm van nierkanker, begint vaak zonder klachten en wordt veelal laat ontdekt. De onderzoekers richtten zich op een eiwit genaamd KIN17, lang bekend om zijn rol bij het beschermen en kopiëren van DNA, maar pas recent gekoppeld aan meerdere andere kankertypen. Door openbare kankerdatabases en tumormonsters van 88 patiënten te analyseren, vonden ze dat KIN17-niveaus veel hoger waren in niertumoren dan in aangrenzend niet-kankergewebe. Patiënten met tumoren met veel KIN17 hadden meestal grotere tumoren, hoger gradige ziekte, gevorderdere stadia en meer uitzaaiingen, en een kortere overleving dan degenen met weinig KIN17. Dit patroon suggereerde dat KIN17 geen bijstander is, maar nauw verbonden met hoe agressief een tumor wordt.
KIN17 testen in kankercellen
Om te ontdekken wat KIN17 precies doet in nierkankercellen, bouwde het team laboratoriumcelijnen die KIN17 ofwel naar beneden konden brengen of juist konden verhogen. Wanneer ze KIN17 verminderden, groeiden de cellen langzamer, vormden ze minder kolonies en konden ze zich minder goed verplaatsen en door kunstmatige membranen heen invaseren. Meer van deze cellen bleven in de rustfase van de celcyclus steken en gingen dood, met hogere niveaus van geprogrammeerde celdood. Het omgekeerde gebeurde wanneer KIN17 werd overgeproduceerd: cellen vermenigvuldigden zich sneller, kopieerden hun DNA gemakkelijker, sloten krasachtige openingen in celmonolagen sneller en invadeerden agressiever. Deze experimenten toonden aan dat KIN17 fungeert als het gaspedaal voor groei en spreiding van nierkankercellen.
Een groeipad op heterdaad betrapt
De onderzoekers vroegen zich vervolgens af hoe KIN17 deze invloed uitoefent. Hun genactiviteitsonderzoeken en eiwittesten wezen op een bekend groeien overlevingsnetwerk in cellen, de PI3K–AKT–mTOR-route. Deze route wordt vaak vergeleken met een centraal regelcentrum dat cellen aangeeft wanneer ze moeten groeien, delen en afsterven vermijden. Nierkankercellen met veel KIN17 hadden sterkere "aan"-signalen — chemische labels genaamd fosfaten — op sleutelcomponenten van deze route, hoewel de totale hoeveelheid van deze eiwitten niet veranderde. Wanneer KIN17 werd geremd, daalden deze activatielabels en verschoof ook het patroon van moleculen die betrokken zijn bij celbeweging en invasie. In muisexperimenten groeiden tumoren opgebouwd uit KIN17-rijke cellen groter en sneller, en weefselkleuring liet zien dat dezelfde groeiroute in die tumoren sterk geactiveerd was.
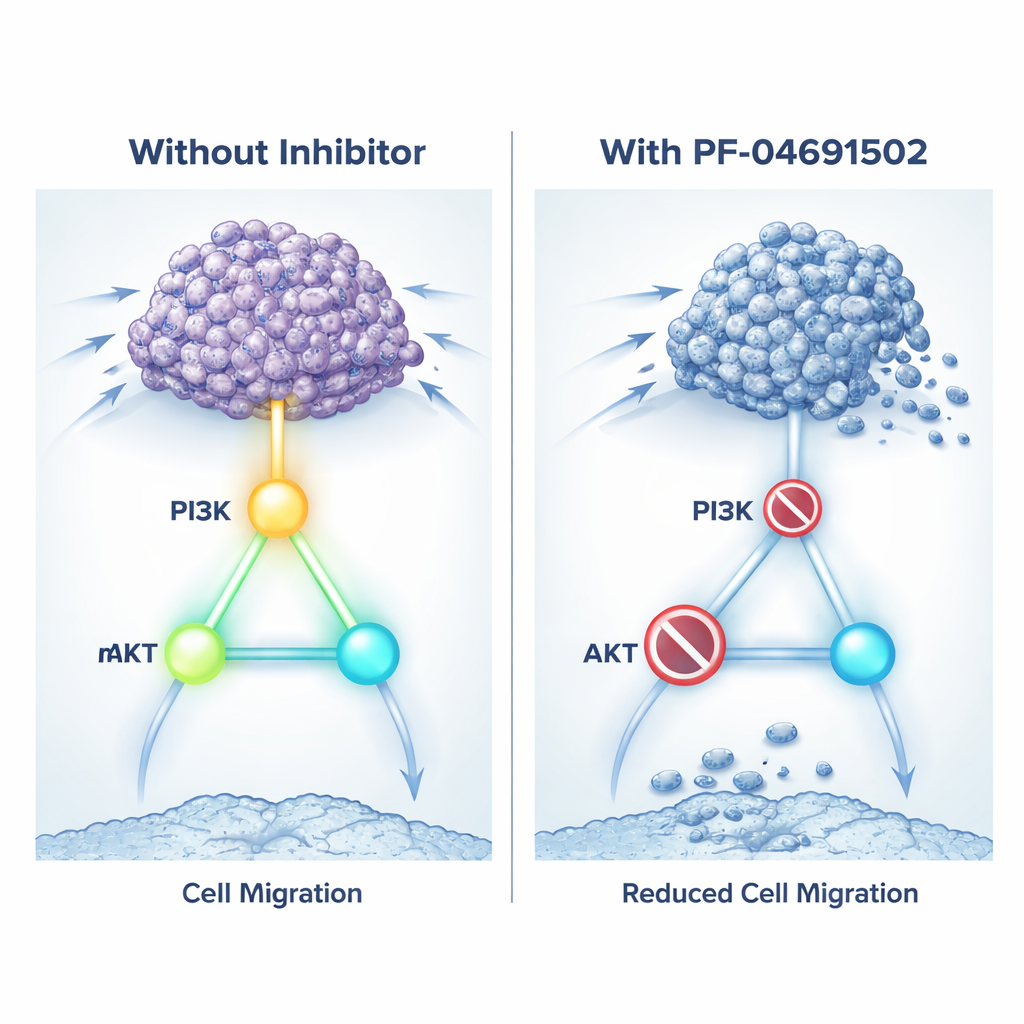
Het signaal dempen met een dubbelrichtingsremmer
Aangezien KIN17 direct remmen met bestaande middelen nog niet mogelijk is, testte het team een andere tactiek: de groeiroute die KIN17 lijkt te sturen uitschakelen. Ze gebruikten PF‑04691502, een experimenteel middel dat zowel PI3K als mTOR blokkeert, twee sleutelschakelaars in de route. In kweekschalen vertraagde behandeling van KIN17-rijke nierkankercellen met deze remmer hun groei, verminderde hun migratie- en kolonievormend vermogen en duwde meer cellen richting celdood. Het middel sneed ook de activatielabels op PI3K, AKT en mTOR weg en verlaagde niveaus van invasie-gerelateerde eiwitten. Bij muizen met niertumoren verkleinden dagelijkse doses PF‑04691502 tumoren die KIN17 overproduceerden en verminderden markers van celdeling terwijl signalen van celdood toenamen. In wezen kon het geneesmiddel de schadelijke effecten van KIN17 dempen door zijn favoriete groeipad stil te leggen.
Wat dit voor patiënten zou kunnen betekenen
Voor mensen met nierkanker suggereren deze bevindingen twee hoopgevende ideeën. Ten eerste kan het meten van KIN17 in tumormonsters artsen helpen inschatten hoe agressief een kanker is en hoe waarschijnlijk uitzaaiing is. Ten tweede kunnen tumoren die sterk afhankelijk zijn van KIN17 bijzonder gevoelig zijn voor middelen die de PI3K–AKT–mTOR-route raken, zoals PF‑04691502 of vergelijkbare dubbelgerichte remmers die al in klinische studies voor andere kankers worden onderzocht. Hoewel er veel werk resteert voordat een nieuwe behandeling de kliniek bereikt, brengt deze studie een heldere keten van gebeurtenissen in kaart — van KIN17 via een sleutelgroeiroute naar ongecontroleerde tumoruitbreiding — en toont aan dat het verbreken van die keten nierkanker in het laboratorium en bij dieren kan vertragen.
Bronvermelding: Wen, Y., Lyu, L., Zhang, H. et al. KIN17 facilitates the initiation and progression of renal tumor progression through the PI3K-AKT-mTOR pathway. Sci Rep 16, 5721 (2026). https://doi.org/10.1038/s41598-026-35851-5
Trefwoorden: niercelcarcinoom, KIN17, PI3K AKT mTOR, gerichte therapie, PF-04691502