Clear Sky Science · nl
Eiwitinhoud van extracellulaire vesikels bij patiënten met gevorderde melanomen verandert bij progressie tijdens anti-PD1-therapie
Waarom kleine boodschappers in het bloed behandelingssucces van kanker kunnen voorspellen
Voor mensen met gevorderd melanoom kunnen krachtige nieuwe immunotherapieën soms tumoren laten verdwijnen — maar bij veel anderen zet de kanker snel door. Deze studie onderzoekt microscopische “pakketjes” die tumoren in het bloed afgeven om te zien of ze vroegtijdig en zonder biopsie kunnen aangeven wie waarschijnlijk baat heeft bij anti-PD1-behandeling en wie een andere aanpak nodig heeft.
Kleine belletjes met grote aanwijzingen
Ons bloed bevat talloze nanoschaal belletjes, extracellulaire vesikels genaamd. Dit zijn kleine, door een membraan omsloten pakketjes die cellen gebruiken om moleculaire boodschappen te versturen. Kankercellen geven ze ook af en vullen ze met eiwitten die weerspiegelen wat er binnenin de tumor en in de omgeving gebeurt. Omdat deze vesikels vrij circuleren, kunnen ze uit een eenvoudige bloedafname worden gehaald in plaats van een tumor te snijden. De onderzoekers vroegen zich af of het eiwitcargo van deze vesikels bij patiënten met gevorderd melanoom vroegtijdig kon signaleren hoe goed iemand zou reageren op anti-PD1-immunotherapie, een veelgebruikte klasse medicijnen die de rem op immuuncellen opheft.
Patiënten volgen tijdens de behandeling
Het team bestudeerde negen mensen met gevorderd melanoom die allemaal anti-PD1-medicatie kregen. Bloedmonsters werden genomen op drie tijdstippen: vóór aanvang van de behandeling, kort na de eerste dosis, en ofwel bij ziekteprogressie of negen maanden later als die er niet was. Uit elk monster isoleerden de wetenschappers extracellulaire vesikels en gebruikten geavanceerde massaspectrometrie om hun eiwitinhoud in kaart te brengen. Na zorgvuldige datafiltering richtten ze zich op 969 betrouwbaar gemeten eiwitten. Ze groepeerden deze eiwitten vervolgens in netwerken die belangrijke biologische processen vertegenwoordigen — zoals immuunactiviteit, celadhesie, bloedstolling en energiemetabolisme — en onderzochten hoe deze patronen verschilden tussen patiënten wiens ziekte onder controle bleef en degenen bij wie de tumoren bleven groeien.
Vroege tekenen van respons verborgen in eiwitpatronen
Al vóór de behandeling begonnen, zagen de vesikels er anders uit bij latere responders versus non-responders. Patiënten die het later beter deden hadden vaak vesikels verrijkt met eiwitten die gelinkt zijn aan cel–cel contacten en bepaalde beschermende reacties op ultraviolet licht, een belangrijke factor bij huidkanker. Daarentegen waren sommige immuun-gerelateerde eiwitten en ontstekingsmarkers meer aanwezig bij degenen die later progressie kregen, wat suggereert dat een “hete maar verkeerd gerichte” immuunomgeving het voordeel van de therapie kan verminderen. Door te focussen op individuele moleculen bouwden de onderzoekers een handtekening van acht eiwitten — in wezen een gewogen combinatie van eiwitniveaus — die patiënten in een hoog- en laagrisicogroep voor vroegtijdige ziekteverslechtering verdeelde. In deze kleine groep kon deze handtekening deze groepen met veelbelovende nauwkeurigheid onderscheiden.
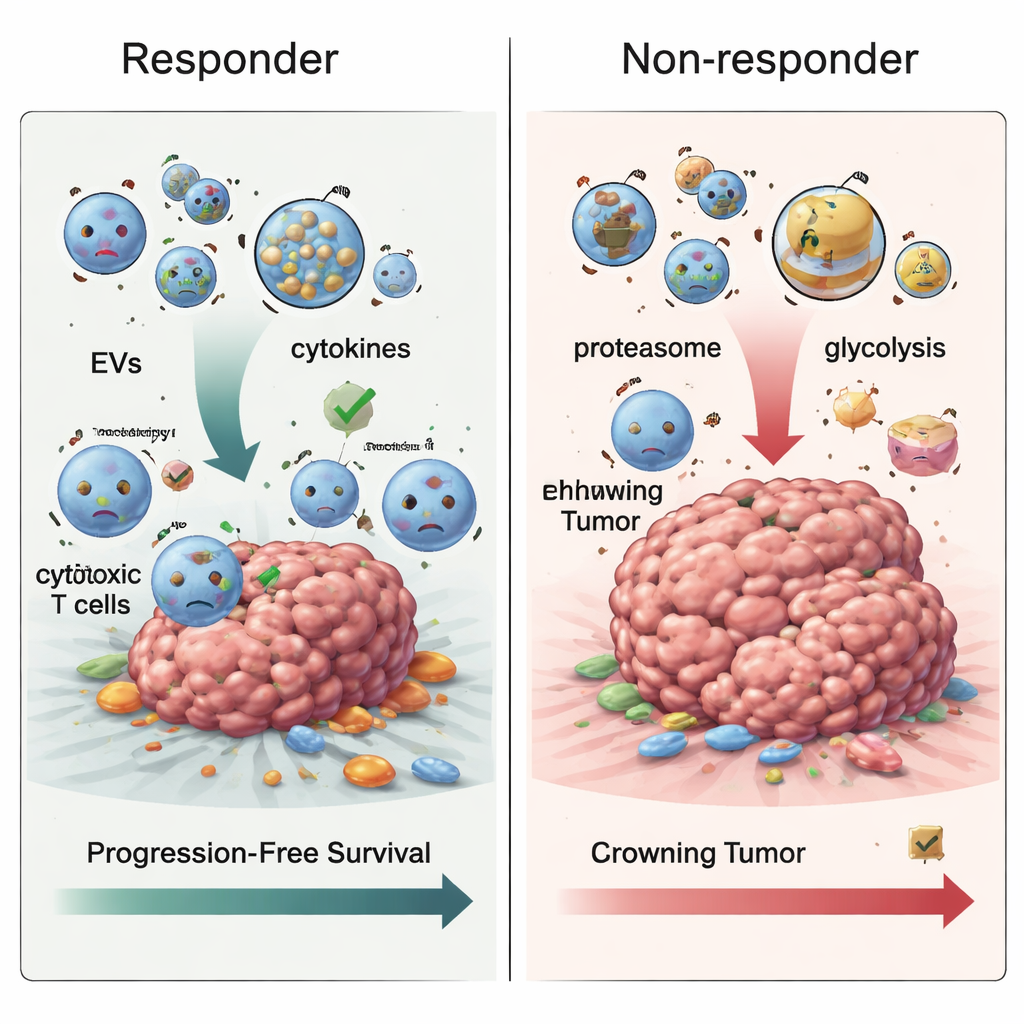
Hoe resistentie in de loop van de tijd kan ontstaan
Toen het team monsters bekeek die na de start van de behandeling waren genomen, kwam een ander patroon naar voren. Bij patiënten van wie het melanoom vorderde, werden extracellulaire vesikels verrijkt met eiwitten die betrokken zijn bij de afvalverwerkingsmachine van de cel, het proteasoom, en bij energie producerende routes zoals glycolyse, het suikerverbrandingsproces waarop veel tumoren vertrouwen. Deze veranderingen passen bij het idee dat resistente tumoren hun metabolisme en eiwitverwerking herprogrammeren om immuunaanvallen te overleven. Door alle drie de tijdstippen samen te volgen zagen de onderzoekers ook dat eiwitten gerelateerd aan bloedstolling in de loop van de tijd bij non-responders daalden, terwijl eiwitten die betrokken zijn bij het presenteren van tumorfragmenten aan het immuunsysteem toenamen — paradoxaal genoeg vertaalde dit zich niet in betere controle van de kanker, wat suggereert dat de manier waarop deze signalen in vesikels worden verpakt de effectieve immuunvernietiging juist kan belemmeren.
Wat dit voor patiënten kan betekenen
In eenvoudige bewoordingen suggereert de studie dat kleine belletjes in de bloedbaan een gedetailleerde moleculaire vingerafdruk dragen van hoe melanomtumoren en het immuunsysteem reageren op anti-PD1-therapie. Specifieke eiwitpatronen in deze vesikels — gemeten vóór en tijdens de behandeling — zouden artsen kunnen helpen voorspellen wie waarschijnlijk langer ziektecontrole zal hebben en wie mogelijk resistentie ontwikkelt door ontsteking en veranderd metabolisme. Hoewel het werk is gebaseerd op slechts negen patiënten en bevestigd moet worden in grotere groepen, wijst het op een toekomst waarin een routinematige bloedafname immunotherapie voor melanoom kan sturen en aanpassen, waardoor deze krachtige medicijnen preciezer en effectiever worden.
Bronvermelding: Trilla-Fuertes, L., Gámez-Pozo, A., Laso-García, F. et al. Protein content of extracellular vesicles from patients with advanced melanoma changes upon progression to anti-PD1 therapy. Sci Rep 16, 5891 (2026). https://doi.org/10.1038/s41598-026-35848-0
Trefwoorden: melanoom immunotherapie, extracellulaire vesikels, bloed biomarkers, anti-PD1 resistentie, proteomics