Clear Sky Science · nl
Ag-gedecorateerde Cu-gedopeerde ZnO-nanomateriaal voor verbeterde antibacteriële toepassing
Waarom kleine deeltjes ertoe doen bij grote infecties
Infecties met antibioticaresistente bacteriën nemen wereldwijd toe, terwijl het ontwikkelen van nieuwe geneesmiddelen traag en kostbaar is. Deze studie onderzoekt een ander tactiek: zorgvuldig ontworpen kleine deeltjes van zinkoxide, gedoteerd met koper en zilver, die bacteriën zowel fysisch als chemisch aanvallen, ook in het donker. Door te begrijpen hoe deze deeltjes zijn opgebouwd en hoe ze microben beschadigen, hopen onderzoekers coatings, verbanden en oppervlakken te ontwikkelen die stilletjes ziekteverwekkers doden voordat ze ernstige ziekte kunnen veroorzaken.
Betere deeltjes bouwen tegen ziektekiemen
De onderzoekers wilden zinkoxide verbeteren, een materiaal dat bekendstaat om zijn bacteriedodende eigenschappen maar meestal alleen bij lichtactivatie werkt. Ze gebruikten een "bottom-up combustion"-methode, waarbij metaalzouten en een veelgebruikt polymeer worden verhit zodat ze opschuimen, verbranden en een stijf, sterk poreus netwerk van kleine kristallen achterlaten. In het zinkoxide-raamwerk introduceerden ze koper en zilver, waardoor een gemengd materiaal ontstond dat een heterostructuur wordt genoemd, waarin meerdere metalen en metaaloxiden zeer dicht bij elkaar liggen. 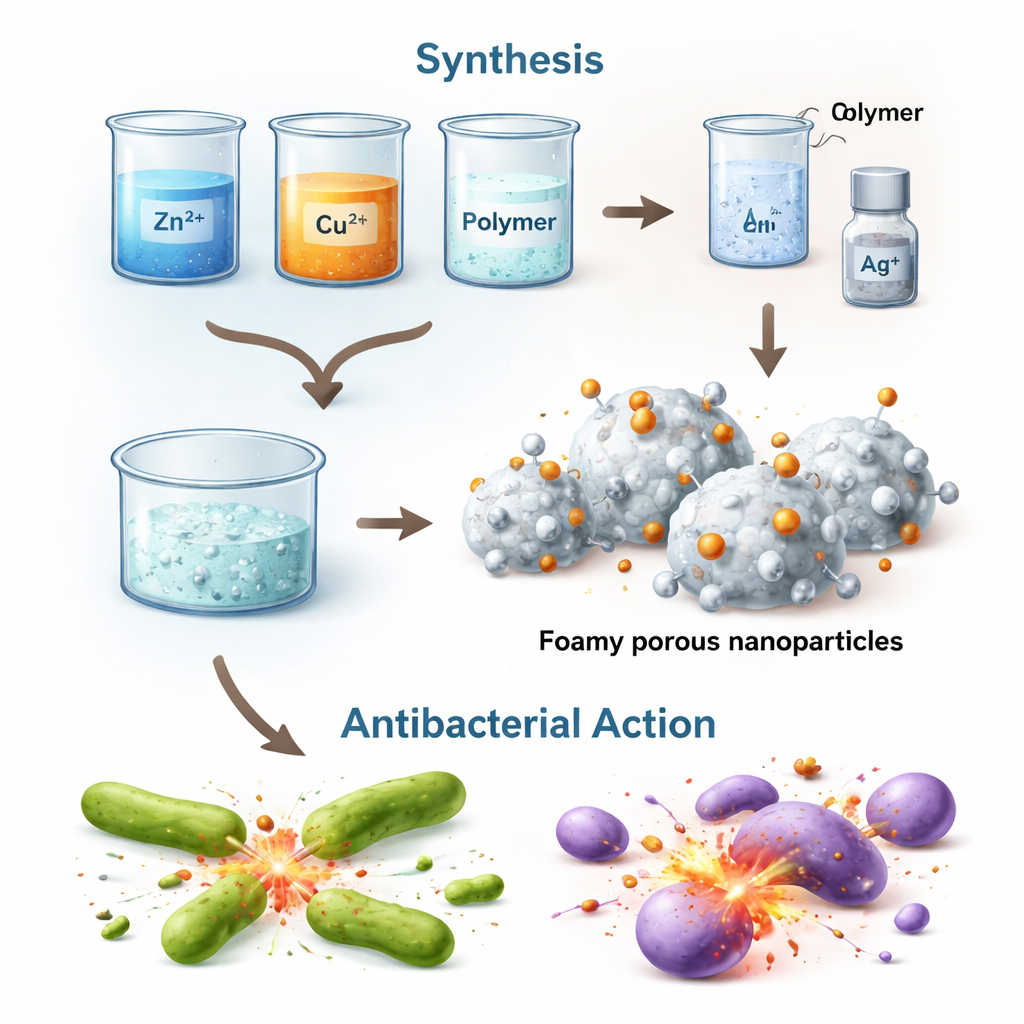
In het nieuwe materiaal kijken
Om te zien wat ze hadden gemaakt, gebruikte het team een reeks structurele en optische onderzoeken. Röntgenmetingen toonden aan dat kopersoorten in het zinkoxide-kristalrooster insprongen en dit lichtjes samendrukten, terwijl zilver voornamelijk zijn eigen kleine kristallen aan het oppervlak vormde. Hoge-resolutie elektronenmicroscopie toonde deze verschillende componenten gepakt samen binnen poreuze, schuimachtige structuren. Lichtgebaseerde metingen bevestigden dat het toevoegen van koper en zilver de bandkloof van zinkoxide verkleinde en verbeterde hoe ladingsdragers door het materiaal bewegen. In praktische zin betekent dit dat het eenvoudiger schadelijke, kortlevende zuurstofgebaseerde chemicaliën kan genereren en reactieve ladingen kan scheiden, beide nuttig voor het doden van bacteriën.
Structuur omzetten in antibacteriële kracht
De cruciale test was of deze ontworpen deeltjes daadwerkelijk de groei van bacteriën konden stoppen. De wetenschappers vergeleken puur zinkoxide met koper‑gedopeerde, zilver‑gedecorateerde en volledig gecombineerde koper–zilver–zinkoxide-deeltjes tegen zowel Gram-positieve als Gram-negatieve bacteriën, die verschillen in celwandstructuur. Ze bestudeerden ook versies gemaakt vóór en na een extra verwarmingsstap genaamd calcinatie. Zuiver zinkoxide werkte bescheiden, voornamelijk vóór de laatste verhitting, maar verloor grotendeels zijn effect daarna. Daarentegen werd het volledig gecombineerde materiaal—bevatte zinkoxide, koperoxide en zilver—krachtiger na calcinatie en bereikte een remzone tot 22 millimeter tegen Streptococcus pyogenes, een Gram-positieve bacterie, bij de hoogste geteste dosis. Over het geheel genomen presteerden de nieuwe gemengde deeltjes beter dan enkelmetaaldeeltjes, vooral tegen Gram-positieve stammen.
Hoe de deeltjes bacteriën in het donker aanvallen
In tegenstelling tot veel lichtgeactiveerde materialen zijn deze deeltjes ontworpen om zonder belichting te werken. De studie stelt dat de gemengde metaaldeeltjes bacteriën via een meerledig aanvalsscenario doden. Ten eerste lossen zink-, koper- en zilverionen langzaam van het deeltjesoppervlak op en binden ze aan bacteriële membranen, enzymen en DNA, waardoor vitale processen verstoord raken en de celomhulling lek wordt. Ten tweede helpt het nauwe contact tussen de verschillende metalen bij de generatie van reactieve zuurstofsoorten—zeer agressieve vormen van zuurstof—even in het donker. Deze soortengroepen beschadigen eiwitten, vetten en genetisch materiaal. Ten derde vergroot de poreuze, ruwe textuur van de deeltjes het contact met bacteriële cellen en kan het fysiek de buitenlagen beschadigen. Gezamenlijk overbelasten deze effecten bacteriële verdedigingsmechanismen en bemoeilijken ze het ontstaan van resistentie. 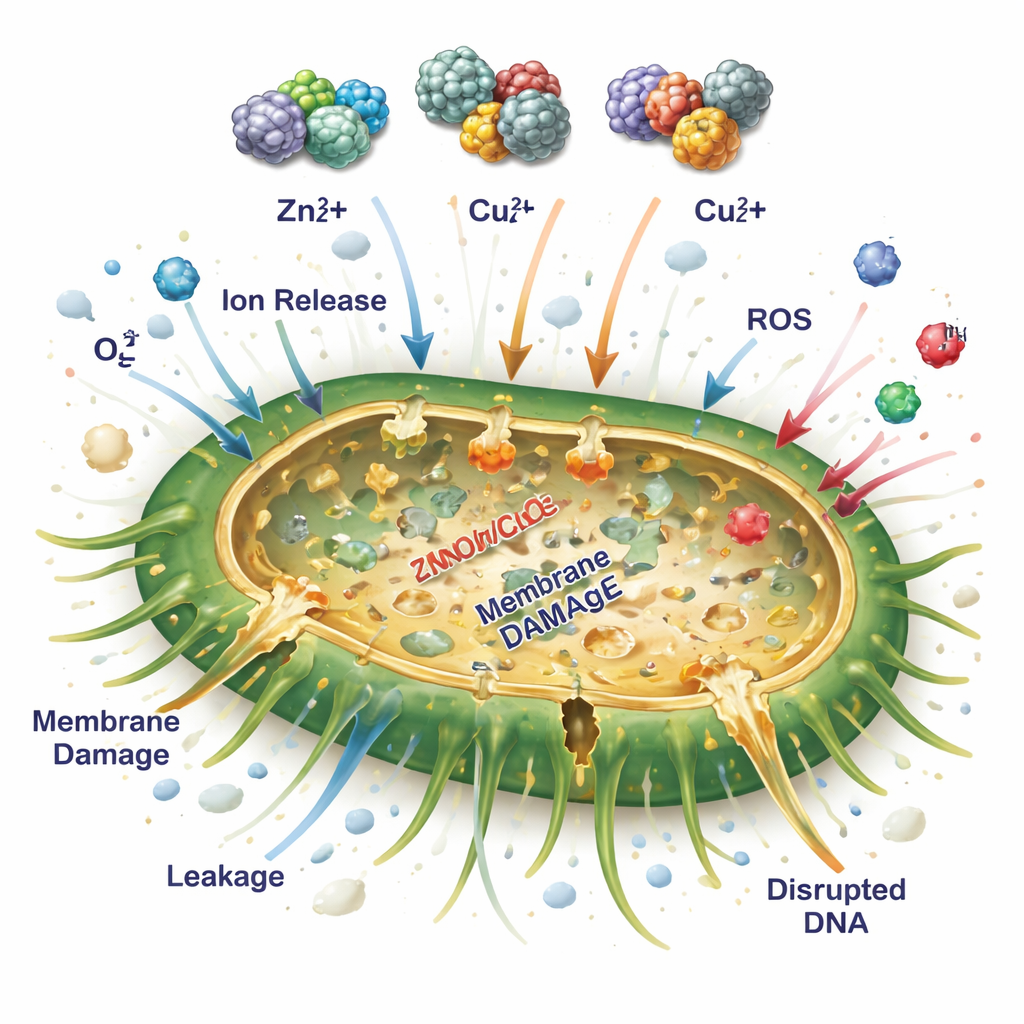
Van petrischaal naar bescherming in de praktijk
Voor niet‑specialisten is de kernboodschap dat het zorgvuldig combineren van bekende metalen zoals zink, koper en zilver in één goed gestructureerde nanodeeltje een alledaags ingrediënt kan omvormen tot een krachtig, breedspectrum antibacterieel middel. Het meest effectieve materiaal in dit werk remde bepaalde bacteriën bijna net zo goed als een standaard antibioticum, zonder afhankelijk te zijn van licht. Omdat deze deeltjes als poreuze schuimen in een relatief eenvoudig proces gemaakt kunnen worden, zouden ze uiteindelijk opgeschaald kunnen worden voor gebruik in wondverbanden, coatings voor medische implantaten of oppervlakken in ziekenhuizen die passief bacteriegroei onderdrukken. Hoewel aanvullend onderzoek nodig is om veiligheid en effectiviteit in echte weefsels te bevestigen, toont deze studie een veelbelovende weg naar fysisch‑chemische antibacteriële middelen die traditionele antibiotica aanvullen in plaats van vervangen.
Bronvermelding: Gebretsadik, A., Reddy, S.G., Gonfa, B.A. et al. Ag-decorated Cu-doped ZnO nanomaterial for enhanced antibacterial application. Sci Rep 16, 5552 (2026). https://doi.org/10.1038/s41598-026-35838-2
Trefwoorden: antibacteriële nanomaterialen, zinkoxide-nanodeeltjes, koper- en zilverdoping, antibioticaresistentie, heterogestructureerde nanocomposieten