Clear Sky Science · nl
Detectie van sikkelcelziekte onder weinig hulpbronnen met transfer learning en contrastive learning gekoppeld aan explainable AI
Waarom slimere bloedtests ertoe doen
Sikkelcelziekte is een levenslange bloedafwijking die hevige pijn, infecties en vroegtijdig overlijden kan veroorzaken, vooral in delen van Afrika en India waar medische hulp schaars is. Vroege diagnose kan levens redden, maar traditionele tests vragen om geschoold personeel, gespecialiseerde apparatuur en tijd die veel klinieken niet hebben. Dit artikel onderzoekt hoe kunstmatige intelligentie (AI) eenvoudige microscoopbeelden van bloed kan omzetten in snelle, betrouwbare screeningsinstrumenten, waardoor het eenvoudiger wordt om sikkelcelziekte te herkennen, zelfs in omgevingen met weinig middelen.
Een nadere blik op een gevaarlijke bloedziekte
Bij sikkelcelziekte veroorzaakt een kleine wijziging in het gen voor hemoglobine—het eiwit dat zuurstof vervoert—dat rode bloedcellen buigen in stijve, halve maan- of “sikkel”vormen in plaats van zacht en rond te blijven. Deze misvormde cellen kunnen kleine bloedvaten verstoppen, de bloedstroom blokkeren en organen beschadigen. 
Van overbelaste laboratoria naar AI-hulp
Traditionele manieren om sikkelcelziekte te bevestigen—zoals hemoglobine-elektroforese of genetische tests—zijn nauwkeurig maar vaak duur, apparatuur-intensief en traag. Daarentegen hebben veel klinieken al basale microscopen, en moderne camera’s kunnen hoge-resolutiebeelden van bloeduitstrijkjes vastleggen. De auteurs bouwen voort op deze realiteit: in plaats van te veranderen hoe bloed wordt verzameld, veranderen ze hoe beelden worden geanalyseerd. Ze voeden gedigitaliseerde bloeduitstrijkbeelden in AI-modellen die al hebben geleerd patronen te herkennen uit miljoenen alledaagse foto’s, en verfijnen deze modellen vervolgens om normale rode bloedcellen van gesikkelde cellen te onderscheiden. Dit hergebruik van eerder verworven kennis, transfer learning genoemd, is cruciaal wanneer slechts enkele honderden medische beelden beschikbaar zijn voor training.
Machines leren subtiele vormen te onderscheiden
Niet alle AI-trainingsmethoden zijn gelijk, zeker wanneer data beperkt zijn. De onderzoekers vergelijken drie populaire beeldherkenningsnetwerken—ResNet-50, DenseNet-121 en EfficientNet-B0—en drie trainingswijzen. Twee van de trainingsmethoden behandelen het probleem als een simpele ja-nee-vraag (sikkel of niet) en proberen de ruwe classificatienauwkeurigheid van het model te verbeteren. De derde, genoemd triplet loss, leert het netwerk in plaats daarvan beelden te rangschikken in een “vormruimte” waarin beelden van sikkelcellen samenklonteren en zich verwijderen van beelden van normale cellen. Deze op contrast gerichte training verandert het model in een specialist in het opmerken van kleine, vormgebaseerde verschillen—precies wat telt bij sikkelcelmicroscopie.
Het besluitproces inzichtelijk maken
Artsen en laboratoriummedewerkers moeten elk geautomatiseerd systeem dat invloed heeft op de patiëntenzorg kunnen vertrouwen. Om de AI-‘zwarte doos’ te openen gebruiken de auteurs een verklaarbare AI-methode genaamd Grad-CAM, die een heatmap over het originele microscoopbeeld legt om te laten zien welke gebieden het meest bijdroegen aan de beslissing. 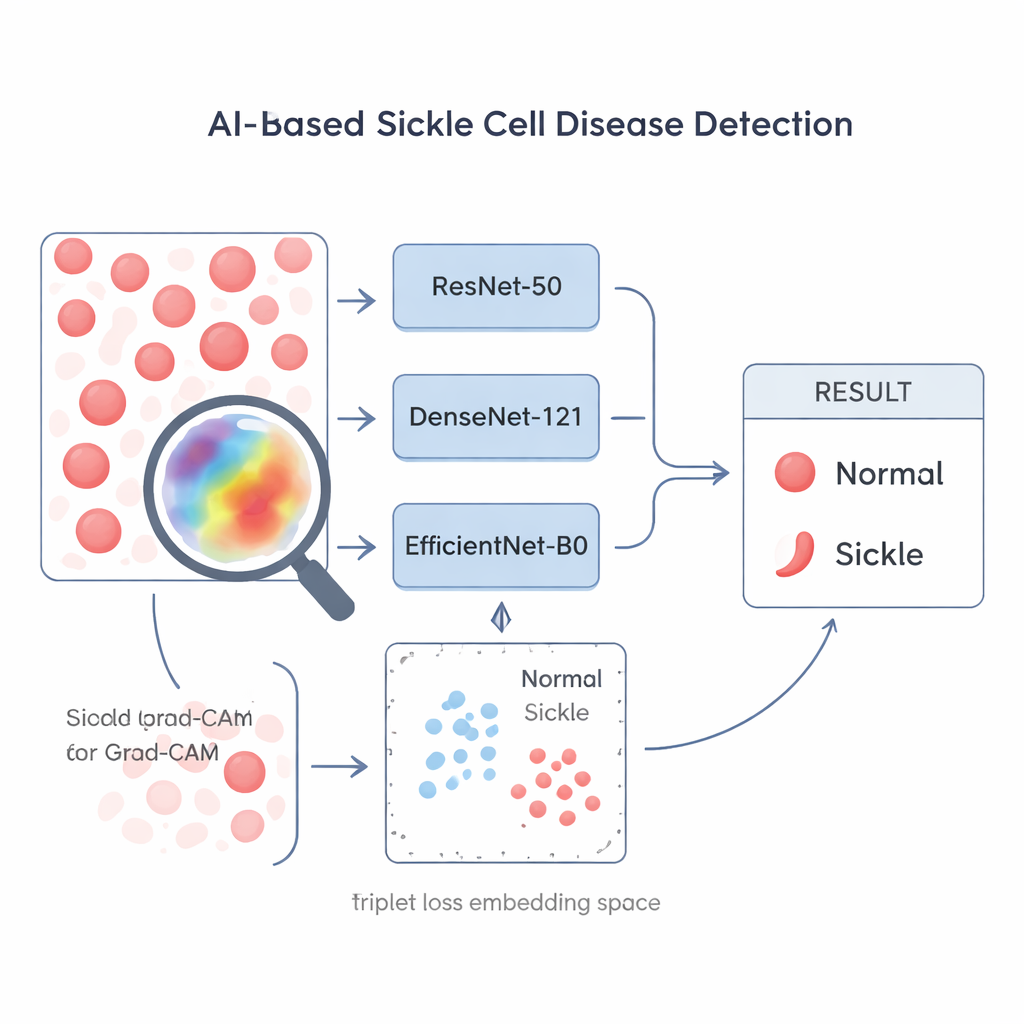
Van onderzoek naar klinische praktijk
De studie concludeert dat slim hergebruik van bestaande beeldherkenningsnetwerken, gecombineerd met triplet-loss-training en visuele verklaringen, nauwkeurige en transparante detectie van sikkelcelziekte kan leveren op basis van relatief weinig beelden. Simpel gezegd kan een standaardmicroscoop plus een camera en laptop hulpverleners in de frontlinie snel patiënten aanwijzen die waarschijnlijk sikkelcelziekte hebben, zelfs zonder geavanceerde labtests. Hoewel grotere en meer diverse datasets nog nodig zijn voordat dergelijke hulpmiddelen breed inzetbaar zijn, toont dit werk een duidelijke route naar goedkope, AI-ondersteunde screening die daadwerkelijk verschil kan maken in regio’s waar sikkelcelziekte veel voorkomt maar diagnostische middelen beperkt zijn.
Bronvermelding: Patel, J., Muralikrishna, H., Chadaga, K. et al. Sickle cell disease detection in low-resource conditions using transfer-learning and contrastive-learning coupled with XAI. Sci Rep 16, 6104 (2026). https://doi.org/10.1038/s41598-026-35831-9
Trefwoorden: sikkelcelziekte, medische beeldvorming, deep learning, diagnostiek met weinig middelen, verklaarbare AI