Clear Sky Science · nl
Gemeenschappelijke veranderingen in genexpressie en methylering in twee ratmodellen van verworven epilepsie
Waarom veranderingen in genen ertoe doen bij aanvallen
Epilepsie treft miljoenen mensen en bij ongeveer één op de drie bieden de huidige medicijnen geen volledige controle over de aanvallen. De meeste medicijnen dempen alleen de elektrische stormen in de hersenen, maar voorkomen niet dat epilepsie zich in de eerste plaats ontwikkelt. Deze studie onderzoekt of blijvende chemische markeringen op DNA en de manier waarop genen aan- of uitgezet worden, kunnen verklaren hoe een gezonde hersenfunctie epileptisch wordt — en of die veranderingen gemeenschappelijk zijn voor verschillende vormen van de ziekte.
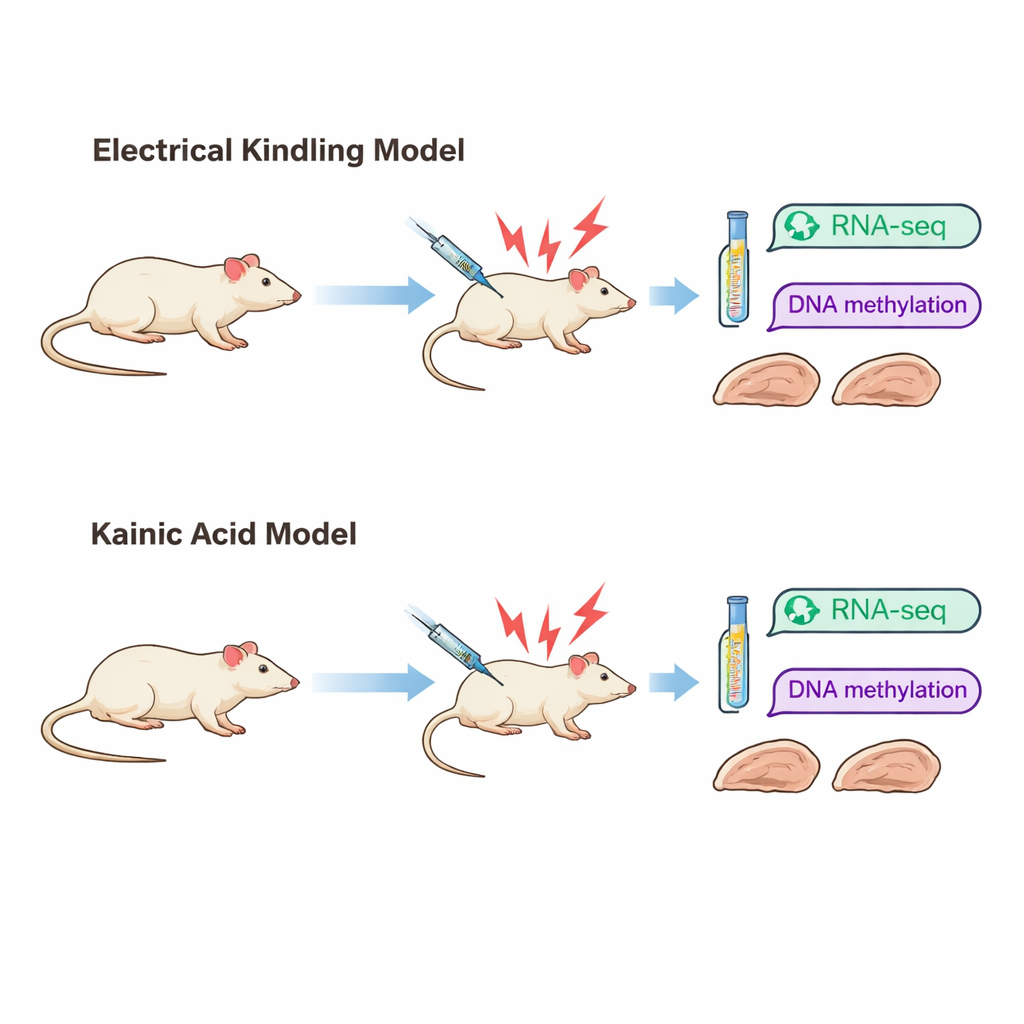
Twee verschillende wegen naar dezelfde ziekte
De onderzoekers richtten zich op temporale lob epilepsie, een veelvoorkomende vorm die vaak moeilijk te behandelen is. Ze gebruikten twee gangbare ratmodellen die verschillende manieren nabootsen waarop epilepsie kan ontstaan. In het “kindling”-model worden over langere tijd korte elektrische pulsen aan een deel van de hippocampus gegeven totdat aanvallen gemakkelijk uitgelokt worden. In het “kaininezuur”-model veroorzaakt een chemische stof een intense aanvalsgolf, waarna later spontaan aanvallen ontstaan. Hoewel beide modellen uiteindelijk vergelijkbaar gedrag opleveren — ernstige tonisch-clonische aanvallen — ziet de hersenschade er zeer verschillend uit. Bij gekindelde ratten is de weefselstructuur grotendeels bewaard gebleven, terwijl bij aan kaininezuur behandelde ratten opvallend celverlies en littekenvorming in belangrijke hippocampale gebieden zichtbaar is.
De genetische activiteit van de hersenen lezen
Om te zien hoe deze verschillende routes naar epilepsie het brein op moleculair niveau veranderen, onderzocht het team de hippocampus nadat ratten in elk model drie ernstige aanvallen hadden doorgemaakt. Ze bepaalden welke genen meer of minder actief waren met RNA-sequencing en brachten chemische etiketten, methylgroepen op DNA, in kaart met een methode die bekendstaat als reduced-representation bisulfite sequencing. Veranderingen in genactiviteit weerspiegelen hoe cellen reageren en zich aanpassen, terwijl methylatiekenmerken vaak worden gezien als een langeretermijn ‘‘geheugen’’ dat kan beïnvloeden of genen aan- of uitgezet zijn.
Veranderingen in genactiviteit lopen voor op DNA-markeringen
De twee modellen gaven opvallend verschillende patronen van genactiviteit. Het kindling-model toonde veranderingen in meer dan tien keer zoveel genen als het kaininezuur-model. Toch vonden de onderzoekers bij het overlappen van de lijsten nog steeds meer dan honderd genen die in beide modellen verschoven, en de meeste daarvan veranderden in dezelfde richting. Een voorbeeld is Mmp9, een gen dat gelinkt is aan hoe hersencellen hun verbindingen herstructureren en aan schade gerelateerd aan aanvallen; dit gen was in beide modellen sterk verhoogd. Deze gedeelde veranderingen wijzen erop dat er kernreacties op epileptogenese bestaan, zelfs wanneer de aanvangs-trigger en zichtbare hersenbeschadiging verschillen.
DNA-etiketten vertellen een ander verhaal
Toen het team naar DNA-methylering keek, veranderde het beeld. Beide modellen toonden veel genen met gewijzigde methylering, en er was een aanzienlijke overlap tussen hen. Echter, slechts een bescheiden subset van genen toonde zowel gewijzigde methylering als gewijzigde activiteit binnen hetzelfde model, en nog minder gedroegen zich zo in beide modellen. Bij sommige van deze gedeelde genen, zoals Nedd9 en Ptpre, nam de expressie in beide modellen toe, maar de richting van de verandering in DNA-methylering op individuele sites kon tussen de modellen tegengesteld zijn. Over het geheel genomen was er geen eenvoudige regel van ‘‘meer methylering betekent minder genactiviteit’’ of andersom. Dit suggereert dat in deze epilepsiemodellen de meeste verschuivingen in genactiviteit niet direct worden aangedreven door brede veranderingen in DNA-methylering.
Wat dit betekent voor toekomstige behandelingen
Voor mensen die op betere therapieën voor epilepsie hopen, bieden deze bevindingen zowel waarschuwing als richting. Het werk toont aan dat de genetische programma’s die tijdens de ontwikkeling van epilepsie worden geactiveerd behoorlijk model-specifiek kunnen zijn, en dat DNA-methylering slechts een onderdeel is van een groter, complexer regulatoir geheel. Veelbelovende gentargets die in één diermodel worden geïdentificeerd, generaliseren mogelijk niet, dus ze zouden in meerdere modellen getest moeten worden voordat ze naar menselijke behandelingen worden doorontwikkeld. Tegelijkertijd kan de kleine groep genen die in zowel expressie als methylering tussen modellen verandert, bijzonder robuuste startpunten vormen voor de ontwikkeling van ziekte-modificerende therapieën die niet alleen aanvallen onderdrukken, maar ook proberen te voorkomen dat epilepsie zich vestigt.
Bronvermelding: Purnell, B.S., Hur, J., Ruskin, D. et al. Commonalities in gene expression and methylation changes across two rat models of acquired epilepsy. Sci Rep 16, 5095 (2026). https://doi.org/10.1038/s41598-026-35826-6
Trefwoorden: epileptogenese, DNA-methylering, genexpressie, temporale lob epilepsie, ratmodellen