Clear Sky Science · nl
Cellulaire bio-energetische en migratoire reacties van menselijke gingivale fibroblasten op 940 nm diodelaser photobiomodulatie
Licht dat mondwonden helpt genezen
Iemand die ooit een tand heeft laten trekken of een tandvleesoperatie heeft ondergaan, weet hoe ongemakkelijk het genezingsproces in de mond kan zijn. De weefsels worden continu belast door kauwen, praten en bacteriën, dus alles wat het herstel veilig kan versnellen, wekt grote belangstelling bij tandartsen en patiënten. Deze studie onderzocht of een veelgebruikte dentale laser, toegepast op zeer laag vermogen, zachtjes gingivale cellen kan "aansturen" om harder te werken en sneller te bewegen tijdens het herbouwen van beschadigd weefsel, zonder ze te verbranden of te beschadigen.
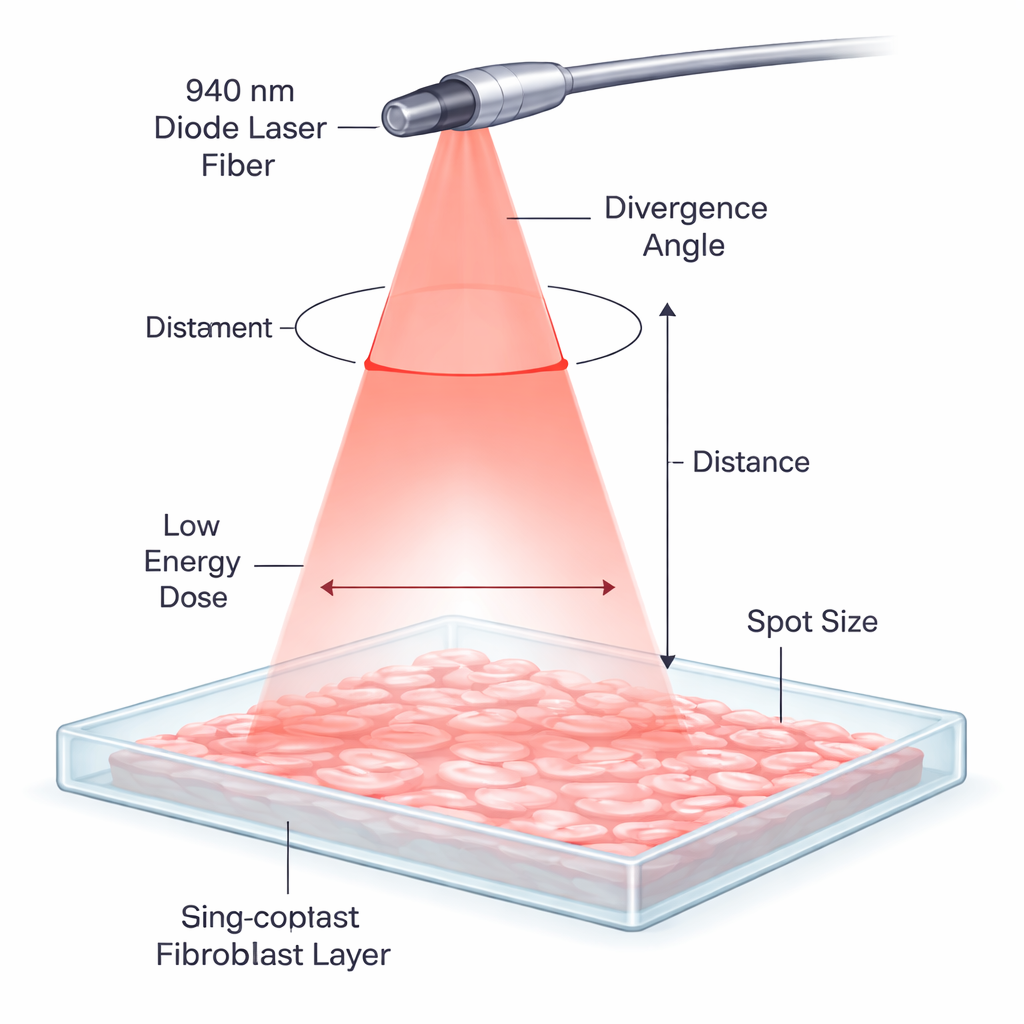
Hoe een zachte laser verschilt van een snijdende laser
In veel tandartspraktijken worden diodelasers routinematig gebruikt om zacht weefsel te snijden of te vormen door warmte te genereren. Hier werd hetzelfde type 940 nanometer laser op een veel lager niveau ingesteld en op een heel andere manier gebruikt. In plaats van het weefsel aan te raken en te verbranden, werd licht gedurende slechts één seconde van korte afstand toegediend, zich verspreidend in een zachte kegel over een dun laagje menselijke tandvleescellen gekweekt in een petrischaal. Bij deze lage doseringen is het doel niet te snijden, maar het interne machinerie van de cellen zachtjes te stimuleren — een proces dat bekendstaat als photobiomodulatie — zodat ze efficiënter repareren en zich reorganiseren.
Testen van de energie en veiligheid van tandvleescellen
De onderzoekers concentreerden zich op fibroblasten, de belangrijkste cellen die de vezels en de matrix produceren die het tandvlees zijn stevigheid geven. Commercieel verkregen menselijke gingivale fibroblasten werden als uniforme lagen gekweekt en blootgesteld aan drie verschillende energiedoseringen van de 940 nm laser, terwijl een vierde groep geen licht kreeg. Het team mat vervolgens verschillende indicatoren: hoe metabolisch actief de cellen waren, of hun buitenmembranen beschadigd waren, hoeveel cellulaire brandstof (ATP) ze produceerden en of ze stikstofoxide vrijgaven, een molecuul dat verband houdt met ontsteking. Over alle laserdoseringen heen toonden de cellen geen tekenen van lekkage of letsel en gaven ze geen ontstekingssignaal af, wat aangeeft dat de korte lichtblootstelling zacht en biologisch compatibel was onder de onderzochte condities.
Meer cellulaire "brandstof" en een gouden midden voor beweging
Hoewel de cellen in alle groepen gezond bleven, veranderde hun energieproductie op een dosis- en tijdsafhankelijke manier. Bij gematigde lichtniveaus verhoogden fibroblasten de productie van ATP, de universele energievaluta van cellen, met zo’n kwart ten opzichte van onbehandelde cellen na 24 uur. Hun algemene metabolische activiteit steeg ook bescheiden, vooral bij de hoogste dosis. Om te zien of deze extra energie zich vertaalde naar beter herstelgedrag, creëerden de wetenschappers een rechte "krab" in de cellaag en gebruikten digitale holografische beeldvorming om te volgen hoe snel cellen naar binnen kropen om de kloof te sluiten. Ze vonden dat een lagere laserdosis de migratiesnelheid licht verhoogde en leidde tot de snelste sluiting, terwijl de hoogste dosis de beweging daadwerkelijk vertraagde en de sluiting uitstelde, zelfs al waren de energieniveaus nog verhoogd. Dit patroon, waarbij een beetje stimulatie helpt maar te veel juist belemmert, staat bekend als een biphasische respons.
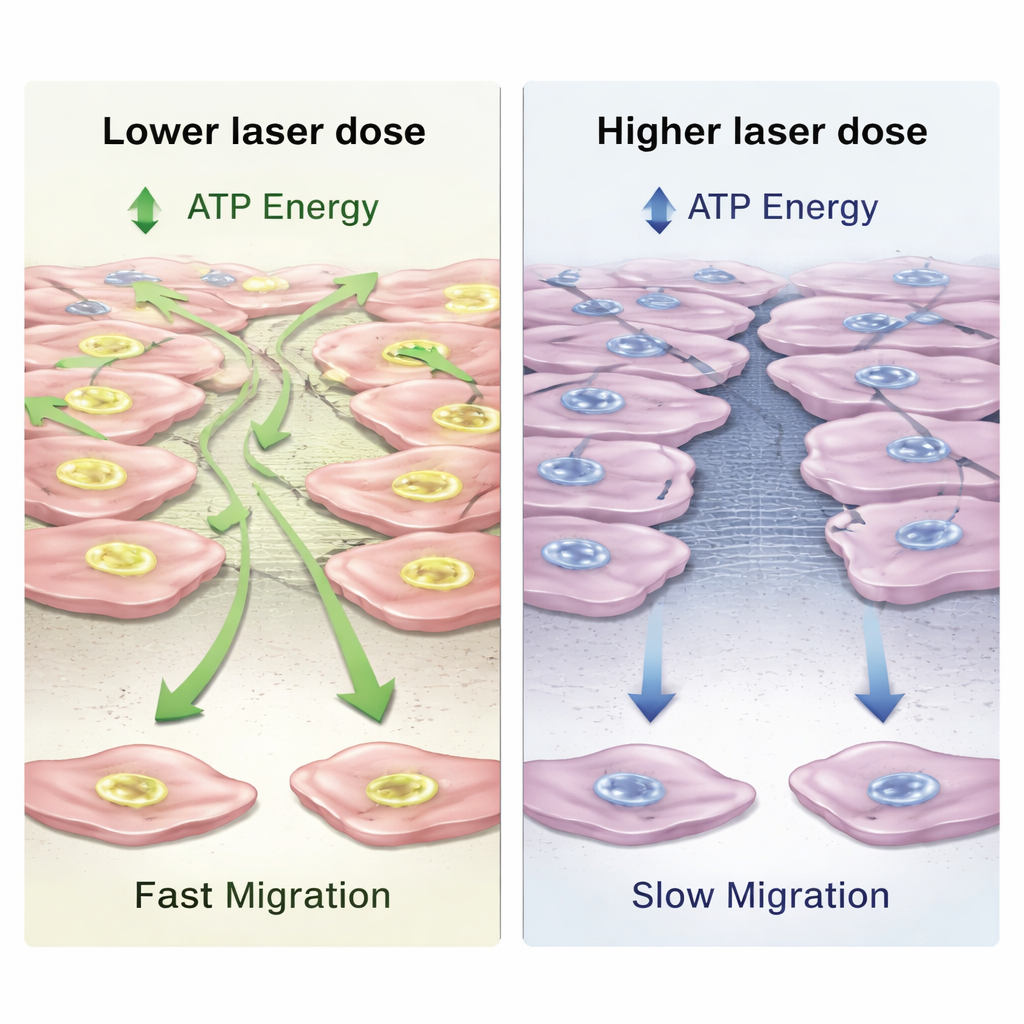
Wat dit zou kunnen betekenen voor tandheelkundige genezing
Aangezien deze experimenten in een vereenvoudigd schakermodel werden uitgevoerd, kunnen ze niet de volledige complexiteit van een genezende wond in een levende mond vastleggen, waar bloedstroom, immuuncellen en bacteriën allemaal een belangrijke rol spelen. Toch schetsen de resultaten een veelbelovend venster van lichtdoseringen waarin een 940 nm dentale laser de energie van tandvleescellen kan verhogen en hun beweging kan sturen zonder schade of ontsteking te veroorzaken. Het werk toont ook aan dat fijn afstemmen van de dosis belangrijk is: de condities die de cellulaire brandstof maximaliseerden waren niet precies dezelfde als die welke de snelste sluiting van de kunstmatige wond produceerden.
Conclusie voor patiënten en zorgverleners
Voor leken is de belangrijkste boodschap dat laag-energetisch laserlicht, zorgvuldig gecontroleerd, mogelijk op termijn kan helpen tandvlees sneller en voorspelbaarder te laten genezen na ingrepen zoals grafts, implantaten of extracties. In deze studie moedigde zeer korte, niet-contactblootstelling aan een 940 nm diodelaser gekweekte tandvleescellen aan om gezond te blijven, meer energie te maken en — binnen het juiste dosisbereik — sneller te kruipen om een wondachtige kloof te sluiten. Deze instellingen zijn nog niet klaar voor directe toepassing in de kliniek, maar ze vormen een wetenschappelijke basis voor toekomstige proeven bij dieren en mensen die erop gericht zijn een alledaagse dentale laser te veranderen in een precies instrument om natuurlijke weefselherstel te versterken in plaats van alleen te snijden.
Bronvermelding: Mizrahi, I.K., Neculau, C., Balasea, B.V. et al. Cellular bioenergetic and migratory responses of human gingival fibroblasts to 940 nm diode laser photobiomodulation. Sci Rep 16, 5972 (2026). https://doi.org/10.1038/s41598-026-35824-8
Trefwoorden: genezing van tandvleeswonden, laag-energetische lasertherapie, herstel na mondchirurgie, photobiomodulatie, gingivale fibroblasten