Clear Sky Science · nl
Spierverlies door sepsis wordt verminderd door farmacologische remming van het STAT3‑signaleringspad bij muizen
Waarom ernstige infecties je kracht kunnen wegnemen
Het overleven van een levensbedreigende infectie zoals sepsis is nog maar de helft van de strijd. Veel patiënten verlaten de intensive care zo verzwakt dat lopen, traplopen of zelfs hun armen optillen een moeite wordt. Deze studie stelt een eenvoudige maar urgente vraag: kunnen we voorkomen dat het lichaam zijn eigen spieren afbreekt tijdens sepsis, en zo ja, hoe? Met muizen, spiercellen in een kweek en observaties van mensen op een intensivecare-afdeling traceren de onderzoekers een sleutelroute van signaaloverdracht die spierverlies aandrijft — en tonen aan dat een gerichte geneesmiddeltherapie die schade deels kan blokkeren.
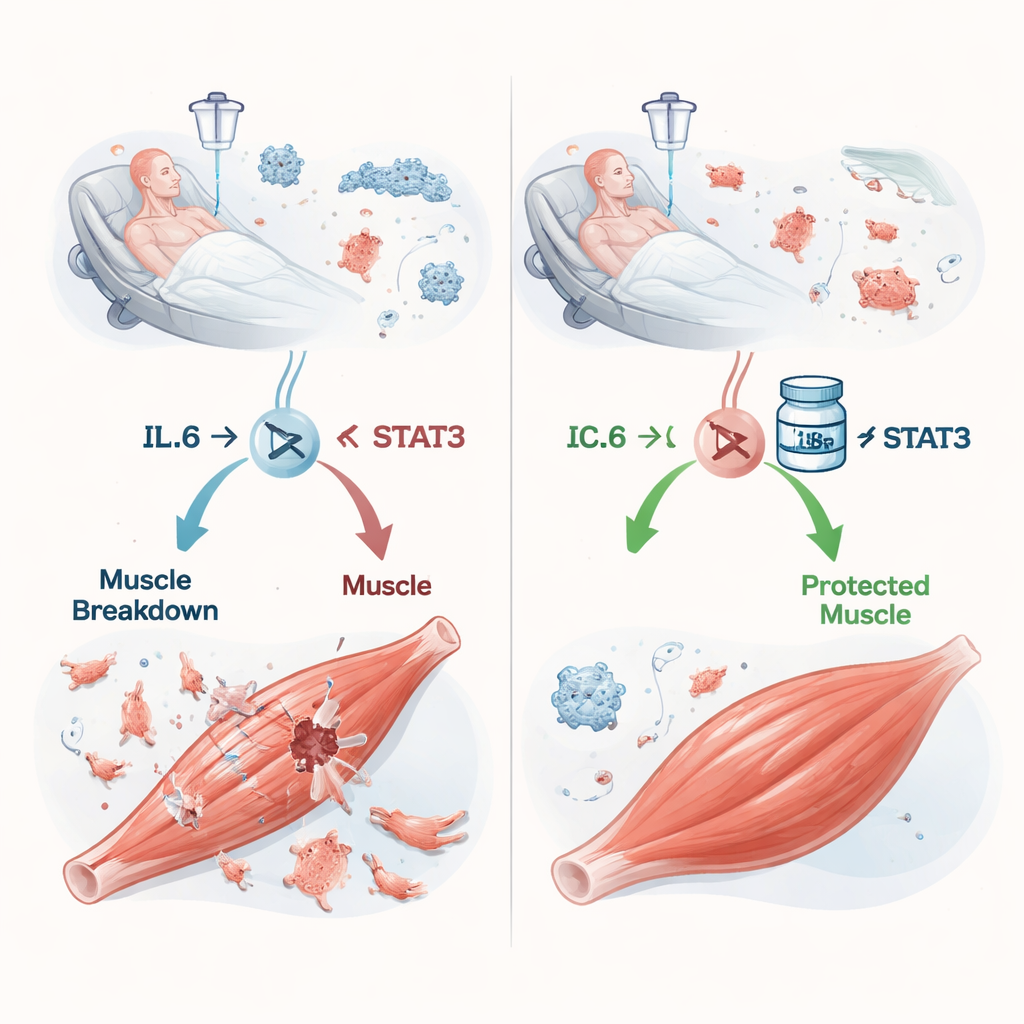
Een kettingreactie van infectie naar spierverlies
Sepsis ontstaat wanneer de reactie van het lichaam op een infectie uit de hand loopt en de bloedbaan overspoelt met ontstekingsstoffen. Een van de belangrijkste is interleukine‑6 (IL‑6). Eerder onderzoek suggereerde dat IL‑6 spieren kan aanzetten tot het afbreken van eigen eiwitten, maar de details waren onduidelijk. De auteurs richtten zich op STAT3, een eiwit in cellen dat het signaal van IL‑6 doorgeeft aan de kern, waar genen aan- of uitgezet worden. Bij muizen die een cecale slurry kregen — in wezen een gecontroleerde, gemengde bacteriële infectie — schoten de IL‑6‑waarden in bloed en beenspieren omhoog naarmate de sepsis verergerde. Tegelijkertijd werd STAT3 in spieren geactiveerd en verloren de dieren gewicht, spiermassa en grijpkracht in een graad‑afhankelijke mate die sterk leek op wat wordt gezien bij kritisch zieke patiënten.
Hoe sepsis spiercellen herprogrammeert
Om te begrijpen wat sepsis binnen spiervezels deed, analyseerde het team de genactiviteit in de tibialis anterior, een belangrijke beenspier. Duizenden genen veranderden hun activiteit in septische muizen vergeleken met gezonde controles. Paden die betrokken zijn bij ontsteking, cellulaire stress en vooral IL‑6/STAT3‑signalering werden geactiveerd. Twee grote eiwitafbraaksystemen werden opgeschroefd: het ubiquitine‑proteasoomsysteem, dat specifieke spiereiwitten markeert voor vernietiging, en autofagie, een algemenere recyclingproces. Belangrijke «spiervretende» enzymen, MuRF1 en atrogin‑1, namen sterk toe, terwijl groeibevorderende paden en klassieke celdoodsignalen grotendeels onveranderd bleven. In parallelle experimenten lieten gekweekte muizenspiercellen die werden blootgesteld aan lipopolysacharide (LPS), een bestanddeel van Gramnegatieve bacterieomgevingen, hetzelfde patroon zien: activering van IL‑6 en STAT3, toename van MuRF1 en atrogin‑1, meer autofagie en zichtbare dunner wordende spiervezels.
Een belangrijke schakel blokkeren om spieren te beschermen
Het centrale experiment testte of het uitschakelen van STAT3 spieren kon sparen. Muizen met sepsis kregen een kleinmolecuul‑STAT3‑remmer genaamd C188‑9, beginnend één uur na de infectie en vervolgens dagelijks. Het middel verzachtte de aanvankelijke «cytokinestorm» niet — de bloedwaarden van IL‑6 en een andere ontstekingsfactor, TNF‑α, bleven hoog en lichaamsgewicht en eetlust herstelden niet snel. Toch beschermde C188‑9 duidelijk het skeletspierweefsel: behandelde muizen behielden meer tibialis‑spiermassa, hadden een sterkere grip en grotere spiervezels onder de microscoop dan onbehandelde septische muizen. In de spieren verminderde C188‑9 sterk geactiveerd STAT3 en verlaagde het de niveaus van MuRF1 en atrogin‑1, maar liet het merkers van autofagie grotendeels onveranderd. In kweekexperimenten dempte het voorbehandelen van spiercellen met C188‑9 op vergelijkbare wijze STAT3‑activatie en de toename van MuRF1 en atrogin‑1 en voorkwam het door LPS geïnduceerde krimpen van de vezels, opnieuw zonder autofagie uit te schakelen.
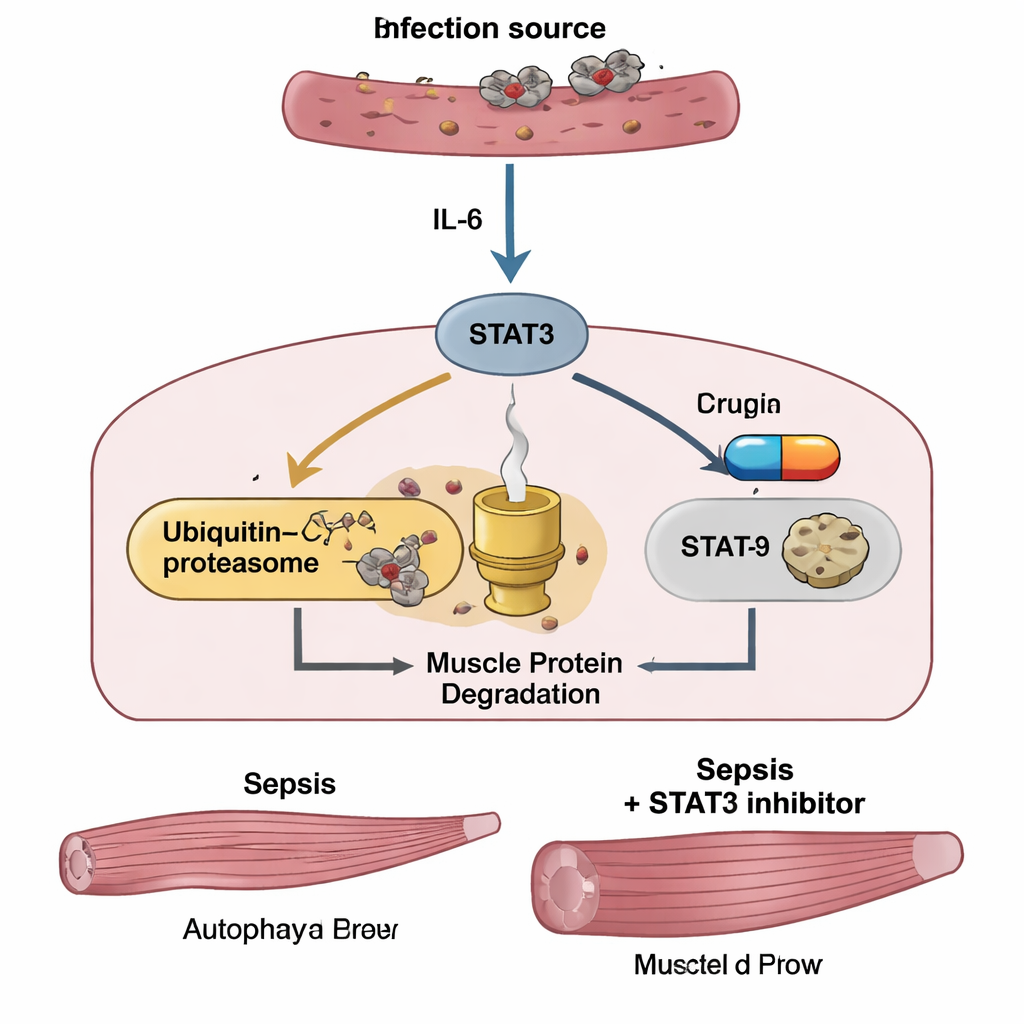
Aanwijzingen van patiënten op de intensivecare
Om te zien of deze mechanismen ook bij mensen relevant zijn, volgden de onderzoekers 67 volwassenen met sepsis die werden opgenomen op een intensivecareafdeling in Japan. Bloedtests bij opname toonden dat patiënten met septische shock bijzonder hoge IL‑6‑waarden hadden. Over de hele groep hield IL‑6 — maar niet TNF‑α — nauw verband met scores voor sepsisseverity en met bloedmarkers van ontsteking en spierschade. In een subgroep van 45 patiënten die twee CT‑scans van de buik ondergingen, voorspelden de IL‑6‑waarden bij opname hoeveel de psoas‑spier bij de onderrug in de volgende één tot drie weken kromp. Degenen die de meeste spiermassa verloren, hadden een duidelijk slechtere overleving op twee jaar dan degenen die meer spiermassa behielden, wat benadrukt dat sepsisgerelateerd verlies van spieren niet alleen cosmetisch is — het hangt samen met lange termijn mortaliteit.
Wat dit kan betekenen voor toekomstige behandelingen
Samengenomen schetsen de muizen-, cel- en patiëntgegevens een plausibel verhaal: tijdens sepsis activeert de sterk verhoogde IL‑6 STAT3 in spier, wat op zijn beurt een eiwitafbrekend systeem opvoert dat spiervezels van hun contractiele componenten berooft. Autofagie neemt ook toe maar lijkt minder rechtstreeks door STAT3 te worden aangestuurd. Door STAT3 farmacologisch te blokkeren met C188‑9 konden de onderzoekers deze «zelf‑kanibalisatie»‑route onderbreken in muizen en gekweekte spiercellen, waardoor kracht behouden bleef zelfs terwijl de infectie en ontsteking voortduurden. Hoewel dit werk nog preklinisch is en niet bewijst dat STAT3‑remmers menselijke patiënten zullen helpen, wijst het op de IL‑6/STAT3‑as als een veelbelovend doelwit voor geneesmiddelen die bedoeld zijn om het ingrijpende krachtverlies te voorkomen of te verminderen dat veel overlevenden van sepsis treft.
Bronvermelding: Ono, Y., Saito, M., Yoshihara, I. et al. Sepsis-associated skeletal muscle wasting is ameliorated by pharmacological inhibition of the STAT3 signaling pathway in mice. Sci Rep 16, 5008 (2026). https://doi.org/10.1038/s41598-026-35815-9
Trefwoorden: sepsis, spierverlies, STAT3, ontsteking, herstel na kritieke ziekte