Clear Sky Science · nl
Lichte SwiM-UNet met multidimensionale adapter voor efficiënte medische beeldsegmentatie op het apparaat
Slimmere scans bij het bed
Hersenscans kunnen levensbedreigende tumoren onthullen, maar het omzetten van ruwe beelden naar duidelijke contouren waar artsen op kunnen handelen is nog steeds traag en rekenintensief. Deze studie introduceert SwiM‑UNet, een nieuw algoritme dat hersentumoren uit 3D‑MRI-scans kan segmenteren met toonaangevende nauwkeurigheid terwijl het efficiënt draait op lokale apparaten, waardoor nauwkeurige beeldanalyse dichter bij het bed van de patiënt of zelfs in mobiele klinieken komt. 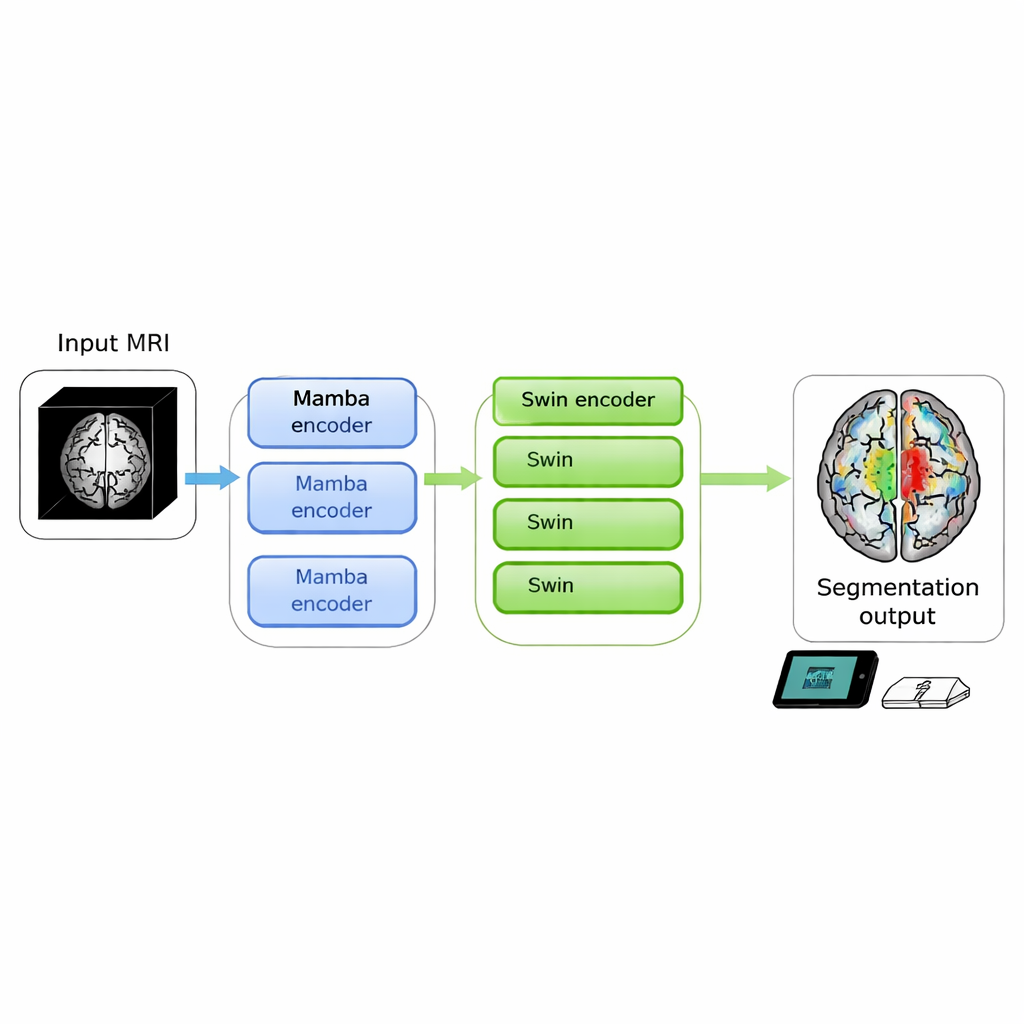
Waarom nauwkeurige tumorencontouren ertoe doen
De moderne geneeskunde is sterk afhankelijk van beeldvorming om operaties, bestralingstherapie en medicamenteuze behandelingen te plannen. Voor hersentumoren moeten artsen niet alleen vaststellen dat er een tumor is, maar precies weten waar verschillende delen beginnen en eindigen. Deze taak, segmentatie genoemd, wordt meestal door specialisten uitgvoerd of per plakje bijgesteld — een tijdrovend proces dat beslissingen kan vertragen en tussen experts kan verschillen. Geautomatiseerde segmentatiehulpmiddelen op basis van deep learning hebben deze situatie verbeterd, maar de meest nauwkeurige methoden vereisen vaak grote grafische processors, waardoor ze moeilijk direct in de kliniek inzetbaar zijn, vooral op kleinere of draagbare machines.
Twee krachtige ideeën die niet gemakkelijk op kleine apparaten passen
Recente doorbraken in computerzicht komen voornamelijk uit twee modelfamilies. Transformer‑gebaseerde systemen, zoals de Swin Transformer, zijn uitstekend in het herkennen van globale patronen over een volledige 3D‑scan en hebben top presterende hersentumorsegmenters mogelijk gemaakt. Hun kernbewerking, zelf‑attention, wordt echter extreem kostbaar naarmate de beeldgrootte toeneemt, wat hun gebruik in real‑time of op compacte hardware beperkt. Een nieuwere familie, bekend als Mamba en gebaseerd op state‑space modellen, biedt een slimme omweg: het verwerkt sequenties in effectief lineaire tijd en vermindert het aantal benodigde berekeningen. Vroege experimenten in medische beeldvorming toonden aan dat Mamba‑achtige modellen snel en efficiënt zijn, maar meestal achterblijven bij transformers qua segmentatiekwaliteit, vooral bij complexe tumorvormen.
Snelheid en nauwkeurigheid verenigd in één ontwerp
De auteurs stelden zich tot doel de sterke punten van beide werelden in één 3D‑model te combineren. Hun SwiM‑UNet behoudt de bekende U‑vormige structuur die veel wordt gebruikt in medische beeldvorming, met een encoder die informatie comprimeert en een decoder die gedetailleerde segmentaties herstelt. In de vroege stadia, waar de scan nog groot en hoogresolutief is, gebruiken ze efficiënte Mamba‑blokken om de berekeningen beheersbaar te houden. Dieper in het netwerk, nadat de data zijn gedownsampled, schakelen ze over naar gestroomlijnde Swin Transformer‑blokken die nu langeafstandrelaties kunnen modelleren zonder de hardware te overbelasten. Een op maat gemaakte brug, de MS‑adapter, koppelt deze twee regimes. Deze kijkt naar kenmerken langs breedte, hoogte en diepte van het volume afzonderlijk, en ook over kanalen heen, en leert via kleine gating‑units hoeveel elk perspectief het uiteindelijke beeld moet beïnvloeden. 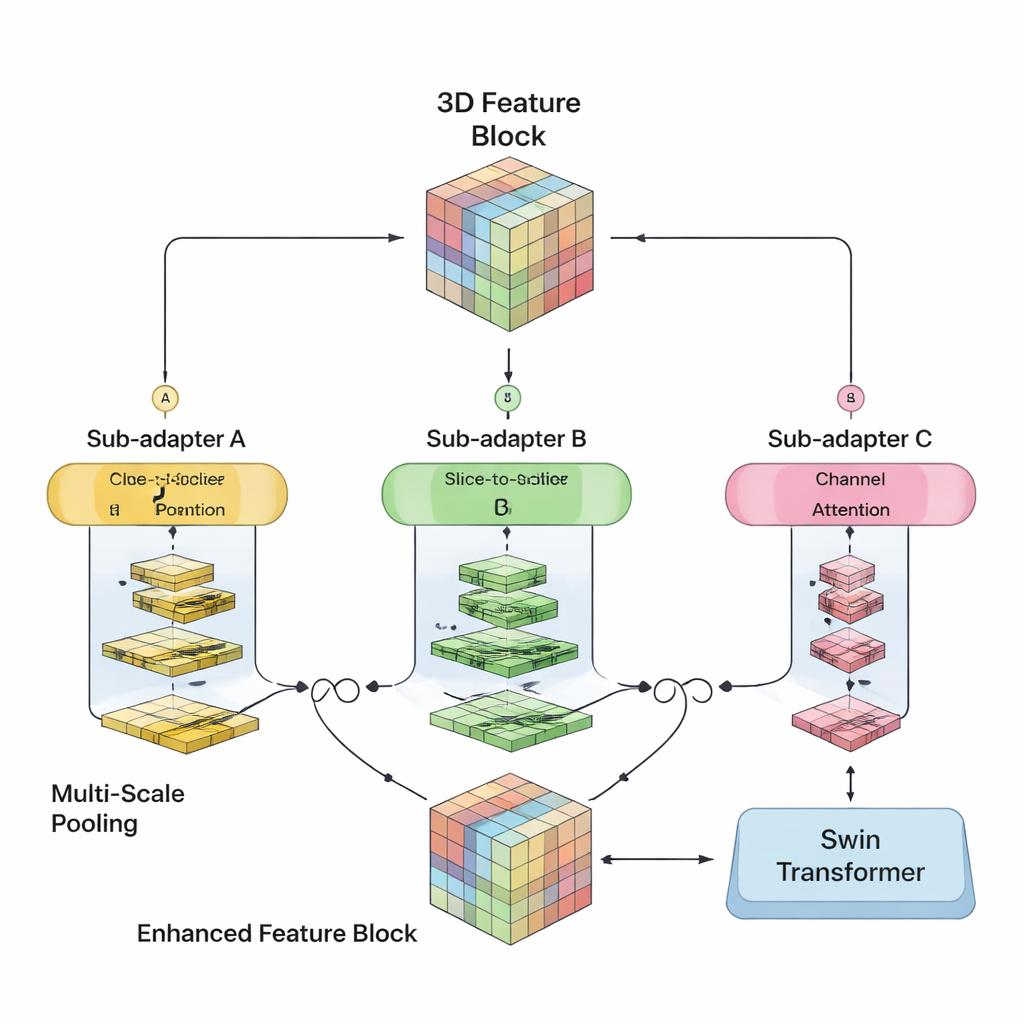
Meer doen met minder berekeningen
Bovenop deze hybride opzet reduceert het team overtollige berekeningen door lage‑rang volledig verbonden lagen te gebruiken en een decoder die het aantal te verwerken kanalen bewust vermindert. Ze testten meerdere varianten met verschillende combinaties van Mamba‑ en Swin‑lagen en vonden dat het gebruik van Mamba in de eerste drie encodervlakken en Swin alleen in de diepste laag de beste balans tussen snelheid en nauwkeurigheid gaf. Op twee grote openbare hersentumordatasets uit de BraTS 2023 en 2024 uitdagingen behaalde SwiM‑UNet hogere nauwkeurigheid en scherpere grenzen dan toonaangevende uitsluitend‑transformer, uitsluitend‑Mamba en eerdere hybride modellen, terwijl het veel minder floating‑point‑operaties gebruikte en de inferentietijd terugbracht tot ongeveer 45 milliseconden per scanpatch op een moderne grafische kaart.
Klaar voor real‑world apparaten
Om te controleren of deze voordelen buiten het lab relevant zijn, vergeleken de auteurs de rekenkundige eisen van het model met de mogelijkheden van typische klinische edge‑systemen — draagbare MRI‑consoles, point‑of‑care computers en operatiekamerworkstations. Hun analyse suggereert dat, in tegenstelling tot zwaardere transformer‑modellen, SwiM‑UNet comfortabel past binnen de stroom-, geheugen‑ en snelheidslimieten van dergelijke apparaten en vaak aan realtimevereisten voldoet. Het presteerde ook goed op een aparte buik‑CT dataset, wat aangeeft dat de aanpak kan generaliseren buiten hersentumoren en zelfs buiten MRI.
Wat dit betekent voor patiënten en clinici
In praktische termen toont SwiM‑UNet aan dat het mogelijk is de nauwkeurigheid van de meest geavanceerde segmentatiemodellen te benaderen terwijl de rekenlast licht genoeg blijft voor gebruik op het apparaat. Dat kan snellere, consistentere tumorencontouren mogelijk maken op de spoedeisende hulp, in landelijke ziekenhuizen of mobiele beeldvormingsunits zonder gevoelige scans naar verre servers te hoeven sturen. Hoewel verder werk nodig is om de methode aan te passen aan verschillende scanners en omstandigheden, wijst dit hybride ontwerp op een toekomst waarin hoogwaardige beeldanalyse draait waar de patiënt is, niet alleen in datacenters.
Bronvermelding: Noh, Y., Lee, S., Jin, S. et al. Lightweight SwiM-UNet with multi-dimensional adaptor for efficient on-device medical image segmentation. Sci Rep 16, 5807 (2026). https://doi.org/10.1038/s41598-026-35771-4
Trefwoorden: segmentatie van hersentumoren, medische beeldvorming AI, hybride neurale netwerken, inferentie op het apparaat, 3D MRI-analyse