Clear Sky Science · nl
KChIP1-splicevarianten moduleren Kv4-kanalen door P/C-type inactiveringskenmerken te bevorderen
Hoe kleine poriën het elektrische ritme van de hersenen vormen
Elke gedachte, herinnering en beweging in de hersenen berust op snelle elektrische signalen in zenuwcellen. Deze signalen worden fijn afgestemd door microscopische poriën — ionkanalen — die geladen deeltjes laten stromen. Dit artikel onderzoekt hoe subtiele varianten van een hulp-eiwit, KChIP1, het gedrag van één familie van dergelijke kanalen (Kv4-kanalen) wezenlijk kunnen veranderen, en daarmee beïnvloeden hoe makkelijk neuronen opeenvolgende elektrische activiteit kunnen vuren.
Kaliumkanalen als het rempedaal van de hersenen
Kv4-kanalen geleiden een zogenaamde A-type kaliumstroom die snel in- en uitschakelt in het cellichaam en de vertakkingen van neuronen. Deze stroom helpt te bepalen hoe gemakkelijk een neuron vuurt en hoe trouw het binnenkomende signalen kan volgen, vooral bij lage vuursnelheden. Kv4-kanalen werken niet alleen: ze assembleren met hulp-eiwitten in een drieledig complex dat DPP-eiwitten en KChIP-eiwitten omvat. Deze partners beïnvloeden hoe snel de kanalen uitschakelen en hoe snel ze weer klaar zijn om te openen. Tot nu toe suggereerde het meeste werk dat KChIPs over het algemeen maken dat Kv4-kanalen sneller herstellen nadat ze zijn uitgeschakeld, waardoor neuronen snel op herhaalde inputs kunnen reageren.
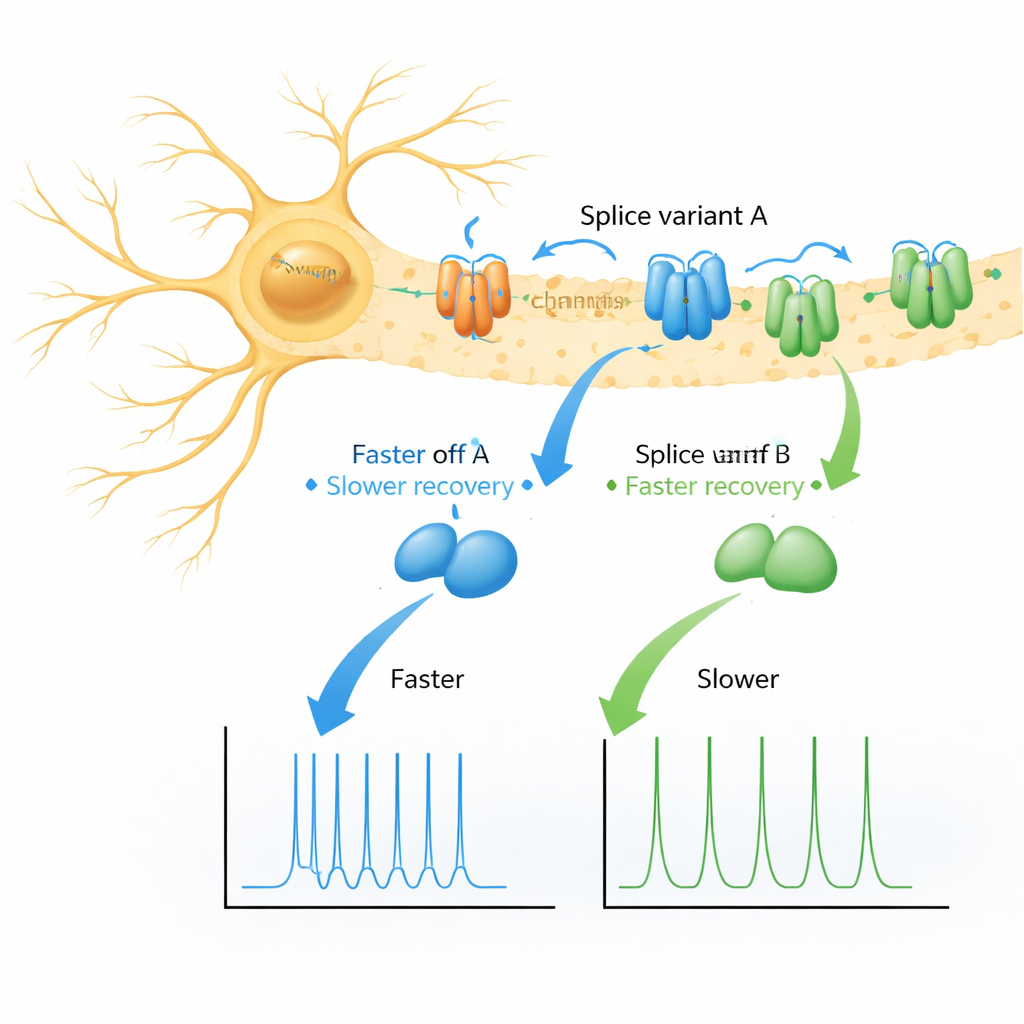
Twee eiwitvarianten, twee smaken van herstel
De auteurs richtten zich op twee vrijwel identieke versies (splicevarianten) van KChIP1, genoemd 1a en 1b, die alleen verschillen door een korte aromatische “staart” aan het begin van 1b. Met behulp van kikkereicellen als gecontroleerde testomgeving, brachten ze verschillende Kv4-kanaaltypes tot expressie alleen, met elk KChIP1-variant, met DPP, of met beide helper-eiwitten samen. Zoals verwacht vormden zowel 1a als 1b het uitschakelgedrag tijdens een spanningsstap licht om, zonder dramatische effecten. De verrassing kwam toen ze onderzochten hoe kanalen herstellen nadat ze waren uitgeschakeld: in plaats van één vloeiende terugkeer naar gereedheid, vertoonden kanalen gekoppeld aan zowel 1a als 1b twee verschillende herstelstadia — een snelle en een veel langzamere — waarbij de langzame route veel duidelijker naar voren kwam bij 1b.
Een verborgen langzaam pad onthuld
Wanneer Kv4-kanalen zonder KChIP1 werden tot expressie gebracht, herstelden ze via een eenvoudig, snel pad, en DPP versnelde dit nog verder. Toevoeging van KChIP1 veranderde dat patroon. Met 1a herstelde het merendeel van de kanalen nog steeds snel, maar een klein deel nam een langzaam omweggetje terug naar de gereedheidsstaat. Met 1b ging een veel groter aandeel deze langzame route in, waardoor het herstel zich over seconden uitstrekten. Dit effect trad op in alle geteste Kv4-subtypen en bleef bestaan zelfs met aanwezigheid van DPP, wat aangeeft dat het langzame pad een ingebouwd kenmerk is van KChIP1-bevattende complexen, en geen artefact van een specifiek kanaal of experimentele opzet. De auteurs vonden ook dat 1b het ‘uitschakel’-spanningsbereik van de kanalen naar meer negatieve waarden verschuift, waardoor ze tijdens aanhoudende activiteit nog meer geneigd zijn onbeschikbaar te zijn.
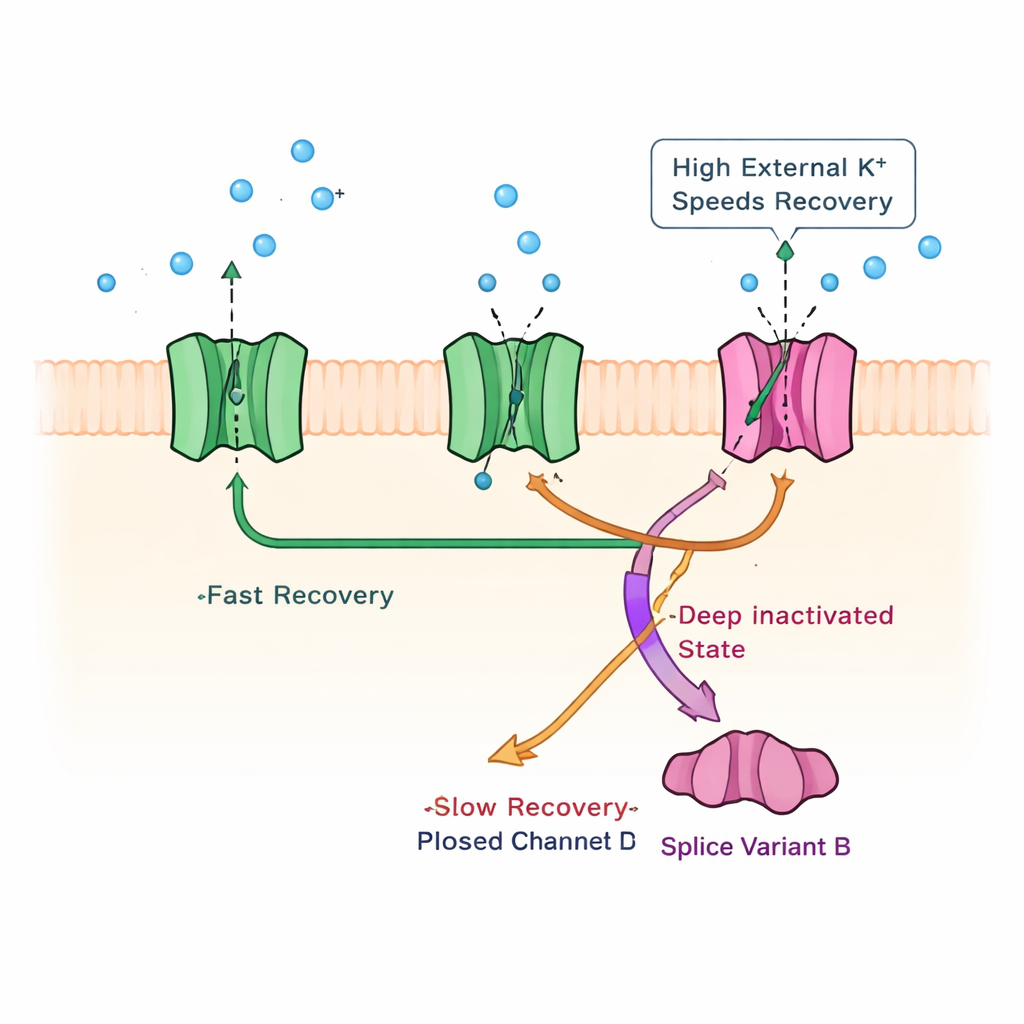
Het ontmaskeren van een slapende inactiveringsmechanisme
Om te begrijpen welke fysieke verandering in het kanaal dit trage herstel onderbouwt, onderzocht het team bekende inactiveringsmechanismen uit andere kaliumkanalen. Ze konden een klassieke ‘bal-en-keten’-blokkade aan de binnenmond van het kanaal uitsluiten door een deel van de interne staart van het kanaal af te knippen; de langzame fase bleef bestaan. Daarna gebruikten ze hoge niveaus van extern kalium, een truc die bekendstaat om poriegebaseerde inactivatieprocessen in andere kanalen te beïnvloeden. Onder deze omstandigheden werd het stilvallen van de stroom sneller, maar belangrijker: de langzame herstelcomponent versnelde specifiek, alsof het hoge kalium de kanalen bevrijdde uit een diepe, langdurige geblokkeerde toestand. Gericht uitgevoerde mutaties in een poortsegment van het kanaal ondersteunden verder het idee dat KChIP1b een poriegerichte inactiveringsroute bevordert — normaal zwak in Kv4-kanalen — die naast hun gebruikelijke, snellere gesloten-toestand-inactivatie coëxisteert.
Waarom dit ertoe doet voor hersenactiviteit
De bevindingen suggereren dat neuronen door te kiezen tussen KChIP1a, KChIP1b of mengsels van beide, nauwkeurig kunnen bijstellen hoe snel A-type stromingen herstellen tussen spikes. In cellen rijk aan KChIP1b raakt een aanzienlijk deel van de Kv4-kanalen ‘geparkeerd’ in een diepe, langzaam omkeerbare geïnactiveerde staat, waardoor hun beschikbaarheid tijdens snel vuren beperkt wordt. Dit kan bepaalde interneuronen — cellen die activiteit in hersencircuits coördineren en remmen — in staat stellen op hogere frequenties te vuren of afwijkende timingpatronen te tonen. In wezen ontgrendelt een kleine splice-variant van één hulp-eiwit een verborgen remmodus in kaliumkanalen, wat een nieuwe laag flexibiliteit toevoegt aan hoe de hersenen hun eigen elektrische ritmes beheersen.
Bronvermelding: Cao, W., Tachtsidis, G. & Bähring, R. KChIP1 splice variants modulate Kv4 channels by promoting P/C-type inactivation features. Sci Rep 16, 2632 (2026). https://doi.org/10.1038/s41598-026-35770-5
Trefwoorden: Kv4-kaliumkanalen, KChIP1-splicevarianten, A-type stroom, neurale prikkelbaarheid, channel inactivation