Clear Sky Science · nl
Voorkomen van antibioticaresistentiegenen in verschillende rioolwaterzuiveringssystemen en effluent‑geïrrigeerde bodems via metagenomische analyse
Waarom het water dat uit zuiveringsinstallaties komt nog steeds van belang is
Antibiotica hebben talloze levens gered, maar de microscopische genen die bacteriën resistent maken tegen deze middelen verdwijnen niet simpelweg als we ze doorspoelen. Deze studie onderzoekt wat er met antibioticaresistentiegenen gebeurt wanneer rioolwater door twee moderne zuiveringssystemen stroomt, en wat er gebeurt als het gezuiverde water vervolgens wordt gebruikt om bodems te beregenen in een droog gebied van China. De bevindingen tonen aan dat zelfs goed beheerde installaties knooppunten kunnen worden waar resistentiegenen veranderen, zich verspreiden en in het bredere milieu terechtkomen.
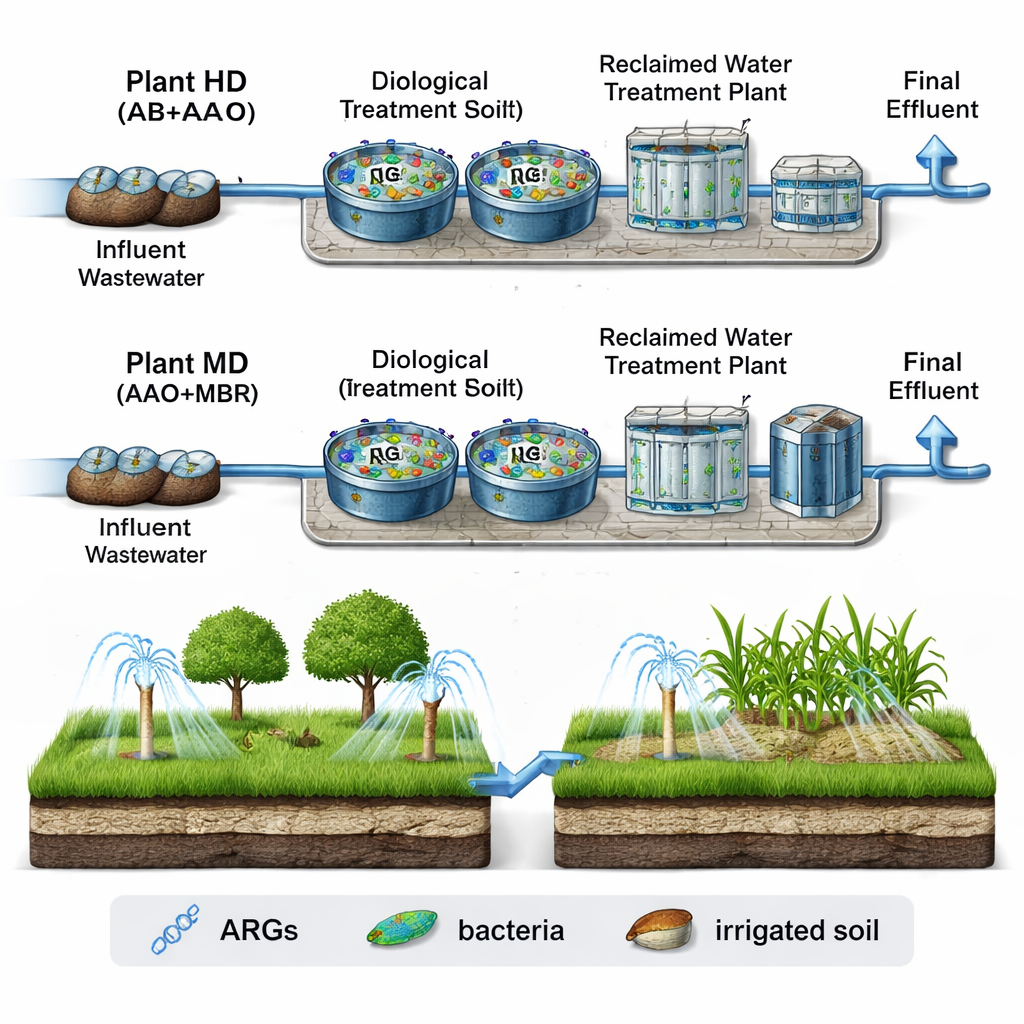
Van riolen naar sproeiers
De onderzoekers bestudeerden twee grootschalige rioolwaterzuiveringssystemen, aangeduid als HD en MD, in de stad Urumqi. Beide ontvangen een mengsel van huishoudelijk, ziekenhuis- en industrieel afvalwater, maar ze gebruiken verschillende procesketens. De ene combineert een adsorptie–bio‑oxidatiestap met een anaeroob–anoxisch–oxisch tanksysteem; de andere gebruikt dezelfde drie‑zones biologische stap gekoppeld aan een membraanbioreactor. In beide gevallen zorgt een afzonderlijke installatie voor gezuiverd water voor het nabezopen van het deels gezuiverde water voordat het wordt gebruikt voor irrigatie van parken, gazons en wegplantsoen. Door Zowel het inkomende rioolwater, het biologisch behandelde water, het eind‑effluent als de nabijgelegen bodems in zowel winter als zomer te bemonsteren, kon het team volgen hoe resistentiegenen zich langs dit hele pad verplaatsten.
Genen die veel medicijnen tarten
Middels metagenomische sequenering—een methode die het gecombineerde DNA van alle microben in een monster leest—brak het team 31 typen antibioticaresistentiegenen in kaart. De duidelijke koplopers waren genen die bacteriën beschermen tegen meerdere medicijnklassen tegelijk, gevolgd door genen die resistentie geven tegen tetracyclines, macroliden en aminoglycosiden, die veel gebruikt worden in de menselijke en veterinaire geneeskunde. Bepaalde specifieke gentyperingen, zoals msrE, mphE en ANT(6)-Ia, kwamen vooral veel voor in rauw rioolwater en bleven detecteerbaar zelfs na behandeling. Interessant genoeg veranderde de algemene samenstelling van resistentietypen weinig tussen winter en zomer, hoewel wintermonsters de neiging hadden iets meer resistentiegenen en een grotere diversiteit daarvan te bevatten.
Behandeling helpt—maar hervormt het probleem ook
De biologische tanks in deze systemen zijn ontworpen om organische verontreiniging af te breken, maar ze creëren ook dichte, voedingsrijke bacteriegemeenschappen die continu worden blootgesteld aan achtergebleven antibiotica en zelfs zware metalen. In het HD‑systeem nam deze fase de totale hoeveelheid en variatie aan resistentiegenen daadwerkelijk toe, waardoor de tanks hotspots van genetische uitwisseling werden. In het MD‑systeem verminderde de biologische behandeling de totale genabundantie enigszins, maar in beide installaties overleefden enkele sleutelgenen. De laatste nabezorgingsstap—met processen zoals aanvullende biologische behandeling, membranen en desinfectie met ultraviolet licht of ozon—verlaagde weliswaar het totale aantal resistentiegenen in het effluent. Toch kon deze stap ook nieuwe gentyperingen bevoordelen die goed tegen deze omstandigheden kunnen, wat betekent dat het totale aantal genen daalde terwijl de diversiteit soms toenam.
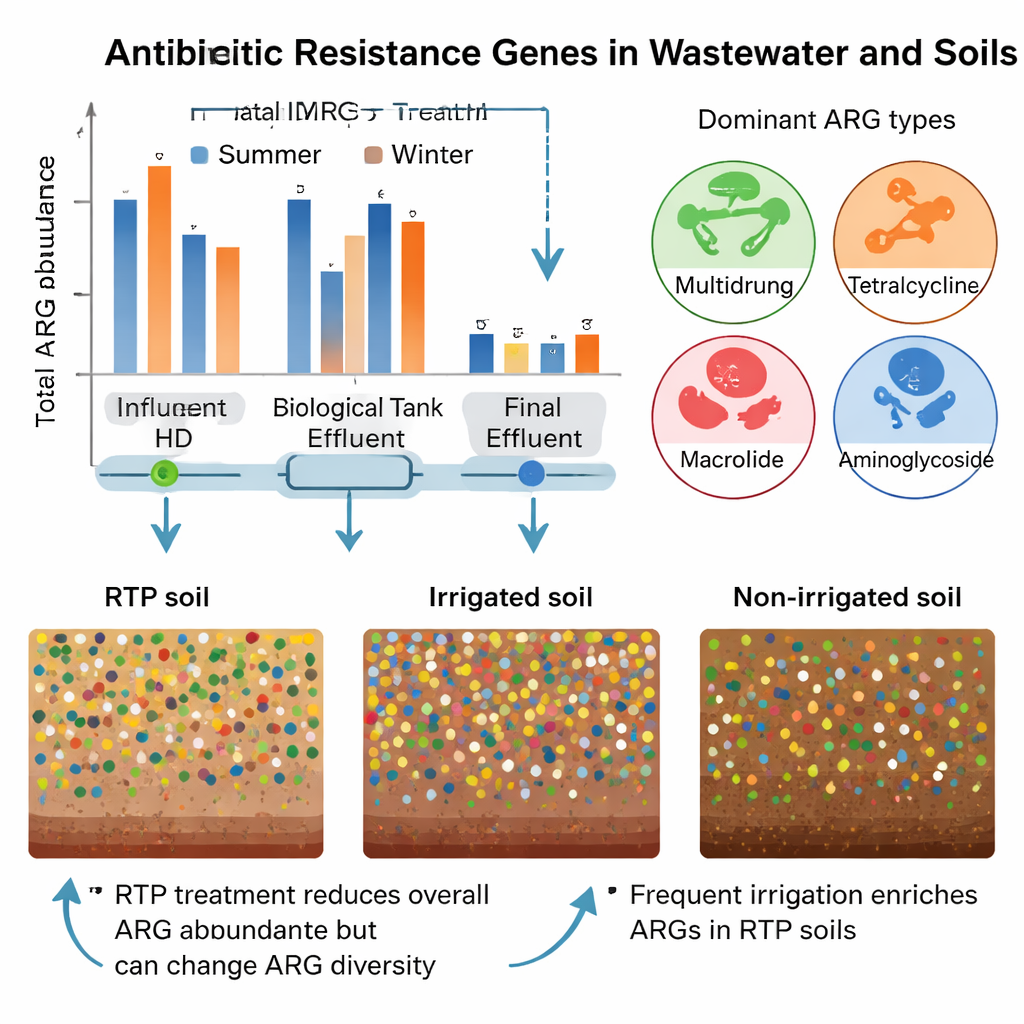
Wat er gebeurt als effluent de bodem bereikt
Om te onderzoeken hoe hergebruik van gezuiverd water land beïnvloedt, vergeleek het team bodems met verschillende irrigatiegeschiedenissen: binnen de installatie voor gezuiverd water zelf, in nabijgelegen groengebieden die regelmatig met effluent werden geïrrigeerd, en in een referentiegebied dat dit water nooit had ontvangen. Alle bodems bevatten resistentiegenen, wat zowel de natuurlijke achtergrond als vroegere menselijke activiteiten weerspiegelt. Bodems binnen de installatie, die het vaakst werden geïrrigeerd, hadden de hoogste genabundantie en diversiteit. Verrassend genoeg was de totale resistentie in geïrrigeerde parkbodems op de korte studieduur niet dramatisch hoger dan in niet‑geïrrigeerde bodems. Wel verschoof de samenstelling van de resistentie“gemeenschap”: sommige specifieke genen, zoals bepaalde tetracycline‑resistentiesubtypes, kwamen vaker voor in geïrrigeerde percelen, wat suggereert dat gezuiverd water de bodem eerder richting bepaalde resistentieprofielen duwt dan simpelweg alle genen tegelijk te verhogen.
Wie draagt deze genen—en waarom dat ertoe doet
Het team bracht ook in kaart welke bacteriegroepen geneigd waren welke genen te dragen. Veelvoorkomende rioolwatergenera zoals Arcobacter, Acinetobacter, Pseudomonas en Sphingomonas toonden sterke verbanden met meerdere resistentiegenen, waaronder diegenen die tegen veel medicijnen tegelijk beschermen. Zowel in water als in bodem waren sommige genen gekoppeld aan verschillende bacteriële gastheren, wat suggereert dat horizontale genoverdracht—het uitwisselen van DNA tussen microben—een belangrijke motor van verspreiding is. Toen de wetenschappers resistentiegenen vergeleken met gemeten antibioticaniveaus, vonden ze zowel positieve als negatieve correlaties. Dit duidt erop dat hoewel antibiotica duidelijk resistente microben kunnen bevoordelen, andere milieu‑drukfactoren, zoals metalen of algemene verontreiniging, ook mede bepalen waar en hoe deze genen blijven bestaan.
Wat dit betekent voor het dagelijks leven
Voor niet‑specialisten is de kernboodschap dat rioolwaterzuiveringsinstallaties weliswaar antibioticaresistentiegenen verminderen, maar ze niet uitwissen. Sommige behandelingsstappen kunnen bepaalde genen zelfs verrijken voordat latere stappen de totalen weer terugbrengen. Wanneer het resulterende effluent wordt gebruikt om parken en ander groen te irrigeren—zoals steeds vaker gebeurt in waterschaarse regio’s—kunnen resistentiegenen zich ophopen in nabijgelegen bodems en langzaam de onzichtbare microbieelsamenstelling onder onze voeten veranderen. De studie suggereert dat het verbeteren van de laatste nabezorgings‑ en desinfectiestappen, het nauwlettend monitoren van sleutelresistentiegenen en het extra letten op vaak geïrrigeerde locaties allemaal kunnen helpen de verspreiding van antibioticaresistentie in het milieu te beperken, zonder het waardevolle praktijk van waterhergebruik op te geven.
Bronvermelding: Fang, H., Pu, M., jiang, A. et al. Prevalence of antibiotic resistance gene in different wastewater treatment systems and effluent-irrigated soils through metagenomic analysis. Sci Rep 16, 5167 (2026). https://doi.org/10.1038/s41598-026-35758-1
Trefwoorden: antibioticaresistentiegenen, rioolwaterzuivering, gezuiverd water voor irrigatie, bodemmicrobioom, hergebruik van water