Clear Sky Science · nl
De rol van de α7-nicotinerge acetylcholinereceptor bij het bevorderen van M2-macrofagenpolarizatie op ontstekingsplaatsen
Hoe zenuwen helpen wegrakende ontsteking te kalmeren
Als we in een vinger snijden of een infectie bestrijden, start ons lichaam een ontstekingsreactie om ons te beschermen. Raakt die reactie echter te lang uitgeput, dan kan ze gezond weefsel beschadigen en chronische ziekten aanwakkeren. Deze studie onderzoekt hoe een specifieke "kalmerende" receptor op immuuncellen, de α7-nicotinerge acetylcholinereceptor (α7nAChR), helpt om ontsteking richting herstel in plaats van schade te sturen, en geeft daarmee aanwijzingen voor nieuwe behandelingen van aandoeningen zoals sepsis, darmziekten en artritis.
De twee gezichten van de immuunschoonmaakploegen
Macrofagen zijn immuuncellen die fungeren als schoonmaakploegen en reparatieteams. Ze kunnen schakelen tussen twee hoofdmodi. In hun "aanvals"modus, vaak M1 genoemd, geven ze agressieve stoffen af om ziekteverwekkers te doden en debris op te ruimen. In hun "herst"-modus, bekend als M2, laten ze signalen los die ontsteking dempen en weefselherstel bevorderen. Een gezonde reactie begint met meer M1-cellen en verschuift geleidelijk naar M2-cellen als het gevaar voorbij is. De auteurs wilden weten of α7nAChR, een receptor die oorspronkelijk bekend werd door zijn rol in zenuwcommunicatie en de effecten van nicotine op de hersenen, ook helpt macrophagen tijdens ontsteking naar die herstellende M2-toestand te leiden.
Een zenuwgekoppelde schakel naar herstel
Om dit te onderzoeken gebruikten de onderzoekers muizen die óf wel óf geen α7nAChR hadden en veroorzaakten ontsteking in de buikholte op twee manieren: met een bacterieel component (als infectie‑model) en met zacht darmmanipulatie (als model voor steriel chirurgisch letsel). Ze maten moleculaire markers die M1 van M2-gedrag onderscheiden en gebruikten flowcytometrie om de verhoudingen van elk macrofagetype te tellen. Bij normale muizen werd de vroege fase van ontsteking gedomineerd door M1-signalen, maar in de daaropvolgende één tot twee dagen stegen de markers van M2-cellen, wat een natuurlijke verschuiving naar herstel weerspiegelde. Bij muizen zonder α7nAChR waren daarentegen de pro‑inflammatoire markers hoger, de herstelmarkers lager en was het aandeel M2-macrofagen in het ontstoken gebied consistent verminderd, waardoor de lokale balans verschoof naar een M1‑rijke, meer schadelijke toestand.
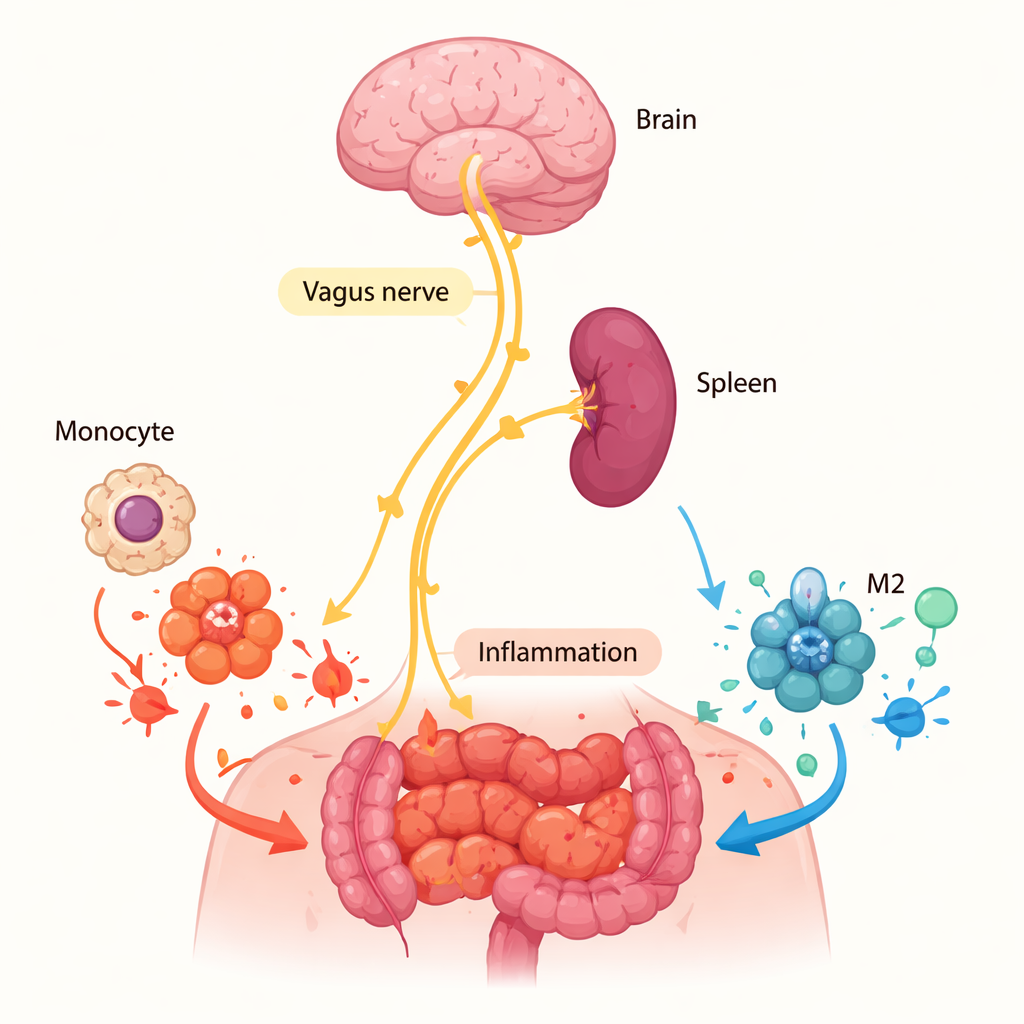
Waarom de milt belangrijker is dan de wond
Het team vroeg zich vervolgens af waar α7nAChR dit werk deed. De receptor had lokaal op de ontstekingsplek kunnen werken als cellen daar acetylcholine vrijgaven, de stof die de receptor activeert. Maar metingen van acetylcholine in de buikvloeistof en in celkweken uit het ontstoken weefsel gaven praktisch niets aan, wat tegen een sterke lokale signaalgeving pleit. De aandacht verschoof naar de milt, een belangrijk immuunorgaan dat al bekendstaat om deelname aan een "cholinergisch anti‑inflammatoir pad" dat door de vaguszenuw wordt gecontroleerd. Wanneer de onderzoekers de milt chirurgisch verwijderden bij normale muizen en vervolgens buikontsteking inducerenden, daalde het aandeel M2-macrofagen in de peritoneale holte en nam het totale aantal macrofagen af. Dit patroon spiegelde wat ze zagen bij muizen zonder α7nAChR en suggereert dat zenuwgestuurde signalen in de milt monocyten—de voorlopers van macrofagen—vooraf trainen om M2-cellen te worden nog voordat ze het ontstoken weefsel bereiken.
De schakel testen in menselijke cellen
Om te zien of dezelfde receptor menselijke cellen kan afstemmen, gebruikten de onderzoekers in het lab gekweekte monocyten uit een leukemiecelliglijn (THP‑1) en uit gedoneerd menselijk bloed. Ze leidden deze cellen naar ontwikkeling tot ofwel M1- of M2-macrofagen met standaard immuunsignalen en voegden daarna een specifiek α7nAChR‑activerend middel toe. In beide menselijke celbronnen verhoogde activatie van α7nAChR de M1‑markers niet, maar nam duidelijk belangrijke kenmerken van M2‑gedrag toe, waaronder het oppervlakte-eiwit CD206 en het anti‑inflammatoire molecuul interleukine‑10. Deze experimenten ondersteunen het idee dat α7nAChR als een biaserende schakel fungeert: het maakt het voor ontwikkelende macrofagen makkelijker om een herstellende identiteit aan te nemen zonder de immuunrespons simpelweg uit te schakelen.
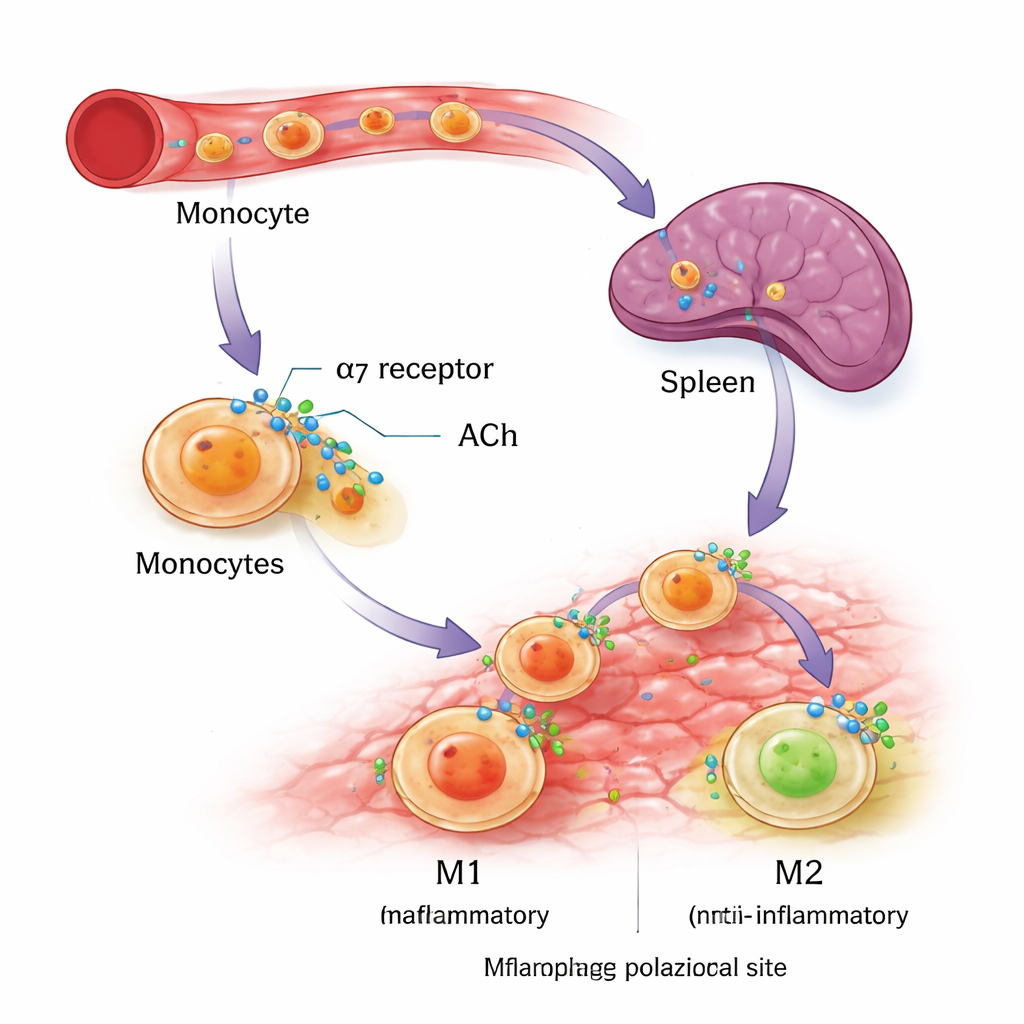
Van nicotineaanwijzingen naar toekomstige therapieën
De bevindingen helpen meerdere raadselachtige observaties te verklaren, zoals waarom stimulatie van de vaguszenuw ontstekingsziekten kan verbeteren en waarom rokers, ondanks veel gezondheidsrisico’s, schijnbaar een iets lager risico op bepaalde darmaandoeningen hebben—nicotine kan α7nAChR activeren. In plaats van alleen ontstekingsbevorderende stoffen te blokkeren, lijkt α7nAChR het lichaam te helpen zijn immuunschoonmaakploegen om te vormen tot meer herstelgerichte M2-cellen, met name via miltgebaseerde training van monocyten. Voor leken betekent dit dat ons zenuwstelsel meer doet dan pijn waarnemen of spieren aansturen; het coacht immuuncellen discreet wanneer ze moeten vechten en wanneer ze moeten herstellen. Leren hoe we deze ingebouwde schakel veilig kunnen omzetten met medicijnen of gerichte zenuwstimulatie kan nieuwe manieren openen om schadelijke ontsteking te kalmeren terwijl het vermogen van het lichaam om zichzelf te verdedigen behouden blijft.
Bronvermelding: Mihara, T., Tanabe, H., Nonoshita, Y. et al. The role of the α7 nicotinic acetylcholine receptor in promoting M2 macrophage polarization at inflammatory sites. Sci Rep 16, 5267 (2026). https://doi.org/10.1038/s41598-026-35757-2
Trefwoorden: macrofagenpolarizatie, ontsteking, vaguszenuw, nicotinerge acetylcholinereceptor, immuunregulatie