Clear Sky Science · nl
Fysiologisch relevante vormen van Tc- en Re-pyrofosfaat radioactieve tracers en de basis van hun transthyretine-amyloïdegevoeligheid
Waarom dit hartbeeldvormingsverhaal ertoe doet
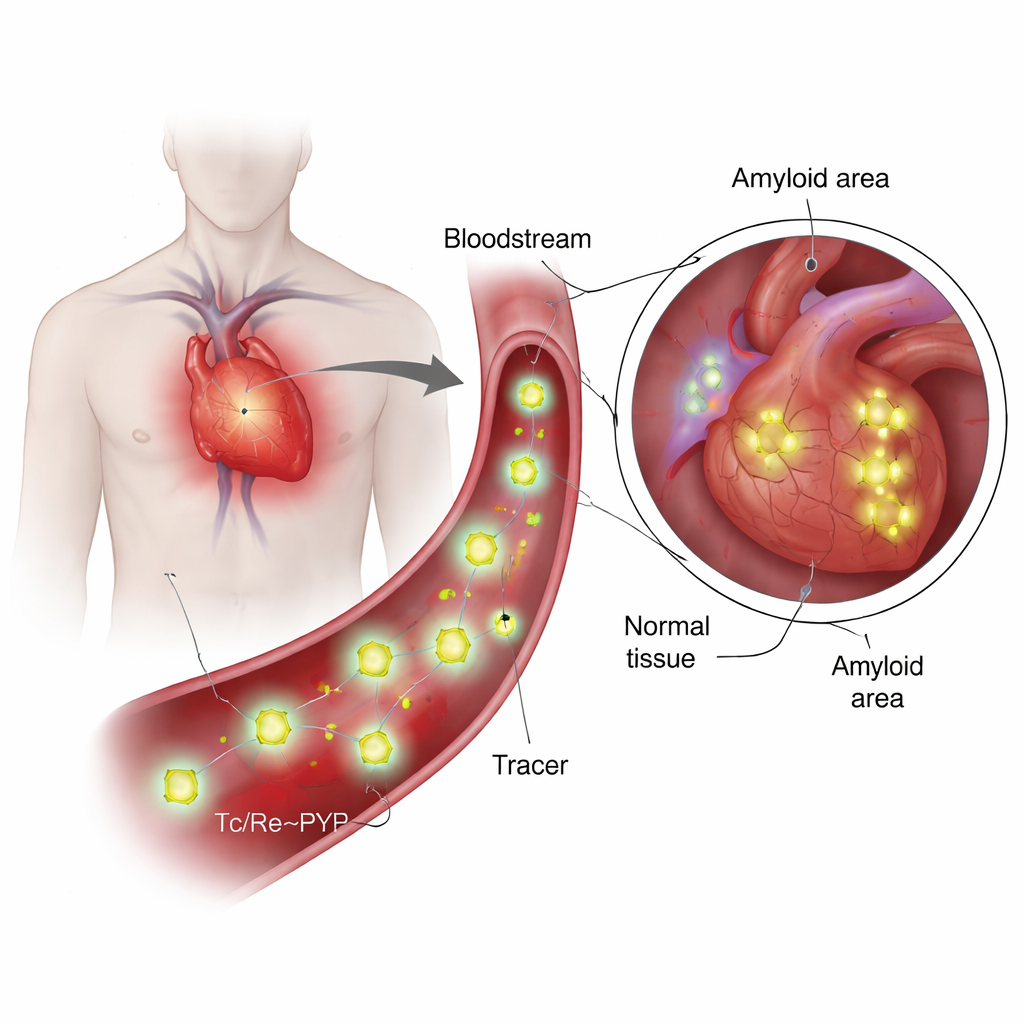
Veel mensen ontwikkelen naarmate ze ouder worden stille afzettingen van verkeerd gevouwen eiwitten, amyloïden genoemd, in het hart. Sommige van die afzettingen, vooral die opgebouwd uit een bloed-eiwit genaamd transthyretine, kunnen het hart verstijven en tot ernstige ziekte leiden. Artsen vertrouwen steeds vaker op een radioactieve tracer die bekendstaat als technetium‑99m pyrofosfaat (99mTc‑PYP) om deze afzettingen op scans zichtbaar te maken. Toch is het verrassend dat de precieze vorm van deze tracer in het lichaam en waarom hij een voorkeur lijkt te hebben voor bepaalde amyloïde typen niet duidelijk was. Dit artikel combineert theorie en experiment om te onthullen hoe de tracer er onder lichaamsachtige omstandigheden werkelijk uitziet en hoe die vorm het in staat kan stellen zich te richten op schadelijke transthyretinefibrillen.
Wat zijn deze tracers en waarom zijn ze bijzonder?
99mTc‑PYP wordt al decennia gebruikt voor het beeldvormen van botten, omdat het de neiging heeft zich te concentreren waar calcium en mineraalvernieuwing hoog zijn. Recente observaties toonden echter dat het ook onderscheid kan maken tussen twee belangrijke soorten cardiale amyloïdose: één opgebouwd uit antilichaam lichtketens (AL) en één uit transthyretine (ATTR). Bij ATTR licht het hart op PYP-scans vaak sterk op, terwijl AL-gevallen doorgaans zwak blijven, zelfs wanneer calciumophoping vergelijkbaar lijkt. Deze discrepantie riep een cruciale vraag op: hecht de tracer alleen aan calcium, of gaat hij een directe interactie aan met het amyloïde-eiwit zelf? Dat beantwoorden vereist kennis van de werkelijke chemische structuur van de tracer onder bloedachtige omstandigheden, iets dat eerder werk slechts globaal had geschetst.
Gebruik van een veiliger plaatsvervanger om het onzichtbare te zien
Aangezien technetium radioactief is en slechts in zeer kleine hoeveelheden aanwezig in medische preparaten, is het moeilijk om het rechtstreeks met veel labtechnieken te bestuderen. De auteurs gebruikten daarom rhenium, een nauw verwant element met nagenoeg dezelfde grootte en bindingsvoorkeuren maar handiger chemie, als plaatsvervanger. Ze bereidden rhenium‑pyrofosfaatmengsels onder omstandigheden die klinische PYP‑kits nabootsen en onderzochten deze met een batterij aan technieken: geavanceerde kwantumchemische berekeningen, UV‑zichtbare absorptie, diverse vibratiespectroscopieën (infrarood en Raman), kernspinresonantie, massaspectrometrie en tin Mössbauer‑spectroscopie. Samen stelden deze methoden hen in staat veel kandidaat‑structuren te toetsen en te vernauwen welke soorten waarschijnlijk bestaan bij neutrale pH, zoals die van bloed.
Een flexibele maar herkenbare moleculaire vorm
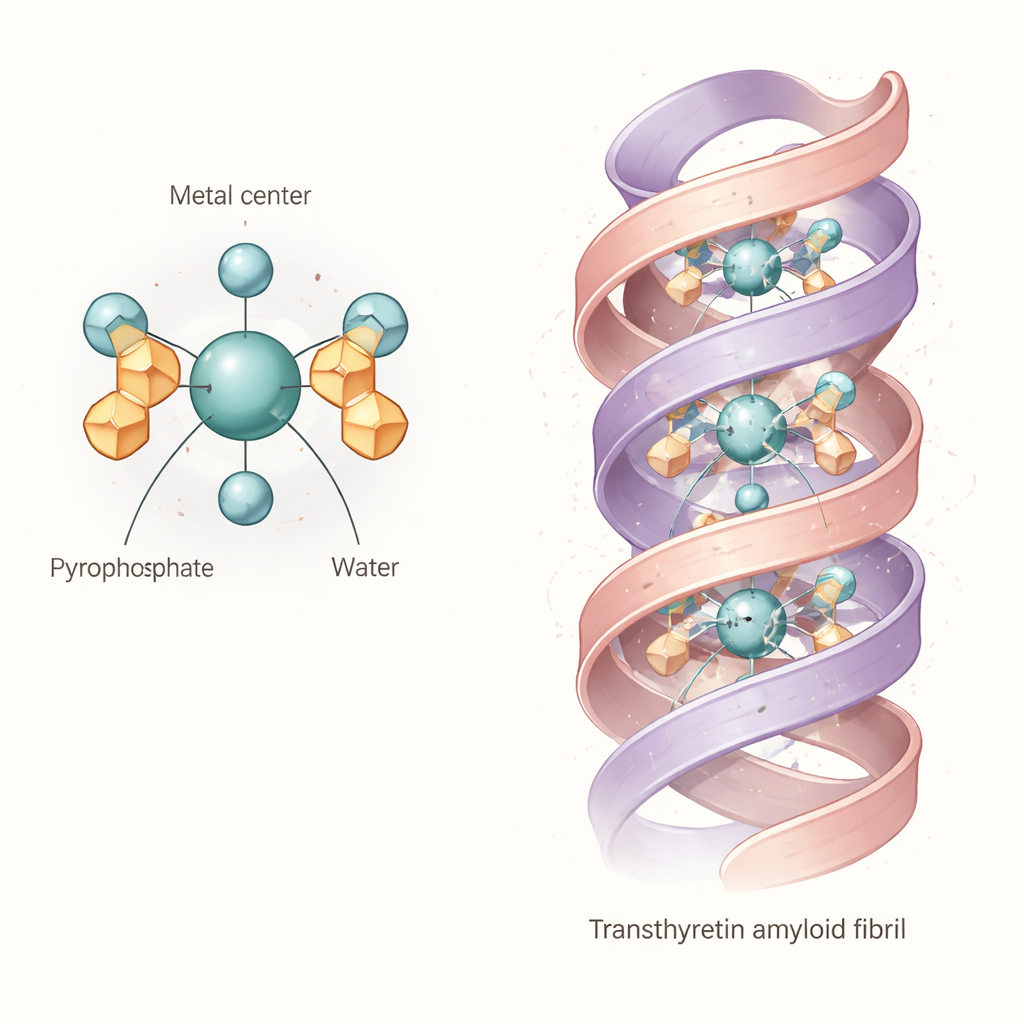
Het gecombineerde bewijs wijst op een gemeenschappelijke "kern"structuur: een octaëdrisch complex waarin een technetium‑ of rheniumatoom in de oxidatietoestand +4 gebonden is aan twee pyrofosfaatgroepen en twee watermoleculen. Simpel gezegd zit het metaal in het midden van een vrijwel octaëdrische kooi gevormd door zuurstofatomen, waarbij de pyrofosfaten fungeren als meerpuntige ankers en de watermoleculen de resterende posities innemen. Deze basale diaqua‑dipyrofosfaateenheid is niet rigide. Omdat de pyrofosfaatarmen kunnen draaien en interne waterstofbruggen met de gebonden wateren kunnen vormen, neemt het molecuul in oplossing vele licht verschillende vormen aan. Berekeningen en spectra suggereren dat deze variaties zijn lichtabsorptie- en vibratiekenmerken verschuiven, wat verklaart waarom experimentele banden breed zijn en waarom eerdere studies moeite hadden om één duidelijke structuur vast te stellen.
Wat dit betekent voor binding aan hartamyloïde
De auteurs vroegen zich vervolgens af of dit flexibele complex zich aannemelijk direct in transthyretine‑amyloïde‑fibrillen zou kunnen nestelen. Met behulp van een gedetailleerde cryo‑elektronenmicroscopie‑structuur van een menselijke transthyretinefibril voerden ze computerdocking‑zoeken uit met het gemodelleerde technetium‑pyrofosfaatcomplex. De resultaten tonen aan dat de diaqua‑dipyrofosfaateenheid in een centrale kanaal langs de fibril kan passen, en meerdere waterstofbruggen en zoutbruggen kan vormen met geladen zijketens die de holte bekleden. Dit suggereert dat, althans voor sommige transthyretinefibrilvormen, de tracer niet alleen nabijgelegen mineraalafzettingen markeert; hij kan direct door het eiwitraamwerk worden vastgehouden. De structurele "geef" in de tracer helpt hem waarschijnlijk aan te passen aan licht verschillende pocketvormen en ladingspatronen in echte patiëntfibrillen.
Gevolgen voor diagnose en toekomstige tracers
Voor de lezer zonder specialistische achtergrond is de conclusie dat de veelgebruikte PYP‑hartscan gebaseerd is op een tracer die subtieler en meer eiwitbewust is dan eerder werd aangenomen. Onder fysiologische omstandigheden is het het beste te beschouwen als een kleine, waterdragende metaal‑pyrofosfaatkooi die kan buigen en meerdere contactpunten kan vormen met transthyretine‑amyloïdekanalen. Dit inzicht helpt verklaren waarom de tracer sterke signalen toont bij sommige amyloïdeziekten maar niet bij andere, en waarom kleine veranderingen in het eiwit of zijn omgeving puzzelende verliezen aan gevoeligheid kunnen veroorzaken. Door de werkende vorm en het ladingspatroon van de tracer te verduidelijken, legt de studie een basis voor het ontwerpen van volgende generatie beeldvormings‑ of therapeutische middelen die ziekteveroorzakende fibrillen in het hart en daarbuiten selectiever herkennen.
Bronvermelding: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Trefwoorden: cardiale amyloïdose, transthyretine, technetiumpyrofosfaat, moleculaire beeldvorming, radiotracerchemie