Clear Sky Science · nl
Synergetische antipersister-, effluxremmende en antibiofilmactiviteit van vaginale door Lactobacillus afgeleide postbiotica tegen UPEC: richting een nieuw therapeutisch middel voor urineweginfecties
Waarom hardnekkige urineweginfecties ertoe doen
Urineweginfecties (UWI’s) behoren tot de meest voorkomende bacteriële infecties, vooral bij vrouwen, en veel mensen krijgen ze herhaaldelijk ondanks behandeling met antibiotica. Deze studie onderzoekt een nieuwe, antibiotica-sparende manier om die hardnekkige terugkerende infecties aan te pakken: gebruikmaken van behulpzame vaginale bacteriën en hun chemische bijproducten om probleemverwekkende E. coli te stoppen voordat ze zich vestigen, verbergen en terugkeren.
De verborgen overlevers achter terugkerende infecties
Standaardantibiotica kunnen de meeste bacteriën uitroeien, maar een kleine subpopulatie, bekend als “persistercellen”, overleeft door in een dormante, laagactieve toestand te gaan. Deze sluimers zijn niet genetisch resistent, maar ze verdragen zeer hoge antibiotica-doseringen en kunnen later weer actief worden, wat chronische en terugkerende UWI’s aandrijft. De onderzoekers werkten met een veelvoorkomende UWI-veroorzakende stam, E. coli UTI89, en toonden aan dat krachtige antibiotica zoals colistine en meropenem deze persistercellen gemakkelijk triggeren. In laboratoriumtesten die urine nabootsen, overleefden kleine fracties van E. coli extreme antibiotica-exposure, wat bevestigt hoe makkelijk persisters kunnen ontstaan en waarom standaard regimes vaak geen blijvende verlichting bieden.
Vriendelijke vaginale bacteriën inzetten als behandeling
Een gezonde vagina wordt meestal gedomineerd door Lactobacillus-soorten, die helpen schadelijke microben onder controle te houden. In plaats van levende “probiotische” bacteriën te gebruiken, richtte deze studie zich op hun celvrije supernatant — in wezen het cocktail van door hen uitgescheiden moleculen, genoemd postbiotica. Uit vaginale Lactobacillus-stammen verkregen van gezonde vrouwen scheidde het team deze secreties en analyseerde ze. Twee belangrijke metabolieten, itaconzuuranhydride en (−)-terpinen-4-ol, vielen op vanwege hun vermogen om samen te werken en het aantal E. coli-persistercellen sterk te verminderen wanneer ze in combinatie met antibiotica werden gebruikt. Een derde verbinding, tryptamine, waarvan eerder is aangetoond dat het de slijmerige biofilmmatrix die bacteriën bouwen afbreekt, werd toegevoegd om de antibiofilmwerking te versterken.
Hoe het nieuwe mengsel moeilijk te doden bacteriën verzwakt
De wetenschappers vonden dat deze door Lactobacillus afgeleide moleculen E. coli-persisters op meerdere fronten tegelijk aanvallen. Ten eerste verhogen ze de productie van reactieve zuurstofsoorten — chemisch reactieve vormen van zuurstof die bacteriële componenten beschadigen — waardoor antibiotica veel dodelijker worden voor dormante cellen. Wanneer antioxidanten werden toegevoegd, nam dit dodeffect af, wat de rol van oxidatieve stress benadrukt. Ten tweede maken de verbindingen de buitenmembraan van bacteriën meer “lekkend”, zoals aangetoond met fluorescente kleurstoffen die gemakkelijker in cellen binnendringen na behandeling. Ten derde remmen ze cellulair “effluxpompen”, kleine exportmachines die normaal antibiotica weer uit de cel pompen. Met de pompen geblokkeerd blijft er meer medicijn in de bacteriën en overleven minder persisters. Gezamenlijk verminderden deze veranderingen reeds gevormde E. coli-biofilms in laboratoriumtesten met tot wel tien ordes van grootte, zonder de geteste doses schadelijk te laten zijn voor zoogdier-immuuncellen.
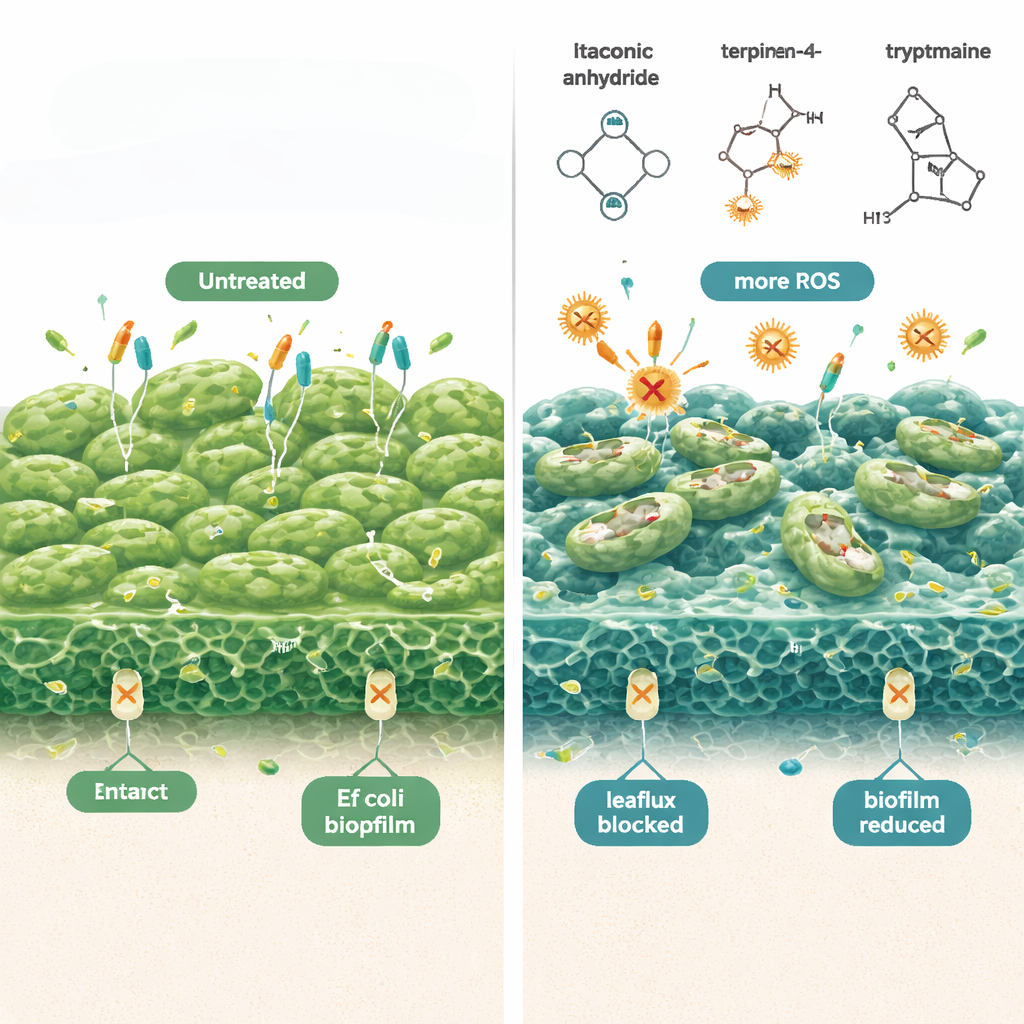
Van laboratoriumbank naar praktische vaginale wasoplossing
Om deze bevindingen bruikbaar te maken voor dagelijks gebruik, ontwierp het team een op maat gemaakte vaginale wasoplossing met een thermogevoelige gelbasis genaamd poloxameer 407. Bij kamertemperatuur gedraagt het zich als een vloeistof voor gemakkelijke toepassing en wordt het bij lichaamstemperatuur zachtjes dikker om het contact met de vaginawanden te verbeteren. De gel bevat een gedefinieerde, veilige combinatie van itaconzuuranhydride, (−)-terpinen-4-ol en tryptamine. Op laboratoriumplaten werkte deze formulering over een reeks pH-waarden vergelijkbaar met vaginale omstandigheden, onderdrukte sterk de vorming van E. coli-biofilms en verminderde het aantal levende bacteriën met ongeveer negen ordes van grootte. Het bleef ten minste drie maanden stabiel en biologisch actief bij koele opslag en liet ook brede werkzaamheid zien tegen andere problematische bacteriën zoals Klebsiella, MRSA en Pseudomonas.
Veiligheidstests en bescherming bij muizen
Vervolgens evalueerden de onderzoekers de wasoplossing in een muismodel van vaginale E. coli-infectie. Muizen werden geïnfecteerd met oplichtende (GFP-getagde) E. coli en vervolgens behandeld met de nieuwe metaboliet-wash, een probiotische wash met levende Lactobacillus, een commerciële vaginale was of een placebobasis. Dieren die de aangepaste metaboliet-wash kregen, toonden aanzienlijk minder vaginale ontsteking, behielden hun lichaamsgewicht en hadden veel lagere bacteriële aantallen in vaginale afscheiding vergeleken met de andere groepen. Het meest opvallend was dat bij behandelde muizen geen detecteerbare E. coli aanwezig was in urine, blaas, nieren of vaginale weefsels en dat ze normale nierfunctie behielden, wat aangeeft dat de formulering niet alleen de lokale infectie verminderde maar ook spreiding naar de hogere urinewegen voorkwam.
Wat dit kan betekenen voor mensen met terugkerende UWI’s
De studie concludeert dat een vaginale was samengesteld uit precieze metabolieten van van nature beschermende Lactobacillus-soorten UWI-veroorzakende E. coli op meerdere manieren kan verzwakken: het verkleinen van persisterpopulaties, het verstoren van biofilms en het verbeteren van de werking van standaardantibiotica. Omdat de benadering steunt op niet-levende moleculen in plaats van levende bacteriën of langdurige kuren met systemische geneesmiddelen, kan het veiliger, stabieler en gemakkelijker te reguleren zijn. Hoewel humane onderzoeken nog nodig zijn, wijst deze op metabolieten gebaseerde wash op een toekomst waarin terugkerende UWI’s niet alleen bestreden worden met sterkere antibiotica, maar door slim de eigen microbiële verdediging van het lichaam bij de bron te versterken.
Bronvermelding: Nair, V.G., Chellappan, D.R., Durai, R.D. et al. Synergistic antipersister, efflux inhibitory & antibiofilm activities of vaginal Lactobacillus-derived postbiotics against UPEC: toward a novel therapeutic for utis. Sci Rep 16, 5005 (2026). https://doi.org/10.1038/s41598-026-35736-7
Trefwoorden: urineweginfectie, vaginale microbiota, Lactobacillus-postbiotica, antibiotica-tolerantie, bacteriële biofilms