Clear Sky Science · nl
HIV Vpr induceert demethylering van de SNCA-antisensepromoter, wat leidt tot neurocognitieve stoornissen
Waarom HIV nog steeds de hersenen kan aantasten
Mensen die met HIV leven worden dankzij moderne antiretrovirale medicijnen ouder en gezonder. Toch ervaren velen nog steeds problemen met geheugen, concentratie en beweging, ook wanneer het virus in hun bloed goed onder controle is. Deze studie onderzoekt waarom dat gebeurt door in te zoomen op een klein viraal eiwit, Vpr, en een herseneiwit, alpha-synucleïne, dat ook een centrale rol speelt bij de ziekte van Parkinson. Inzicht in hoe deze twee moleculen elkaar beïnvloeden kan verklaren waarom HIV het hersenverouderingsproces versnelt en wijzen op nieuwe manieren om de hersenen te beschermen.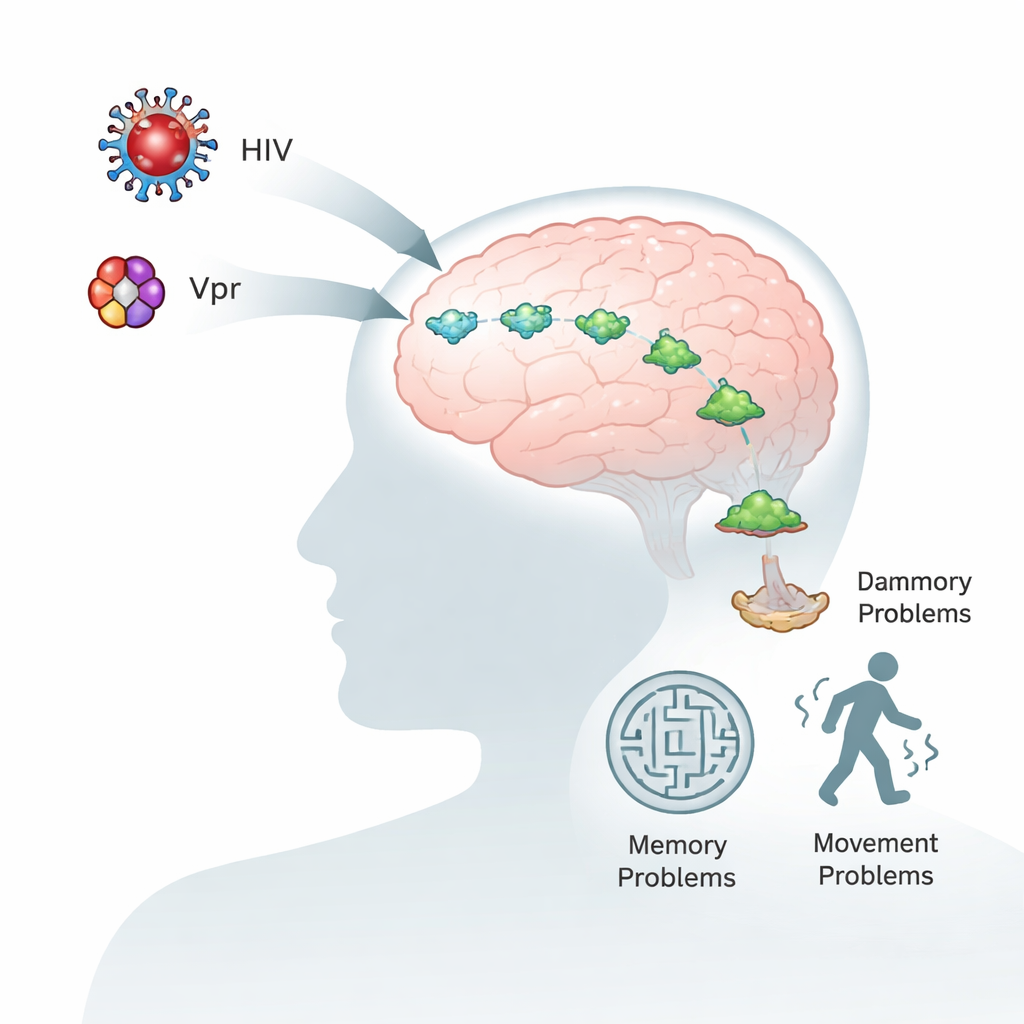
Een herseneiwit op het kruispunt van HIV en Parkinson
Alpha-synucleïne is een eiwit dat zenuwcellen helpt communiceren, vooral in hersengebieden die beweging en geheugen regelen. Wanneer te veel alpha-synucleïne zich ophoopt, klontert het samen tot aggregaten die synapsen beschadigen, de energieproducerende mitochondriën belasten en ontsteking aanwakkeren. Zulke klonten zijn kenmerkend voor de ziekte van Parkinson. De auteurs tonen aan dat alpha-synucleïne ook bij normale veroudering in muizen toeneemt, en dat het HIV-eiwit Vpr de niveaus nog verder verhoogt in zenuwachtige cellen. Daardoor staat alpha-synucleïne op het kruispunt tussen HIV-gerelateerde denkstoornissen en klassieke bewegingsstoornissen.
Hoe een viraal eiwit de cellulaire "punctuatie" herschrijft
Elke cel gebruikt chemische labels op DNA—vaak beschreven als moleculaire leestekens—om genen aan of uit te zetten. In dit werk richtte het team zich op een weinig bekende schakelaar binnen het alpha-synucleïne-gen, de zogenaamde antisensepromoter. In gezonde cellen is deze schakelaar sterk gelabeld met methylgroepen, waardoor hij relatief stil blijft. De onderzoekers ontdekten dat Vpr deze labels op specifieke plaatsen in dit gebied verwijdert, een proces dat demethylering wordt genoemd. Zodra die markeringen zijn verwijderd, wordt de antisensepromoter actiever en stuurt hij extra productie van alpha-synucleïne aan, wat de voedingsbodem vormt voor schadelijke aggregatie.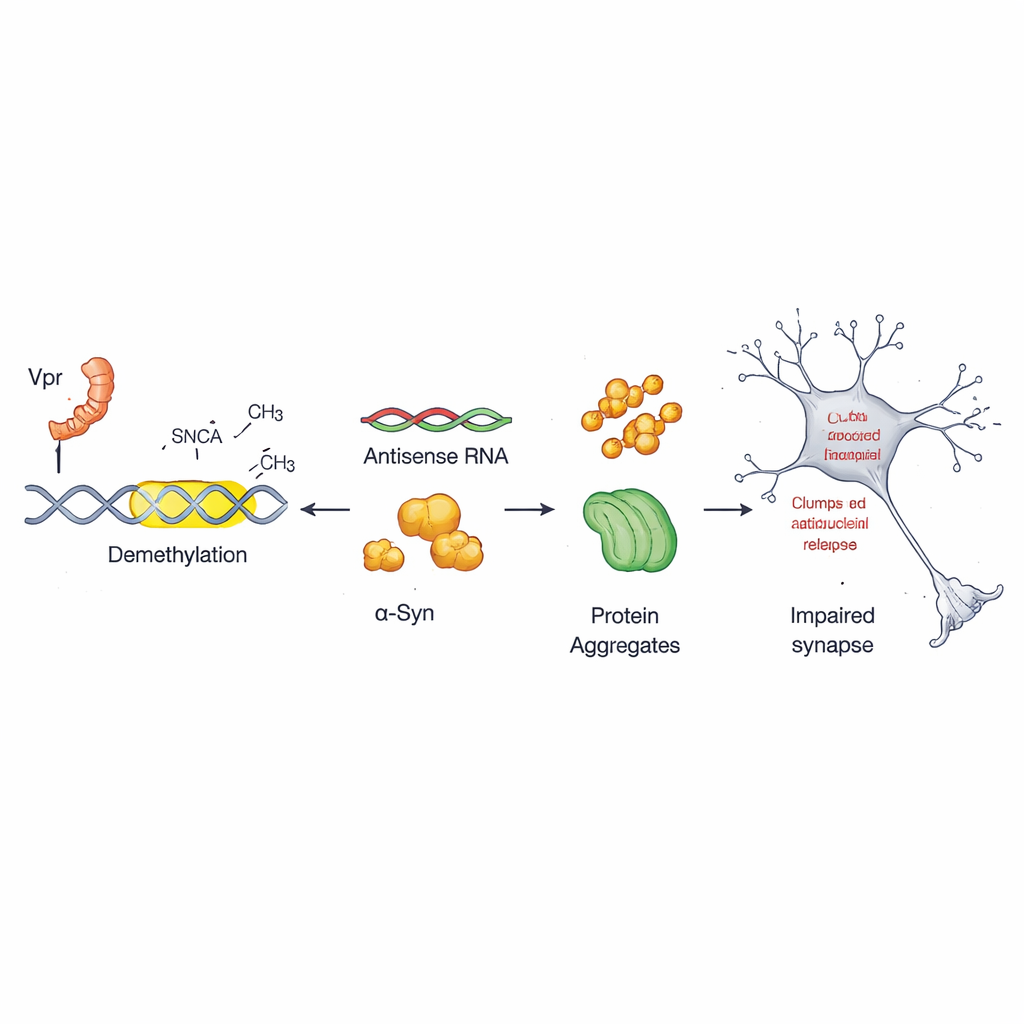
Bewijs uit cellen, muizen en menselijke hersenen
Met gekweekte menselijke zenuwachtige cellen en primaire muisneuronen toonden de auteurs aan dat toevoeging van Vpr in de loop der tijd de boodschapper-RNA- en eiwitniveaus van alpha-synucleïne verhoogt. Een medicijn dat algemeen DNA-demethylering bevordert, imiteerde sommige van deze effecten, wat de rol van epigenetische controle onderstreepte. Daarentegen voorkwam een verbinding genaamd DMOG, die demethylerende enzymen blokkeert, dat Vpr de antisensepromoter volledig activeerde. Het team keek vervolgens naar menselijke hersenmonsters van mensen met en zonder HIV. Hersenweefsel van HIV-positieve donoren—zowel vóór als na antiretrovirale behandeling—had minder methylmerken op hetzelfde DNA-gebied en hogere niveaus van alpha-synucleïne en zijn antisense-transcript, vooral bij donoren met HIV-gerelateerde dementie. Dit suggereert dat het virus een duurzame epigenetische litteken in de hersenen achterlaat.
Van moleculaire veranderingen naar geheugenproblemen
Om deze moleculaire verschuivingen aan gedrag te koppelen, onderzochten de onderzoekers hoe Vpr hersencircuits bij muizen beïnvloedt. Wanneer zij Vpr aan plakjes van de muishippocampus toedienden, een regio die essentieel is voor geheugen, bleef de basale signaalsterkte tussen neuronen onveranderd, maar nam het vermogen om verbindingen te versterken—een proces dat long-term potentiation wordt genoemd—af. Bij levende muizen leidden gerichte injecties van Vpr in de hippocampus tot slechtere prestaties bij een ruimtelijke geheugentaak waarin dieren de locatie van objecten moeten onthouden. Samen suggereren deze experimenten dat door Vpr aangedreven veranderingen in alpha-synucleïne niet louter biochemische eigenaardigheden zijn; ze vertalen zich in verzwakte synapsen en meetbare geheugendeficieten.
Wat dit betekent voor mensen die met HIV leven
Deze studie stelt een duidelijk keten van gebeurtenissen voor: HIV produceert Vpr, Vpr herprogrammeert een belangrijke DNA-schakelaar die alpha-synucleïne reguleert, het eiwit hoopt zich op en klontert, en neuronen verliezen geleidelijk hun vermogen om te communiceren en geheugen te ondersteunen. Omdat vergelijkbare alpha-synucleïneproblemen ten grondslag liggen aan de ziekte van Parkinson, suggereert het werk dat HIV en klassieke neurodegeneratieve ziekten overlappende mechanismen delen. Belangrijker nog, de bevindingen wijzen op mogelijke nieuwe strategieën—zoals geneesmiddelen die DNA-methylering bij de antisensepromoter stabiliseren of het oplopen van alpha-synucleïne beperken—om HIV-gerelateerde cognitieve achteruitgang en bewegingsproblemen te vertragen of te voorkomen.
Bronvermelding: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
Trefwoorden: HIV-geassocieerde neurocognitieve stoornissen, alpha-synucleïne, epigenetica, DNA-methylering, Parkinson-achtige symptomen