Clear Sky Science · nl
In silico ontwerp van een multiepitoopvaccin gericht op DENV-1 en DENV-3
Waarom denguevaccins nog steeds belangrijk zijn
Denguekoorts is niet langer een zeldzame tropische aandoening; het bedreigt nu miljarden mensen in meer dan 100 landen en loopt in delen van Azië, Latijns-Amerika en daarbuiten regelmatig ziekenhuizen vol. Zelfs met twee goedgekeurde vaccins op de markt is de bescherming ongelijk verdeeld, vooral bij mensen die nog nooit dengue hebben gehad en in regio’s waar meerdere virustypen tegelijk circuleren. Deze studie stelt een actueel vraagstuk: kan computergeleide ontwerp ons helpen een veiliger, preciezer vaccin te ontwikkelen, specifiek gericht op gevaarlijke co-infecties met twee dengue-typen die vaak samen voorkomen?
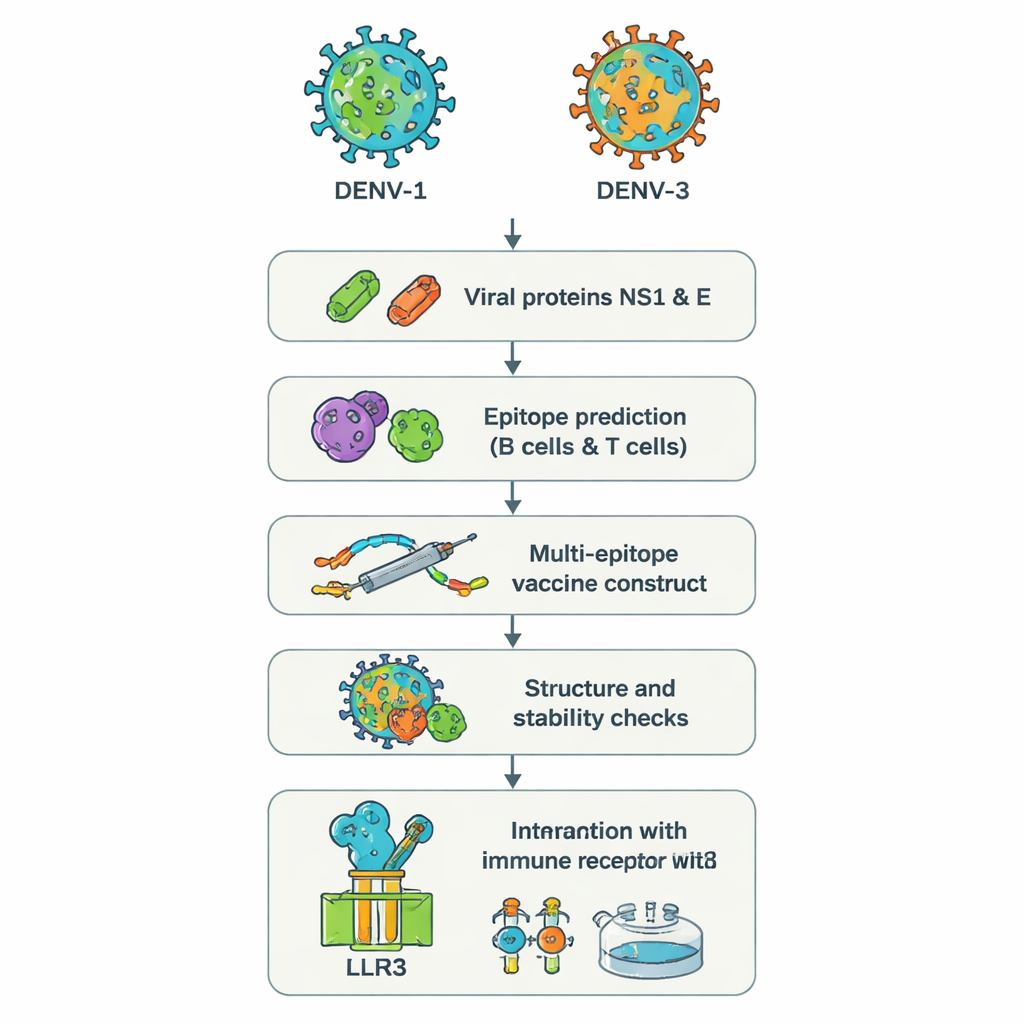
Twee slinkse virustypen en waarom ze een probleem vormen
Denguevirus komt in vier varianten, serotypen genoemd DENV‑1 tot en met DENV‑4. Infectie met een van deze serotypen kan hoge koorts, hevige pijn en in sommige gevallen levensbedreigend bloedverlies of shock veroorzaken. Verontrustend is dat een tweede ziekte episode met een andere serotype de aandoening soms kan verergeren in plaats van verbeteren, omdat bestaande antilichamen het nieuwe virus mogelijk makkelijker de cellen laten binnendringen — een proces dat antibody-dependent enhancement wordt genoemd. Bij recente uitbraken meldde men patiënten die gelijktijdig met DENV‑1 en DENV‑3 waren geïnfecteerd, een combinatie die geassocieerd is met ernstiger ziektebeelden en verwarrende testresultaten. Huidige vaccins bieden niet betrouwbaar bescherming voor alle leeftijdsgroepen en alle serotypen, vooral niet bij mensen zonder eerdere blootstelling, waardoor een gevaarlijke leemte in de verdediging blijft bestaan.
Een vaccin ontwerpen vanaf de molecuulgrenzen
In plaats van volledige virussen in het laboratorium te kweken, gebruikten de onderzoekers een aanpak die soms “reverse vaccinology” wordt genoemd. Ze startten vanuit de genetische sequenties van twee dengue-eiwitten, NS1 en E, van DENV‑1 en DENV‑3. Deze eiwitten zijn cruciaal voor hoe het virus cellen binnendringt en hoe het immuunsysteem het waarneemt. Krachtige webgebaseerde tools scanden de eiwitsequenties om korte fragmenten — epitopen — te vinden die waarschijnlijk door menselijke B-cellen (antilichaamproducerende cellen) en T-cellen (cellen die geïnfecteerde cellen doden en reacties coördineren) herkend worden. Uit honderden kandidaten selecteerde het team een kleine set die naar verwachting goed zichtbaar zijn voor het immuunsysteem, gedeeld worden door de twee serotypen en in staat zijn nuttige antivirale signalen zoals interferon-gamma op te wekken.
Het bouwen van één multifunctioneel vaccinmolecuul
De gekozen epitopen werden vervolgens digitaal aaneengeregen tot één lang kunstmatig eiwit, een “multiepitoop” vaccin. Korte aminozuurbruggen fungeren als flexibele tussenstukken zodat elk epitoop zijn structuur behoudt en toegankelijk blijft voor immuuncellen. Een extra fragment, gebaseerd op een natuurlijk humaan antimicrobieel peptide genaamd bèta-defensine, werd toegevoegd als adjuvans om de algemene respons te versterken. Computerapparatuur voorspelde dat het uiteindelijke construct, met 575 aminozuren, stabiel zou zijn, wateraantrekkend (en daardoor makkelijker oplosbaar) en onwaarschijnlijk als allergeen zou fungeren. Verdere structuurvoorspellende tools genereerden een driedimensionaal model en controleerden dat de meeste bouwstenen in realistische posities lagen, vergelijkbaar met die in bekende eiwitstructuren.
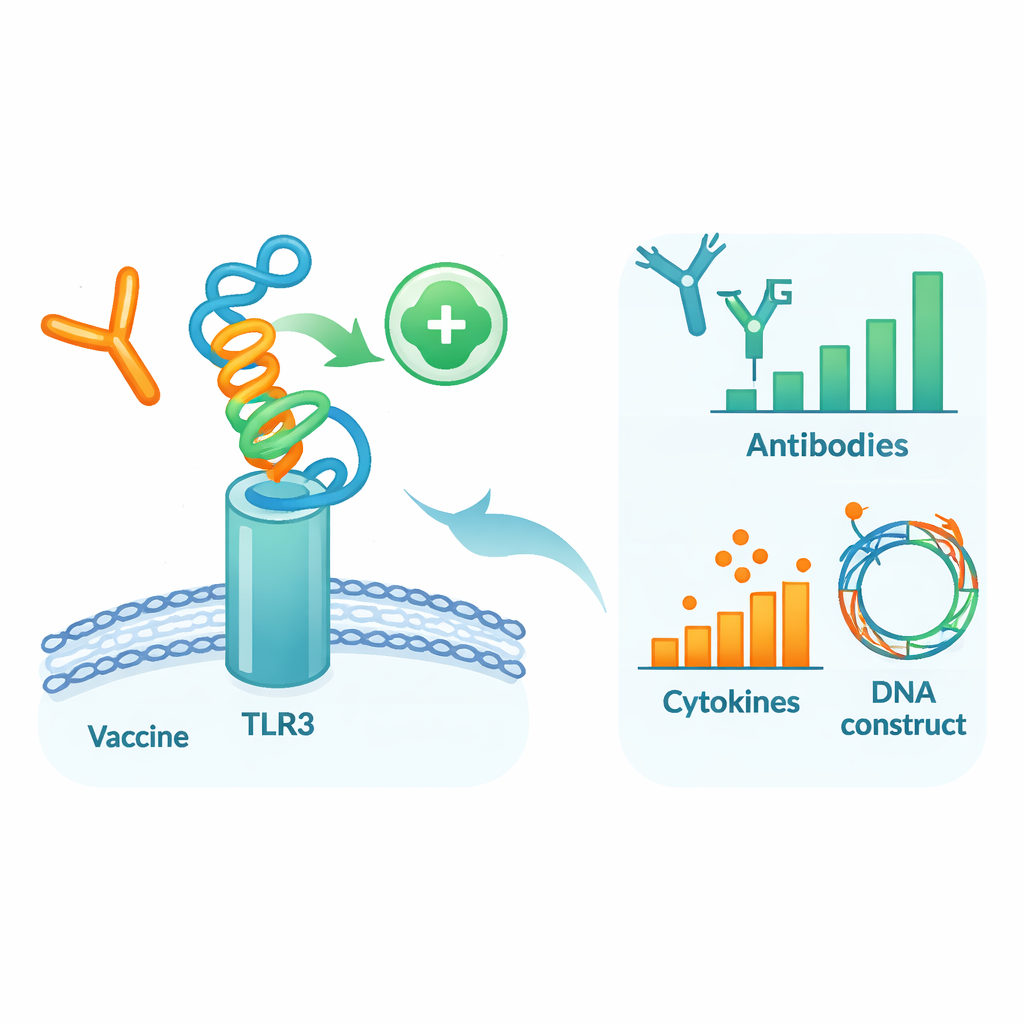
Het kandidaatvaccin testen in een virtueel lichaam
Om te onderzoeken hoe dit ontworpen eiwit zich in een mensachtige omgeving zou gedragen, voerden de auteurs een reeks gedetailleerde computersimulaties uit. Eerst plaatsten ze het vaccinmodel tegen TLR3, een sensor-eiwit op immuuncellen dat viraal materiaal detecteert en helpt bij het starten van vroege verdedigingen. Moleculaire dynamicasimulaties — virtuele films van atomen in beweging — suggereerden dat het vaccin en TLR3 een stabiel complex vormen, ondersteund door gunstige bindingsenergieën en talrijke waterstofbruggen. Aanvullende analyses van beweging en energie wezen op specifieke regio’s van beide moleculen die als contact-“hotspots” fungeren. Daarna werd een immuunsysteem-simulator gebruikt om drie vaccinaties over enkele maanden na te bootsen. Het virtuele immuunsysteem produceerde sterke golven van beschermende IgG-antilichamen, langlevend B- en T-celgeheugen en signaalmoleculen die overeenkomen met een robuuste antivirale respons.
Van computermodel naar laboratoriumklare blauwdruk
Tot slot pasten de onderzoekers de genetische code van het vaccin aan voor efficiënte productie in gebruikelijke laboratoriummicroben en plaatsten ze deze geoptimaliseerde DNA-sequentie met succes in een standaard expressieplasmide, klaar voor toekomstige experimentele testen. In eenvoudige woorden levert hun werk een gedetailleerde blauwdruk voor een nieuw dengievaccin dat zorgvuldig gekozen fragmenten van DENV‑1 en DENV‑3 target, naar verwachting stabiel en veilig is, en beide takken van het immuunsysteem sterk zou activeren. Hoewel deze resultaten puur computationeel zijn en bevestigd moeten worden in cellen, dieren en uiteindelijk mensen, tonen ze hoe moderne bio-informatica snel op maat gemaakte vaccin-kandidaten kan genereren voor complexe problemen zoals dengue co‑infectie.
Bronvermelding: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Trefwoorden: denguevaccin, multiepitoop, DENV-1, DENV-3, immunoinformatica