Clear Sky Science · nl
Integratieve analyse van proteomica en metabolomica onthult stoornis in aminozuurmetabolisme in adriamycine‑resistente acute myeloïde leukemiecellen
Waarom sommige leukemiemedicijnen hun effect verliezen
Chemotherapie heeft de behandeling van acute myeloïde leukemie (AML), een snelgroeiende bloedkanker, ingrijpend veranderd. Toch zien veel patiënten hun ziekte terugkeren omdat de kankercellen leren te overleven onder de invloed van de middelen die hen zouden moeten doden. Deze studie stelt een eenvoudige maar cruciale vraag: wat verandert er in leukemiecellen wanneer ze resistent worden tegen adriamycine, een van de standaard chemotherapiemiddelen, en wijzen die veranderingen op nieuwe manieren om het medicijn weer werkzaam te maken?
Een kijkje in de cellen
Om dit te onderzoeken vergeleken de onderzoekers een veelgebruikte menselijke AML‑cellijn, HL60, met een zustercellijn die resistent was gemaakt tegen adriamycine (HL60/R). In plaats van telkens één gen of eiwit te bestuderen, gebruikten ze twee brede, elkaar aanvullende benaderingen. Proteomica mat duizenden verschillende eiwitten — de werkpaardmoleculen die de meeste taken in de cel uitvoeren. Metabolomica mat honderden kleine moleculen die deel uitmaken van de stofwisseling, waaronder vetten, suikers en aminozuren. Door deze ’omics’ lagen te combineren bouwde het team een gedetailleerd beeld van hoe resistente cellen verschillen van hun nog‑gevoelige tegenhangers.
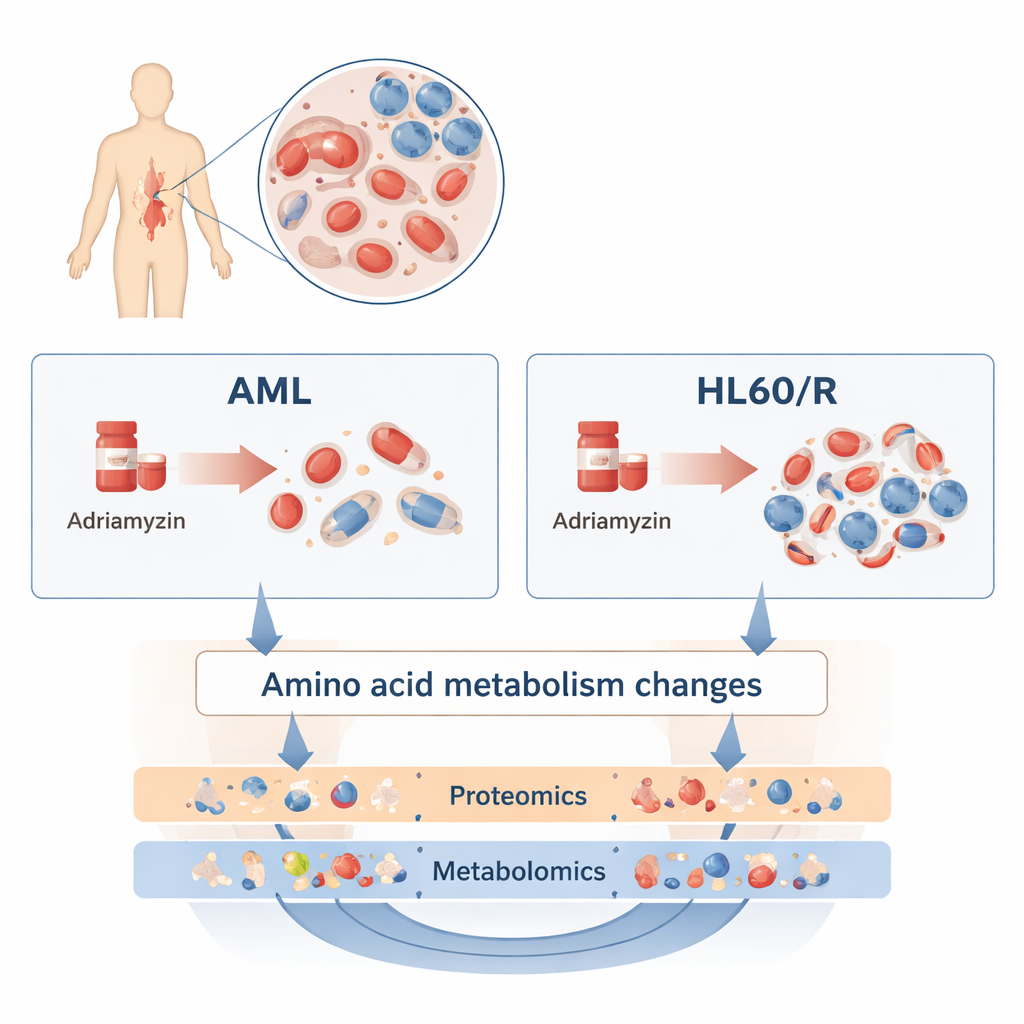
Grote herprogrammering van cellulair apparaat
De proteomica‑analyse toonde ingrijpende veranderingen: meer dan 3.200 eiwitten kwamen in hogere of lagere hoeveelheden voor in adriamycine‑resistente cellen vergeleken met normale HL60‑cellen. Veel van deze eiwitten clusteren in routes die bepalen hoe cellen energie gebruiken en op stress reageren. Met name eiwitten in het cAMP‑signaleringspad, het HIF‑1‑pad (dat cellen helpt omgaan met lage zuurstof) en oxidatieve fosforylering (een belangrijk energieproducerend proces in de mitochondriën) waren veranderd. Deze verschuivingen suggereren dat resistente leukemiecellen herprogrammeren hoe ze ademen, groeien en met elkaar signaleren om chemotherapie te weerstaan.
Metabolisme verschuift richting aminozuren
De metabolomica-aanpak vertelde een aanvullend verhaal. Van ongeveer 1.400 gedetecteerde metabolieten veranderden er 260 significant in de resistente cellen. Statistische modellen maakten een duidelijke scheiding tussen resistente en niet‑resistente cellen, wat wijst op een consistente metabole signatuur van resistentie. Wanneer de veranderde metabolieten werden geplaatst in bekende biochemische routes, vielen meerdere paden op. Veel van de sterkst getroffen routes waren gekoppeld aan aminozuren, de bouwstenen van eiwitten — vooral die met alanine, aspartaat, glutamaat, cysteïne, methionine en glutathion. Andere netwerken, zoals purine‑ en pyrimidinestofwisseling (belangrijk voor DNA en RNA) en de verwerking van bepaalde vetten, waren ook verstoord, wat benadrukt dat resistentie samenhangt met brede metabole herinrichting.
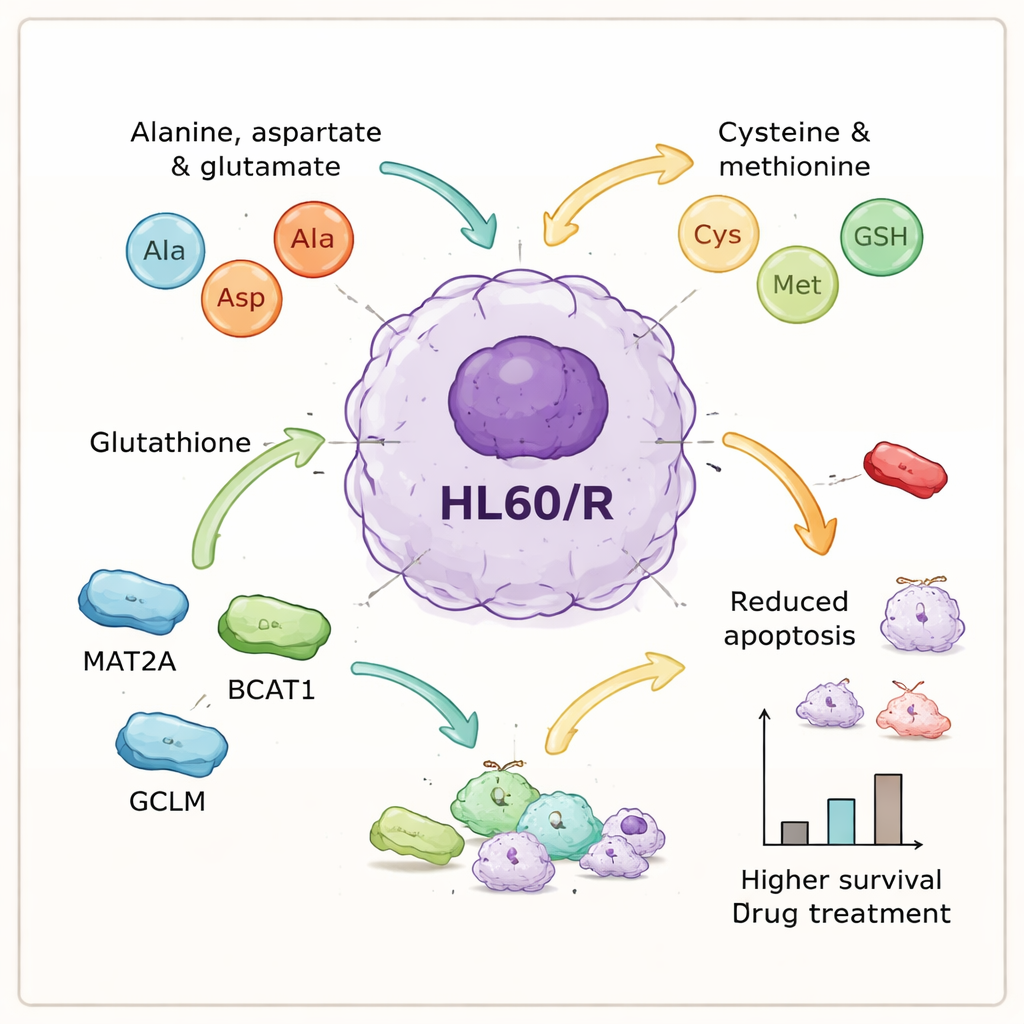
Belangrijke moleculaire spelers die kankercellen helpen volhouden
Door de eiwit‑ en metabolietdata te integreren, zoomden de auteurs in op een reeks aminozuurgerelateerde processen die centraal leken te staan bij resistentie. Ze selecteerden zes eiwitten die aan deze routes zijn gekoppeld — GOT1, GPX1, AHCY, MAT2A, BCAT1 en GCLM — voor nadere bestudering. Laboratoriumtesten bevestigden dat vijf van deze eiwitten meer aanwezig waren in resistente cellen, wat overeenkomt met het idee dat de verwerking van aminozuren is opgevoerd, terwijl één antioxiderend enzym, GPX1, afnam. Om oorzaak en gevolg te onderzoeken gebruikte het team kleine interfererende RNA’s om drie van de opgereguleerde eiwitten — MAT2A, BCAT1 en GCLM — in de resistente cellen af te remmen. Toen deze eiwitten werden gereduceerd, ondergingen de cellen na behandeling aanzienlijk meer geprogrammeerde celdood, wat betekent dat ze veel van hun verworven bescherming tegen adriamycine verloren.
Wat dit betekent voor toekomstige behandelingen
Gezamenlijk suggereren deze bevindingen dat adriamycine‑resistente AML‑cellen overleven niet alleen door afzonderlijke mutaties, maar doordat ze hun interne chemie herstructureren, met aminozuurmetabolisme als een centraal knooppunt. Door meer middelen te richten op specifieke aminozuur‑ en glutathionpaden lijken de cellen beter in staat stress te beheersen, schade te herstellen en te vermijden dat ze sterven bij blootstelling aan chemotherapie. Voor niet‑specialisten is de kernboodschap dat resistentie niet willekeurig is: ze volgt identificeerbare patronen die gemeten en mogelijk gericht kunnen worden. Op de lange termijn zouden middelen die specifieke eiwitten in de aminozuurverwerking, zoals MAT2A, BCAT1 of GCLM, remmen, gecombineerd kunnen worden met adriamycine of vergelijkbare middelen, waardoor clinici nieuwe opties krijgen om resistentie bij patiënten met acute myeloïde leukemie te voorkomen of te doorbreken.
Bronvermelding: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Trefwoorden: acute myeloïde leukemie, medicijnresistentie, adriamycine, aminozuurmetabolisme, multi‑omics