Clear Sky Science · nl
Een functioneel en robuust cellulair model voor high-throughput screening van Piezo1-modulatoren
Waarom kleine druksensoren in onze cellen ertoe doen
Elke keer dat bloed door onze vaten stroomt, of wanneer we gewoon door een kamer lopen, voelen onze cellen kleine mechanische krachten. Een belangrijk "druksensor"-eiwit genaamd Piezo1 helpt cellen deze krachten omzetten in elektrische en chemische signalen die weefsels gezond houden. Omdat Piezo1 betrokken is bij de groei van bloedvaten, botsterkte, immuunrespons en zeldzame genetische ziekten, zijn geneesmiddelontwikkelaars erop gebrand moleculen te vinden die de activiteit ervan kunnen bijsturen. Het hier beschreven artikel presenteert een nieuwe, snellere manier om naar zulke moleculen te zoeken met behulp van geïngineerde cellen en lichtgebaseerde aflezingen in plaats van trage, arbeidsintensieve technieken.
Het omzetten van aanraking naar een lichtsignaal
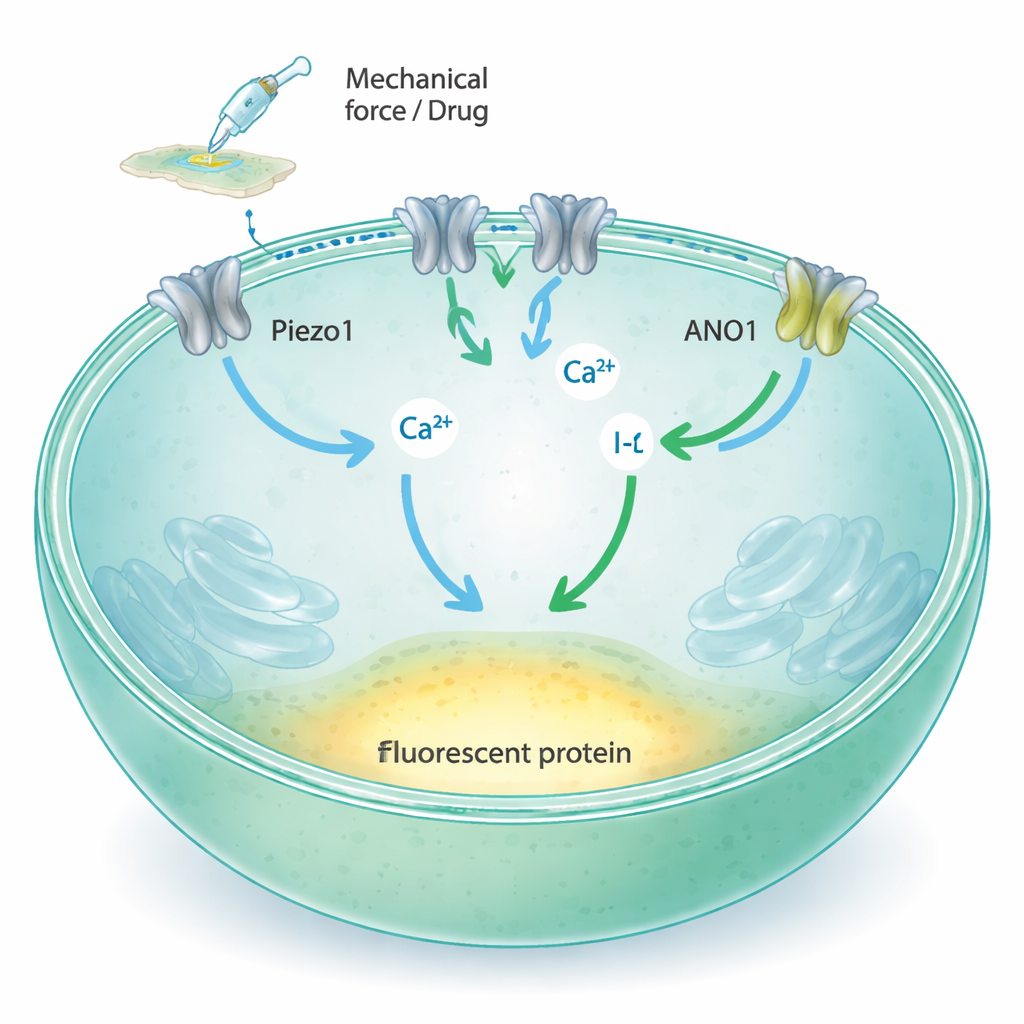
Piezo1 is een kanaal in het celmembraan dat opengaat wanneer het membraan wordt uitgerekt of ingedrukt, waardoor calcium en andere geladen deeltjes de cel kunnen binnendringen. Traditionele methoden om zulke kanalen te bestuderen vertrouwen op fijne glaspipetten of gespecialiseerde fluorescente rapporteurs, die krachtig maar moeilijk op te schalen zijn naar de tienduizenden testen die moderne geneesmiddelontdekking vereist. De auteurs wilden Piezo1-activiteit omzetten in een eenvoudige lichtverandering die een plate reader snel over veel monsters tegelijk kan meten. Hun idee was Piezo1 te koppelen aan twee extra componenten: ANO1, een ander ionkanaal dat op calcium reageert, en een gewijzigde gele fluorescente eiwitvariant die minder helder wordt bij blootstelling aan jodide-ionen.
Het bouwen van een responsieve testcel
De onderzoekers begonnen met Fischer Rat Thyroid (FRT)-cellen, die van nature Piezo1 produceren en goed hechten aan standaard plastic platen. Ze bevestigden dat deze cellen Piezo1 tot expressie brengen maar niet het nauwe verwante Piezo2, en toonden aan dat Piezo1 in deze cellen reageert op stroming en mechanische prikkeling door calcium toe te laten. Vervolgens introduceerden ze het ANO1-kanaal en het jodide‑gevoelige fluorescente eiwit (YFP‑H148Q/I152L) in de cellen. Wanneer het calciumniveau in de cel stijgt, gaat ANO1 open en laat jodide binnen; het fluorescente eiwit wordt dan minder helder naarmate jodide zich ophoopt. Microscopen, flowcytometrie en elektrische opnamen lieten zien dat zowel ANO1 als de fluorescente sensor in hoge mate aanwezig waren en werkten zoals bedoeld.
Van medicijneffect naar een meetbare gloed
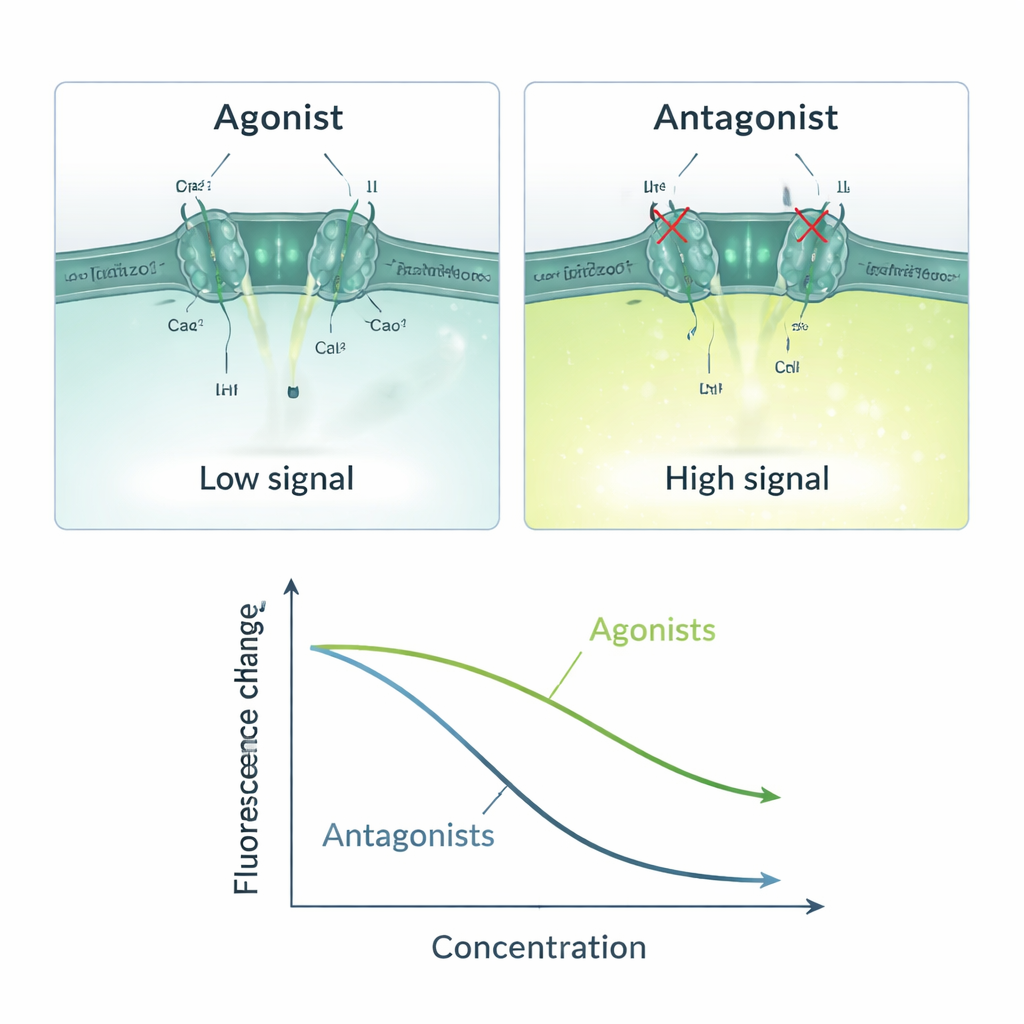
Met dit drieledige systeem creëerde het team een eenvoudige oorzaak‑en‑gevolgketen: als een testmolecuul Piezo1 activeert, stroomt er calcium binnen, ANO1 opent, jodide stroomt naar binnen en daalt het fluorescentiesignaal; als een molecuul Piezo1 blokkeert, blijft het signaal helder. Ze valideerden deze logica met bekende Piezo1-activatoren (Yoda1, Jedi1, Jedi2) en blokkers (Ruthenium Red, GsMTx4). Activatoren veroorzaakten dosisafhankelijke afnames in fluorescentie, met sensitiviteitswaarden die overeenkwamen met eerder gerapporteerde gegevens. Blokkers gaven het omgekeerde patroon en verminderden de respons naarmate hun concentratie toenam. De assay werkte alleen wanneer zowel calcium als jodide aanwezig waren, wat benadrukt dat het signaal daadwerkelijk afhankelijk was van Piezo1‑gedreven calciuminstroom en daaropvolgende ANO1‑gemedieerde jodide-influx. Statistische maten zoals de Z‑factor en signaal‑tegen‑ruisverhouding gaven aan dat de methode stabiel en betrouwbaar genoeg is voor industriële schaal screening.
Snel, schaalbaar testen met enkele kanttekeningen
Het nieuwe cellulaire model kan een enkele putmeting in ongeveer 14 seconden voltooien en een hele 96‑well plaat in ruwweg 22 minuten scannen, en het kan worden aangepast aan instrumenten die honderden wells gelijktijdig uitlezen. De gemodificeerde cellen blijven stabiel over vele generaties onder antibiotische selectie, wat herhaalde experimenten in de tijd mogelijk maakt. Omdat de aflezing optisch is en standaard microplaatapparatuur gebruikt, is de aanpak relatief goedkoop en toegankelijk. De auteurs merken echter op dat hun test indirect is: elk verbinding die inwerkt op stappen voor of na Piezo1 in de signaalketen — zoals ANO1 zelf of andere calciumhandelende eiwitten — kan een vals‑positief resultaat opleveren. Om die reden moeten hits uit dit screen nog worden bevestigd met meer directe methoden zoals elektrofysiologie.
Wat dit betekent voor toekomstige behandelingen
In alledaagse termen hebben de onderzoekers een laboratorium "rookmelder" gebouwd die minder fel gaat branden telkens wanneer een verbinding Piezo1 opent, en helder blijft wanneer Piezo1 wordt geblokkeerd. Deze alarmfunctie is gevoelig, snel en eenvoudig in groten getale uit te voeren, waardoor het uitstekend geschikt is voor de eerste selectie bij de zoektocht naar geneesmiddelen die de mechanische sensoren van het lichaam bijsturen. Hoewel het geen vervanging is voor meer gedetailleerde vervolgstesten, biedt dit cellulaire model een krachtig startpunt om moleculen te ontdekken die mogelijk op een dag kunnen helpen bij de behandeling van vaatstoornissen, botziekten, immuunproblemen en andere aandoeningen die verband houden met hoe onze cellen fysieke kracht voelen en erop reageren.
Bronvermelding: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
Trefwoorden: Piezo1-kanaal, mechanosensitieve ionkanalen, high-throughput screening, celgebaseerde assay, geneesmiddelontdekking