Clear Sky Science · nl
Synthese, karakterisering, DFT-analyse, moleculair docken en antikankeronderzoek bij colorectaal carcinoom van een nieuw pyrazool-hydrazone zink(II)-complex
Waarom een metaalgebaseerd geneesmiddel colonkanker mogelijk milder kan bestrijden
Veel krachtige kankermiddelen zijn opgebouwd rond zware metalen zoals platina. Ze kunnen effectief zijn maar gaan vaak gepaard met zware bijwerkingen en resistentie in de loop van de tijd. Deze studie onderzoekt een andere benadering: een nieuw kandidaat-geneesmiddel rond zink, een essentieel voedingsstof die al in ons lichaam voorkomt, gecombineerd met een organisch skelet genaamd pyrazool–hydrazone. De onderzoekers vroegen zich af of het koppelen van zink aan dit skelet een verbinding kan opleveren die colonkankercellen hard raakt maar gezonde cellen spaart.
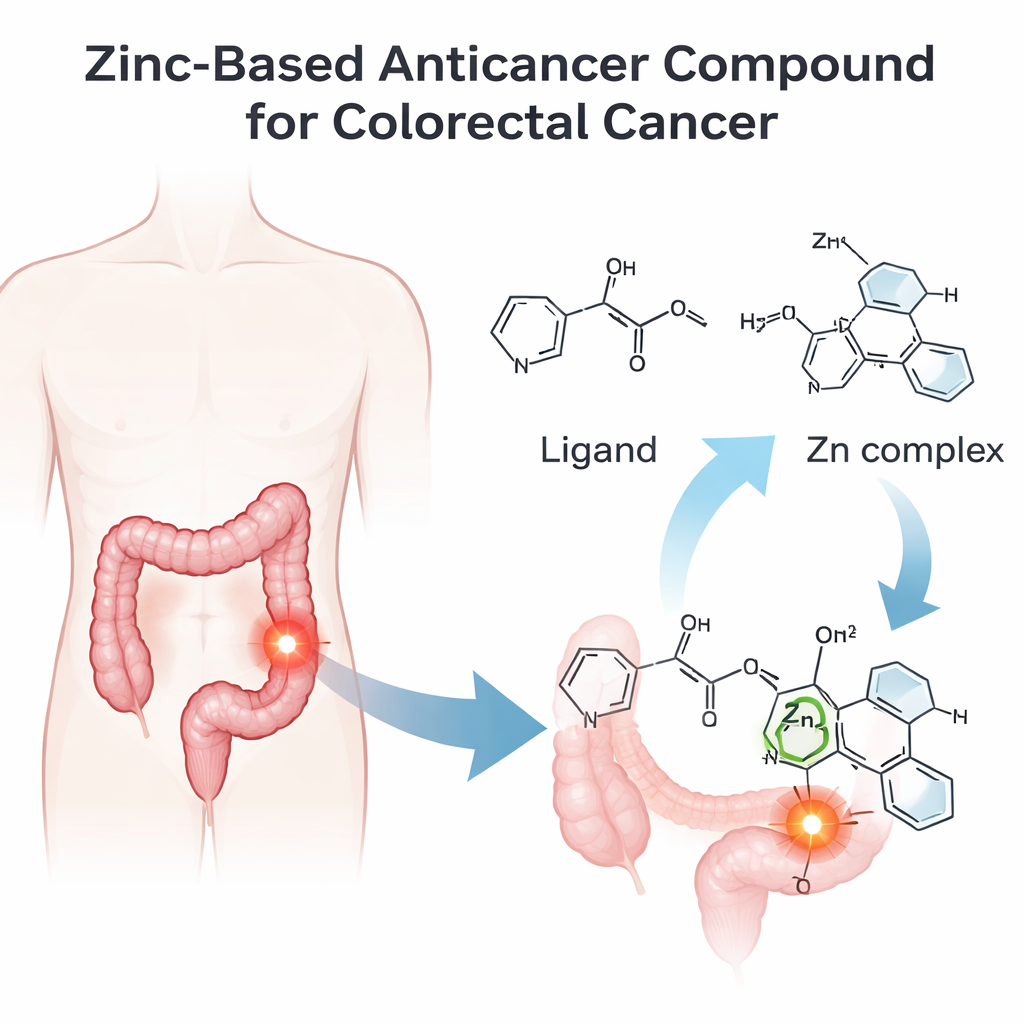
Het bouwen van een slimmer zinkmolecuul
Het team ontwierp en synthetiseerde eerst een nieuw organisch molecuul, aangeduid als IMP, en bond dit vervolgens aan een zinkion om een zinkcomplex te maken dat IMP-Zn wordt genoemd. Ze bevestigden de exacte structuur van beide met een reeks technieken die moleculen als het ware vingerafdrukken: infraroodspectroscopie om te zien welke chemische bindingen aanwezig zijn, kernspinresonantie om atoomposities in kaart te brengen, massaspectrometrie om het molecuulgewicht te verifiëren, en ultraviolet–zichtbaar-spectroscopie om te bestuderen hoe de verbindingen met licht interageren. Deze experimenten, samen met elektrische geleidbaarheidstesten, toonden aan dat zink sterk gecoördineerd is aan drie sleutelatomen in IMP en twee chloride-ionen, waardoor een enkel, goed gedefinieerd zinkgecentreerd complex ontstaat.
Inzoomen op het molecuul met virtuele chemie
Als aanvulling op de laboratoriummetingen voerden de onderzoekers gedetailleerde computersimulaties uit met behulp van dichtheidsfunctionaaltheorie (DFT). Deze berekeningen stelden hen in staat te voorspellen hoe elektronen binnen IMP en IMP-Zn verdeeld zijn, hoe stabiel elke vorm is en hoe gemakkelijk de moleculen aan chemische reacties zouden kunnen deelnemen. De resultaten toonden aan dat zodra zink is gebonden, de energiekloof tussen de zogenaamde grensorbitalen van het molecuul krimpt, wat betekent dat elektronen zich gemakkelijker binnen de structuur kunnen verplaatsen. Dit vertaalt zich meestal in een hogere chemische reactiviteit. Het zinkcomplex toonde ook een hogere zogenaamde elektrofiele-index, wat suggereert dat het beter uitgerust is om met biologische doelwitten te interageren dan de vrije ligand IMP op zichzelf.
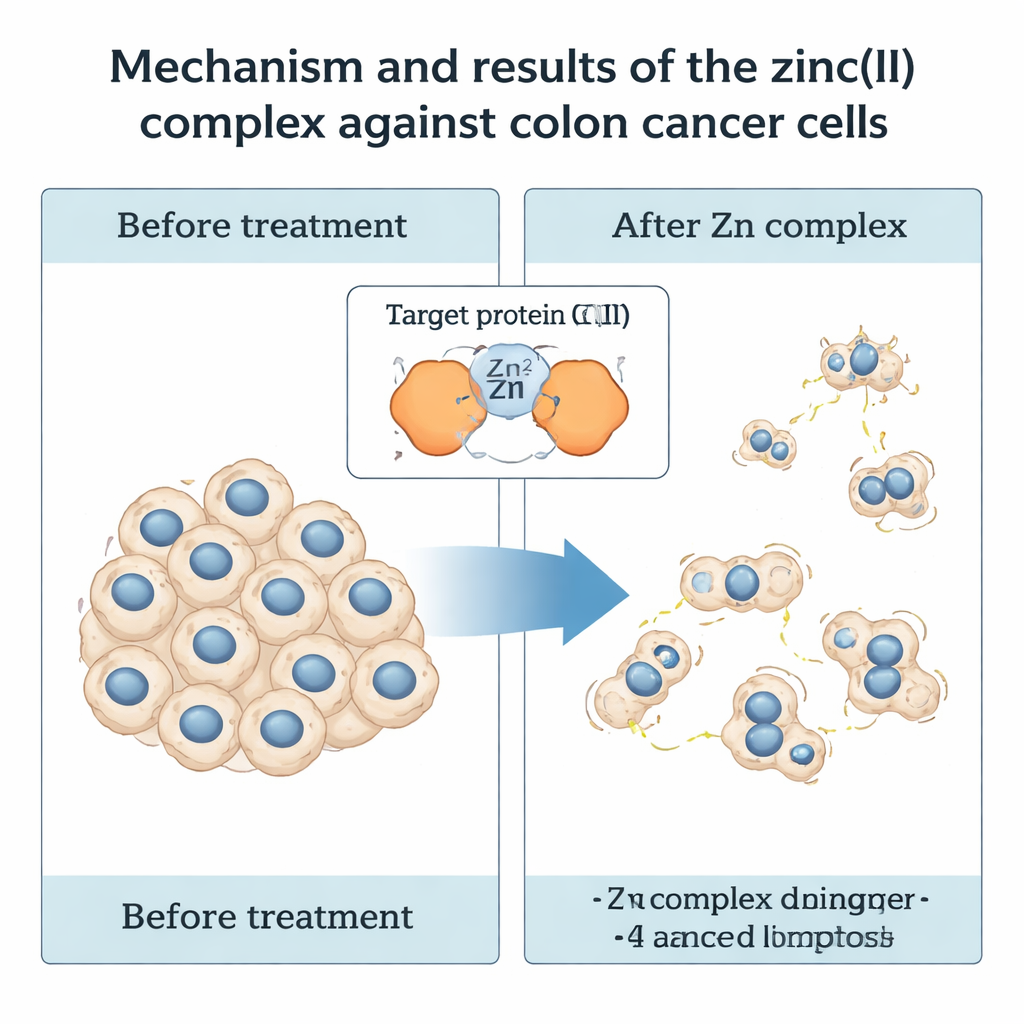
Hoe het zinkcomplex colonkankercellen aanpakt
De echte test was biologisch. De onderzoekers behandelden menselijke colorectale kankercellen (HCT116) met IMP en IMP-Zn in verschillende doseringen en tijden en maten vervolgens hoeveel cellen overleefden. Beide verbindingen vertraagden de groei van kankercellen, maar het zinkcomplex was duidelijk sterker: na 48 uur halveerde IMP-Zn de cellulaire levensvatbaarheid bij ongeveer 25 micromolair, terwijl de ligand alleen een veel hogere dosis nodig had. Even belangrijk was dat dezelfde concentraties IMP-Zn geen detecteerbaar toxisch effect hadden op een normale menselijke niercelijn (HEK293), wat wijst op een zekere mate van selectiviteit voor kankercellen. Toen het team de behandelde kankercellen twee weken volgde, ontdekten ze dat IMP-Zn zowel het aantal als de grootte van de kolonies die de cellen konden vormen scherp verminderde, wat aangeeft dat het hun vermogen tot langdurige proliferatie verstoort.
Indicaties dat de cellen naar geprogrammeerde celdood worden gedreven
Om te begrijpen hoe het zinkcomplex kankercellen schaadt, onderzochten de wetenschappers de celcyclus—de reeks stadia die cellen doorlopen als ze groeien en delen. Na blootstelling aan IMP-Zn verschuift een veel groter deel van de HCT116-cellen naar een “SubG0”-fase, een kenmerk van cellen met gefragmenteerd DNA. Dit patroon wordt vaak geassocieerd met apoptose, een gecontroleerde vorm van celdood die vaak het doel is van antikankermiddelen. Moleculair docken leverde een ander puzzelstuk: virtuele modellen suggereerden dat IMP-Zn sterker bindt dan IMP aan verschillende kankergelateerde eiwitten, waaronder een receptor-tyrosinekinase voor groeifactoren, een celcyclus-regulerende kinase en een geneesmiddel-metaboliserend enzym. Deze stevigere interacties ondersteunen het idee dat zinkcoördinatie helpt de verbinding vast te pakken aan cruciale cellulaire machinerie en zo het overleven van kankercellen verstoort.
Wat dit kan betekenen voor toekomstige behandelingen
Alles bij elkaar laat de studie zien dat het "versieren" van een pyrazool–hydrazone raamwerk met zink meer doet dan alleen de chemie bijstellen: het verandert IMP in een reactiever, krachtiger en schijnbaar selectiever middel tegen colorectale kankercellen. Hoewel IMP-Zn nog ver verwijderd is van een afgewerkt geneesmiddel—het moet nog worden getest in dieren of mensen—maakt het vermogen om de groei van colonkankercellen aanzienlijk te vertragen, cellen richting apoptose te duwen en normale cellen te sparen het tot een veelbelovend lid van een groeiende klasse zink-gebaseerde metallodrugs. Dit werk suggereert dat zorgvuldig ontworpen zinkcomplexen in de toekomst zachtere, gerichte alternatieven of aanvullingen op traditionele metaalgebaseerde chemotherapie kunnen bieden.
Bronvermelding: Mermer, A., Bayrak, A.M., Bolat, Z.B. et al. Synthesis, characterization, DFT analysis, molecular docking and anticancer investigations in colorectal carcinoma of a novel pyrazole-hydrazone zinc(II) complex. Sci Rep 16, 6391 (2026). https://doi.org/10.1038/s41598-026-35664-6
Trefwoorden: zink-gebaseerde antikankermiddelen, kolorectale kanker, pyrazool-hydrazone complex, moleculair docken, apoptose