Clear Sky Science · nl
Radiosensitiserende effecten van zilvernanodeeltjes die angiogenese en matrixmetalloproteinase‑signalering richten in triple-negatieve borstkankercellijnen
Moeilijke borsttumoren kwetsbaarder maken
Triple-negatieve borstkanker is een van de lastigste vormen van borstkanker om te behandelen. Ze groeit vaak snel, zaait vroeg uit en mist de gebruikelijke moleculaire “handvatten” waarop veel moderne medicijnen zich richten. Radiotherapie maakt vaak deel uit van de behandeling, maar deze tumoren kunnen hardnekkig resistent zijn. Deze studie stelt een eenvoudige, intrigerende vraag: kunnen heel kleine zilverdeeltjes de werking van bestraling verbeteren en tegelijkertijd het vermogen van de tumor om nieuwe bloedvaten te vormen en uit te zaaien vertragen?
Kleine zilverhulpen voor bestraling
De onderzoekers richtten zich op zilvernanodeeltjes—ultrakleine bolletjes zilver van nanometerformaat. Omdat zilver dicht is en sterk met röntgenstraling interacteert, kunnen deze deeltjes de effecten van bestraling concentreren op de plekken waar ze zich ophopen. Het team werkte met twee veelgebruikte laboratoriummodellen van triple-negatieve borstkanker en vergeleek die met een niet-kankercellijn uit de borst. Ze testten eerst hoe toxisch de zilvernanodeeltjes op zichzelf waren en vonden dat kankercellen bij veel lagere doses werden gedood dan normale cellen, wat wijst op een bruikbare therapeutische ruimte. Met wiskundige methoden om te analyseren hoe de deeltjes en bestraling samenwerken, lieten ze zien dat de combinatie een duidelijk sterker kanker-dodend effect gaf dan een van beide behandelingen afzonderlijk.
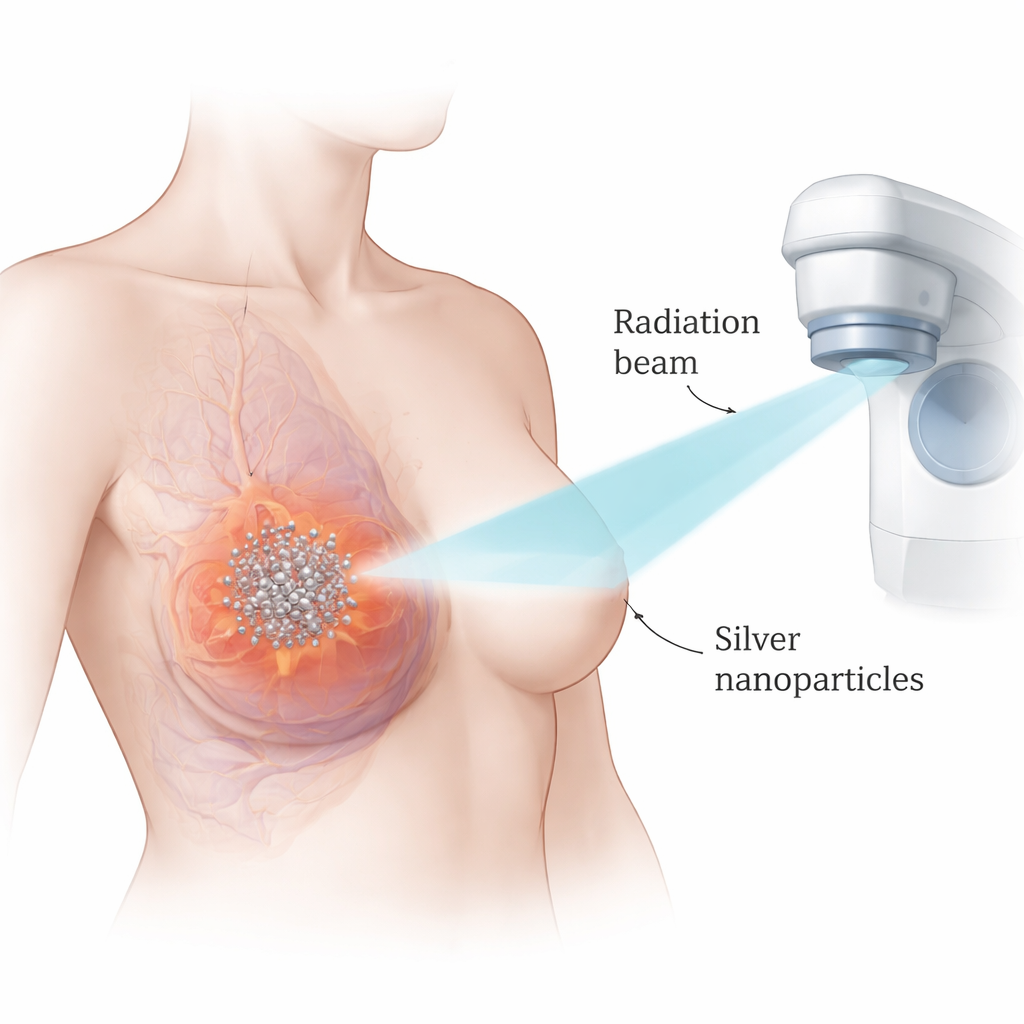
Het aanzetten tot zelfvernietiging van kankercellen
Vervolgens onderzochten de wetenschappers hoe de gecombineerde behandeling cellen deed sterven. Ze maten apoptose, een vorm van geprogrammeerde celdood, en volgden de ophoping van zeer reactieve moleculen, bekend als reactieve zuurstofspecies (ROS). Het is al bekend dat bestraling deels werkt door ROS te genereren die DNA beschadigen. In beide triple-negatieve borstkankercellijnen verhoogden de zilvernanodeeltjes op zichzelf apoptose en ROS-niveaus, en bestraling deed dat ook—maar de combinatie joeg beide meetwaarden dramatisch omhoog. Dat betekent dat meer kankercellen in een ordelijke zelfvernietigingsmodus werden geduwd, in plaats van te blijven hangen in een beschadigde toestand die soms herstel of resistentie kan bevorderen.
De bloedtoevoer afsnijden en uitzaaiing vertragen
Tumoren zijn afhankelijk van bloedvaten voor zuurstof en voedingsstoffen, en agressieve kankers kunnen zelfs bloedvatachtige structuren nabootsen. Het team keek naar twee belangrijke moleculaire schakelaars die betrokken zijn bij de aanleg en stabilisatie van tumorvaten, genoemd VEGFR2 en Tie2. In beide cellijnen verlaagden zilvernanodeeltjes de activiteit van deze genen, en de combinatie met bestraling schakelde ze nog verder uit. Ze onderzochten ook twee enzymen, MMP-2 en MMP-9, die kankercellen helpen het omringende weefsel af te breken en te migreren. In één van de cellmodellen verlaagden zowel bestraling als zilvernanodeeltjes deze enzymen, terwijl de gecombineerde behandeling het sterkste effect liet zien. Toen de wetenschappers observeerden hoe kankercellen naar een kunstmatige “schraap” in een kweekschotel toe bewogen, en toen ze testten hoe goed vaatachtige buisjes vormden in een co-cultuursysteem, vertraagde de combinatiebehandeling het meest duidelijk migratie en buisvorming.
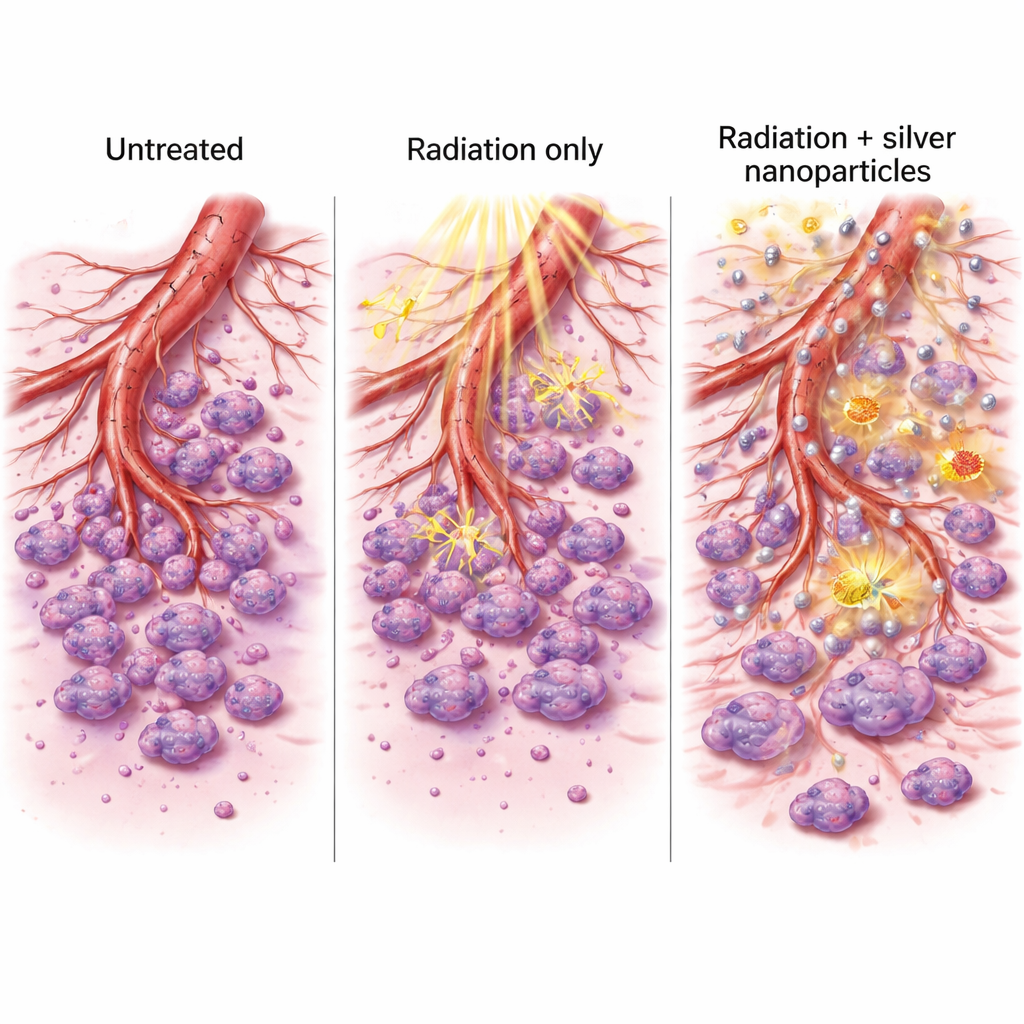
Waarom deze veranderingen ertoe doen
Door genen die nieuwe bloedvatgroei bevorderen en enzymen die cellen helpen invasie te plegen omlaag te schroeven, deed de zilver‑plus‑bestralingcombinatie meer dan alleen kankercellen doden. Ze verstoorde ook de ondersteunende systemen die tumoren gebruiken om uit te breiden en uit te zaaien. De behandelde cellen konden wonden in laboratoriumschotels minder goed sluiten en organiseerden zich minder goed in takachtige netwerken die op vroege bloedvaten lijken. Samen met de sterke toename in celdood en ROS-productie suggereren deze effecten een tweezijdig voordeel: een krachtiger directe aanval op de tumor en verzwakte middelen voor toekomstige groei en metastase.
Wat dit voor patiënten zou kunnen betekenen
Voorlopig zijn deze resultaten afkomstig van kankercellen die in het laboratorium gekweekt zijn, niet van patiënten. Toch schetsen ze een hoopgevend beeld. Zilvernanodeeltjes werkten als radiosensitizers en maakten standaard radiotherapie effectiever tegen cellen van triple-negatieve borstkanker. Tegelijk leken ze de mogelijkheid van de tumor om bloedvoorziening op te bouwen en omliggend weefsel binnen te dringen te verstikken. Als toekomstige dier- en klinische studies bevestigen dat deze deeltjes veilig en selectief naar tumoren kunnen worden afgeleverd, zouden ze artsen kunnen helpen lagere bestralingdosissen te gebruiken met betere resultaten, en zo een nieuwe manier bieden om een van de meest uitdagende vormen van borstkanker aan te pakken.
Bronvermelding: Montazersaheb, S., Farahzadi, R., Mansouri, E. et al. Radiosensitizing effects of silver nanoparticles targeting angiogenesis and matrix metalloproteinase signaling in triple negative breast cancer cell lines. Sci Rep 16, 6820 (2026). https://doi.org/10.1038/s41598-026-35662-8
Trefwoorden: triple-negatieve borstkanker, zilvernanodeeltjes, radiotherapie, angiogenese, metastase