Clear Sky Science · nl
Chemosensorische reactie op Pt-gebaseerde chemotherapeuten via bittere smaakreceptoren in vitro onthult een nieuw mechanisme voor bittere smaakaandoeningen
Waarom kankergeneesmiddelen plotseling alles slecht laten smaken
Patiënten met kanker melden vaak dat voedsel kort na het begin van de chemotherapie vreemd bitter of metaalachtig begint te smaken. Dit doet meer dan slechts maaltijden bederven: het kan de eetlust verminderen, gewichtsverlies bevorderen en de levenskwaliteit aantasten juist wanneer patiënten kracht nodig hebben. Deze studie stelt een schijnbaar simpele vraag met grote praktische gevolgen: hoe precies verstoren veelgebruikte op platina gebaseerde chemotherapeutica ons smaakgevoel, en kan dat effect veilig worden verminderd zonder de behandeling te verzwakken?
De verborgen rol van “bittere sensoren” in mond en darm
Onze tong en het spijsverteringskanaal zitten vol bitteresmaakreceptoren die ontworpen zijn om ons te waarschuwen voor mogelijk schadelijke stoffen. Deze sensoren, bekend als TAS2R's, zijn niet beperkt tot smaakpapillen; ze komen ook voor in cellen van de maag. De onderzoekers gebruikten een humane maagecellijn (HGT-1) die fungeert als een in vitro bitterheidsdetector: wanneer bittere receptoren worden geactiveerd, pompen de cellen meer protonen (zuur) uit, wat meetbaar is als een verandering in een aflezing die het intracellulaire protonenindex wordt genoemd. Door deze cellen bloot te stellen aan twee veelgebruikte platina-gebaseerde kankerdrugs — carboplatine en cisplatine — kon het team veilig onderzoeken hoe “bitter” deze middelen voor menselijke cellen lijken zonder ooit een persoon te vragen een giftige stof te proeven. 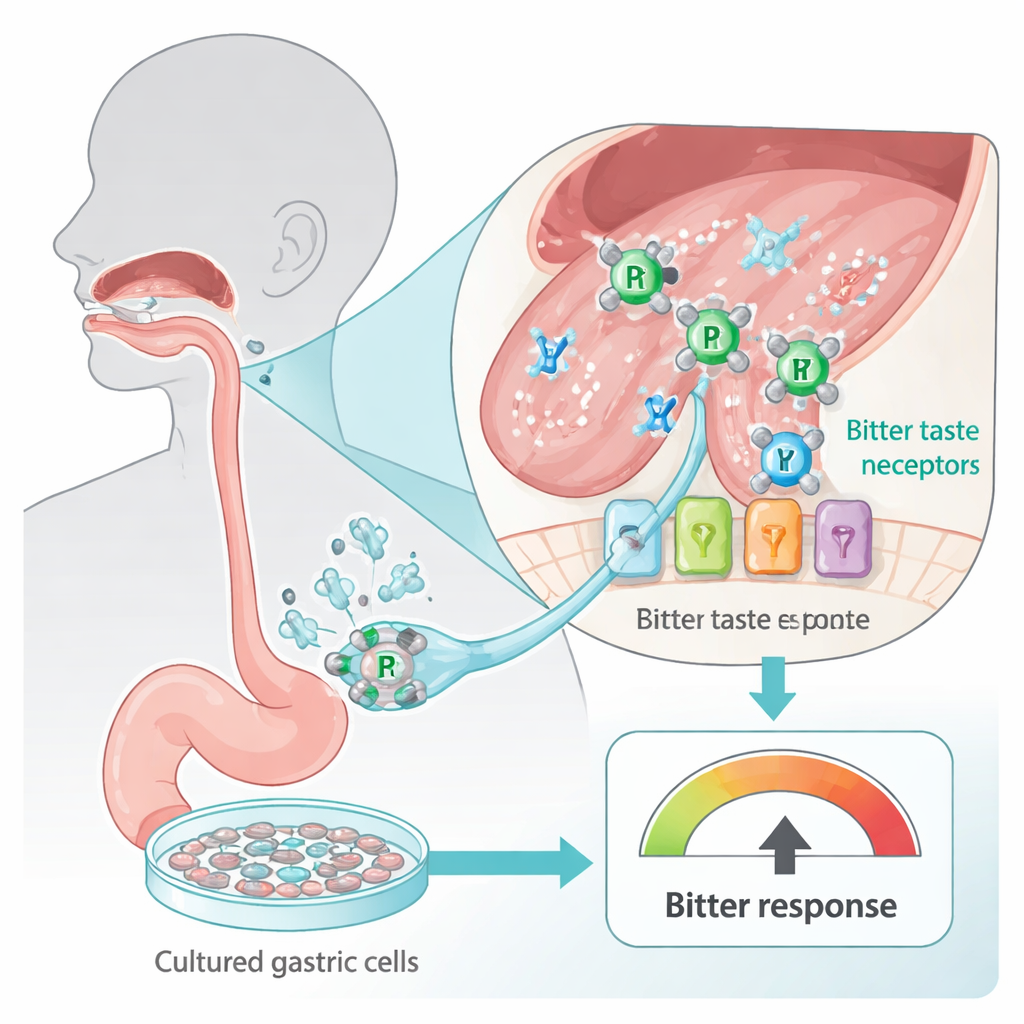
Chemotherapie-middelen die voor cellen bitter smaken
Wanneer de maagcellen werden behandeld met klinisch relevante concentraties carboplatine en cisplatine, veroorzaakten beide geneesmiddelen een duidelijke, dosisafhankelijke bitter-achtige reactie: hoe hoger de dosis, hoe sterker de cellulaire reactie. Cisplatine veroorzaakte echter een intensere reactie dan carboplatine wanneer rekening werd gehouden met hun gebruikelijke therapeutische doseringsverhouding (ongeveer 1:4), wat suggereert dat het mogelijk sterker bijdraagt aan bitterheidsproblemen bij patiënten. Op genetisch niveau veranderde blootstelling aan deze middelen de activiteit van meerdere genen voor bittere receptoren in de cellen, wat aangeeft dat plutonium? platina-geneesmiddelen niet op één enkele “bittere schakelaar” werken maar het bitterdetectiesysteem breed herschikken. Onder deze receptoren vielen TAS2R4 en TAS2R5 op als zowel zeer actief als sterk beïnvloed door de behandeling.
Het uitzetten van bittere signalen en het testen van een natuurlijke bitterblokker
Om vast te stellen welke receptoren het belangrijkst zijn, schakelde het team selectief specifieke bittere receptoren uit. Het uitzetten van TAS2R4 of het verminderen van TAS2R5 verminderde elk de bitter-achtige reactie op carboplatine en cisplatine, wat bevestigt dat deze receptoren helpen de geneesmiddelen te detecteren. De wetenschappers testten vervolgens een veelbelovende tegenmaatregel: het natriumzout van homoeriodictyol (Na-HED), een flavanon oorspronkelijk geïsoleerd uit de Noord-Amerikaanse plant Herba Santa en al bekend om het maskeren van bitterheid door andere verbindingen. Wanneer Na-HED gelijktijdig met de platina-middelen werd toegevoegd, dempte het de cellulaire bittere reactie aanzienlijk — met ongeveer driekwart voor zowel carboplatine als cisplatine — zonder de cellen op zichzelf te schaden. Dit laat zien dat Na-HED direct op bittere receptoren kan werken om het signaal dat door chemotherapiemiddelen wordt veroorzaakt te verminderen.
Waar bittere waarneming en medicijnopname elkaar kruisen
Naast het verklaren waarom platina-chemotherapie bitter kan smaken, onthult de studie een onverwachte wending: dezelfde bittere receptoren lijken ook te beïnvloeden hoeveel van deze middelen in cellen binnendringen. Met behulp van zeer gevoelige massaspectrometrie maten de onderzoekers de platinahoeveelheid binnenin cellen na behandeling. Cellen die bepaalde receptoren misten, zoals TAS2R4 of TAS2R43, stapelden meer platina op dan normale cellen, wat suggereert dat intacte receptoren helpen de cellulaire opname of retentie van deze toxische agentia te beperken. Na-HED veranderde de opname van carboplatine niet, maar verminderde wel hoeveel cisplatine de cellen binnendrong en toonde directe moleculaire interactie met cisplatine in oplossing. Dit suggereert dat een bittermaskerend middel in sommige gevallen ook kan moduleren hoe sterk een geneesmiddel lokale weefsels, zoals smaakcellen of speekselklieren, beïnvloedt. 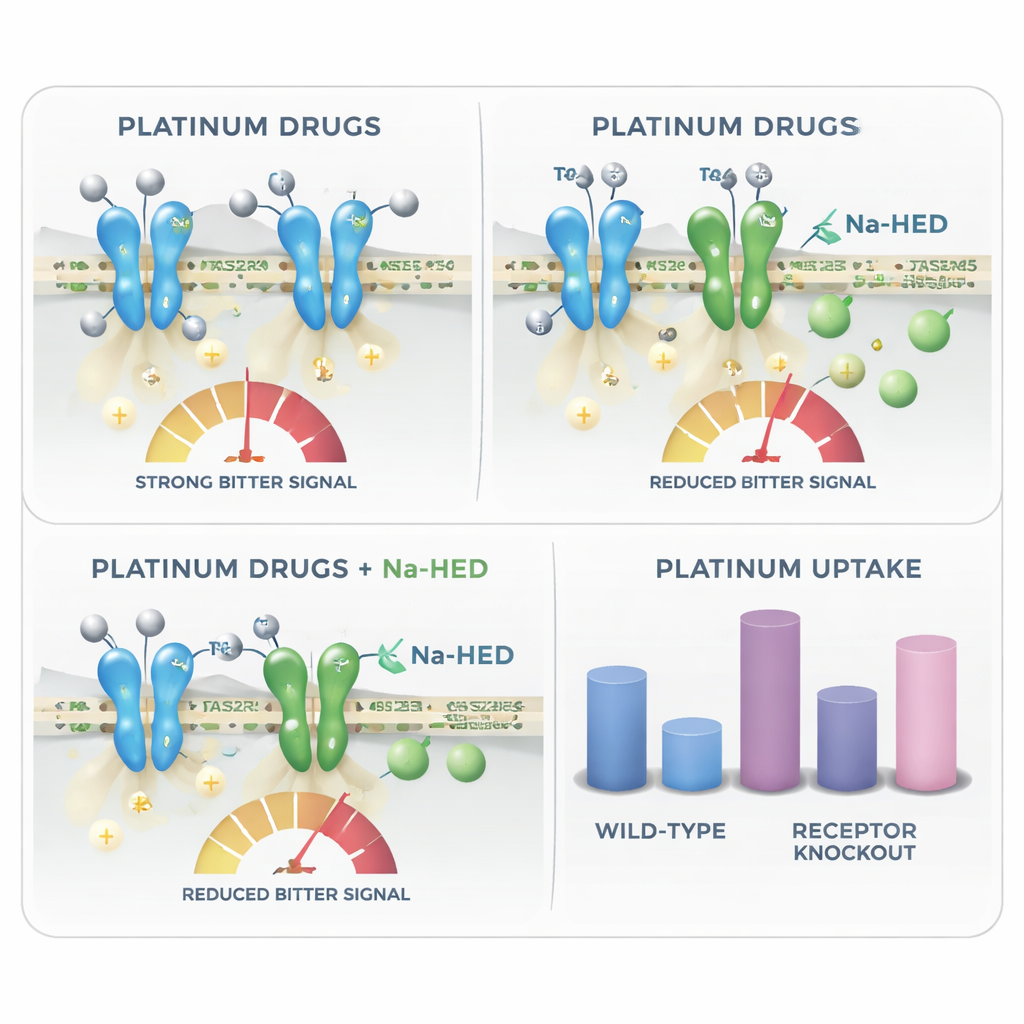
Op weg naar mildere smaaksensaties tijdens chemotherapie
Voor patiënten is de belangrijkste conclusie hoopvol: platina-gebaseerde chemotherapie lijkt bittere smaaksymptomen te veroorzaken door direct bittere receptoren te activeren die niet alleen op de tong maar ook in darmachtige cellen aanwezig zijn. Cisplatine blijkt daarbij bijzonder krachtig te zijn. De studie toont dat Na-HED dit bittere signaal in een gecontroleerd celsysteem aanzienlijk kan dempen en mogelijk ook de lokale opname van cisplatine kan beperken. Hoewel deze bevindingen bij mensen bevestigd moeten worden, wijzen ze op toekomstige “spoel-en-spuug” mondbehandelingen met Na-HED die harde bittere en metaalachtige sensaties kunnen verzachten zonder de kankebestrijdende werking van de middelen door het hele lichaam te verstoren.
Bronvermelding: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
Trefwoorden: veranderingen in smaak door chemotherapie, bittere smaakreceptoren, cisplatine en carboplatine, middelen tegen bitterheid, voeding van kankerpatiënten