Clear Sky Science · nl
Experimenteel onderzoek en thermodynamische correlatie van chlordiazepoxide-oplosbaarheid in superkritische CO₂
Waarom het oplossen van een bekend middel op een nieuwe manier ertoe doet
Veel moderne geneesmiddelen werken goed maar zijn moeilijk efficiënt te formuleren: ze lossen mogelijk niet gemakkelijk op, kunnen tijdens de productie degraderen of vereisen grote hoeveelheden organische oplosmiddelen. Deze studie bekijkt chlordiazepoxide, een al lang gebruikt anxiolyticum, en stelt een praktische vraag met brede gevolgen: hoe goed lost het op in superkritisch kooldioxide, een schoner, afstembaar oplosmiddel dat kan helpen veiliger en effectievere deeltjes van geneesmiddelen te maken?
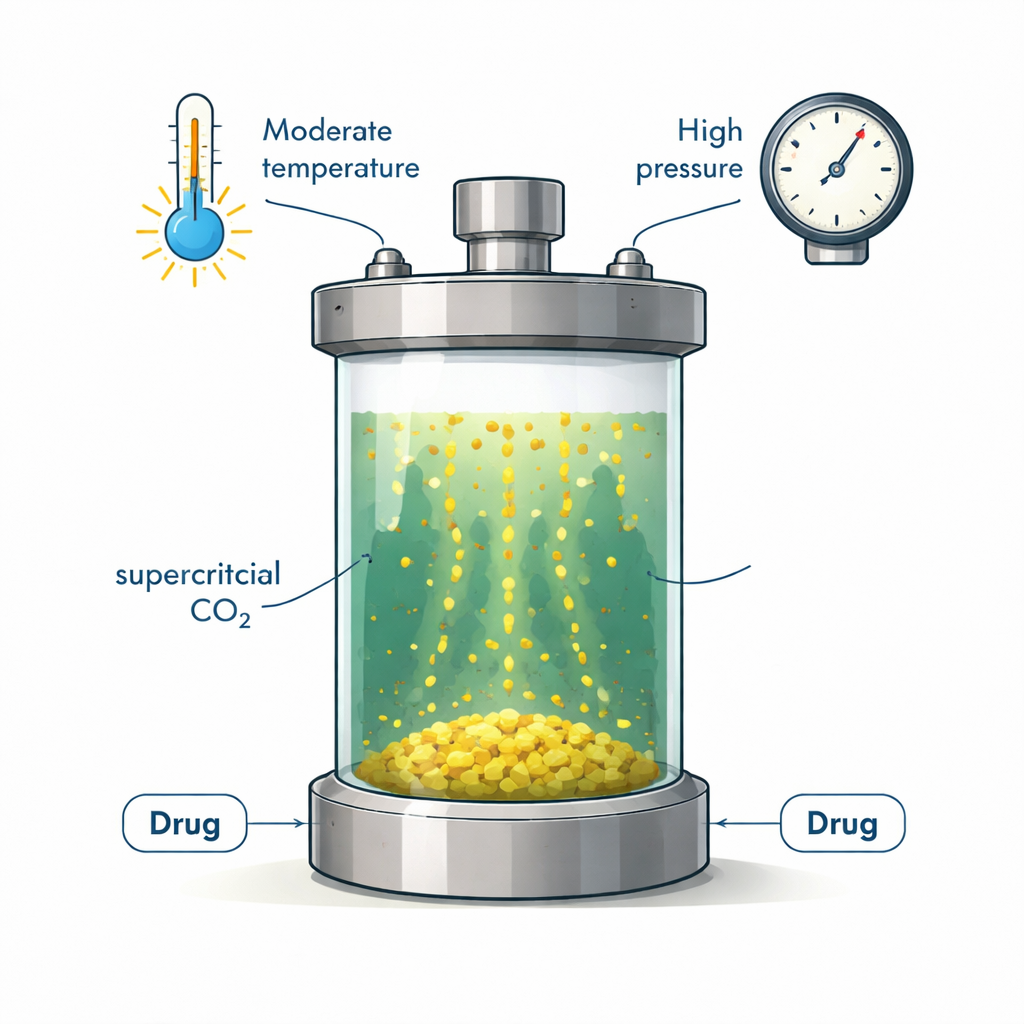
Een groene vloeistof die zich gedraagt als zowel gas als vloeistof
Superkritisch kooldioxide is kooldioxide die boven een bepaalde druk en temperatuur wordt gebracht totdat het noch een gewoon gas noch een normale vloeistof is. In deze toestand stroomt het als een gas maar heeft het een vloeistofachtige dichtheid die veel stoffen kan oplossen. De industrie gebruikt het al om koffie te decafeïniseren en aroma’s en oliën te extraheren. Voor de farmacie is superkritische CO₂ aantrekkelijk omdat het niet-toxisch is, door regelgevers is goedgekeurd, goedkoop en gemakkelijk te recyclen. Het kan helpen bij het creëren van kleine, uniforme deeltjes en de behoefte aan agressieve organische oplosmiddelen verminderen—als, en alleen als, het geneesmiddel er daadwerkelijk in voldoende mate in oplost.
Meten hoe een angstremmer zich onder druk gedraagt
De auteurs gingen na hoeveel chlordiazepoxide voor het eerst oplost in zuivere superkritische CO₂ binnen een praktisch verwerkbaar venster. Ze plaatsten vast poeder van het geneesmiddel in een hogedrukkamer en lieten CO₂ erdoor stromen bij drukken tussen 12 en 30 megapascal en temperaturen tussen 308 en 338 kelvin (ongeveer 35–65 °C). Nadat het systeem evenwicht had bereikt, namen ze een monster van de CO₂-fase, lieten die snel in een oplosmiddel expanderen en bepaalden met ultraviolet–zichtbare absorptie hoeveel geneesmiddel was opgelost. De totale oplosbaarheid liep ongeveer van 20 tot 576 delen per miljoen, overeenkomend met molfracties tussen 0,0198×10⁻³ en 0,576×10⁻³, waarden die in lijn liggen met veel andere matig oplosbare geneesmiddelen in superkritische CO₂.
Hoe druk en temperatuur de oplosbaarheid bepalen
De metingen toonden duidelijke, intuïtieve patronen. Bij een vaste temperatuur verhoogde een stijging van de druk de oplosbaarheid altijd. Hogere druk drukt CO₂-moleculen dichter bij elkaar, waardoor de superkritische fase dichter wordt en beter in staat is geneesmiddelmoleculen om te sluiten en mee te voeren. Temperatuur had een subtieler effect. Bij lagere drukken leidde verwarming doorgaans tot verminderde oplosbaarheid omdat het CO₂ uitdunt en zijn oplossend vermogen vermindert. Boven een kruisingdruk van ongeveer 19 megapascal keerde de trend om: hogere temperatuur verhoogde de oplosbaarheid omdat het de neiging van het geneesmiddel versterkte om uit de vaste fase in de vloeistof te ontsnappen. Dit evenwicht tussen de dichtheid van het fluïdum en de vluchtigheid van het geneesmiddel is kenmerkend voor superkritische systemen en belangrijk bij het kiezen van praktische bedrijfscondities.
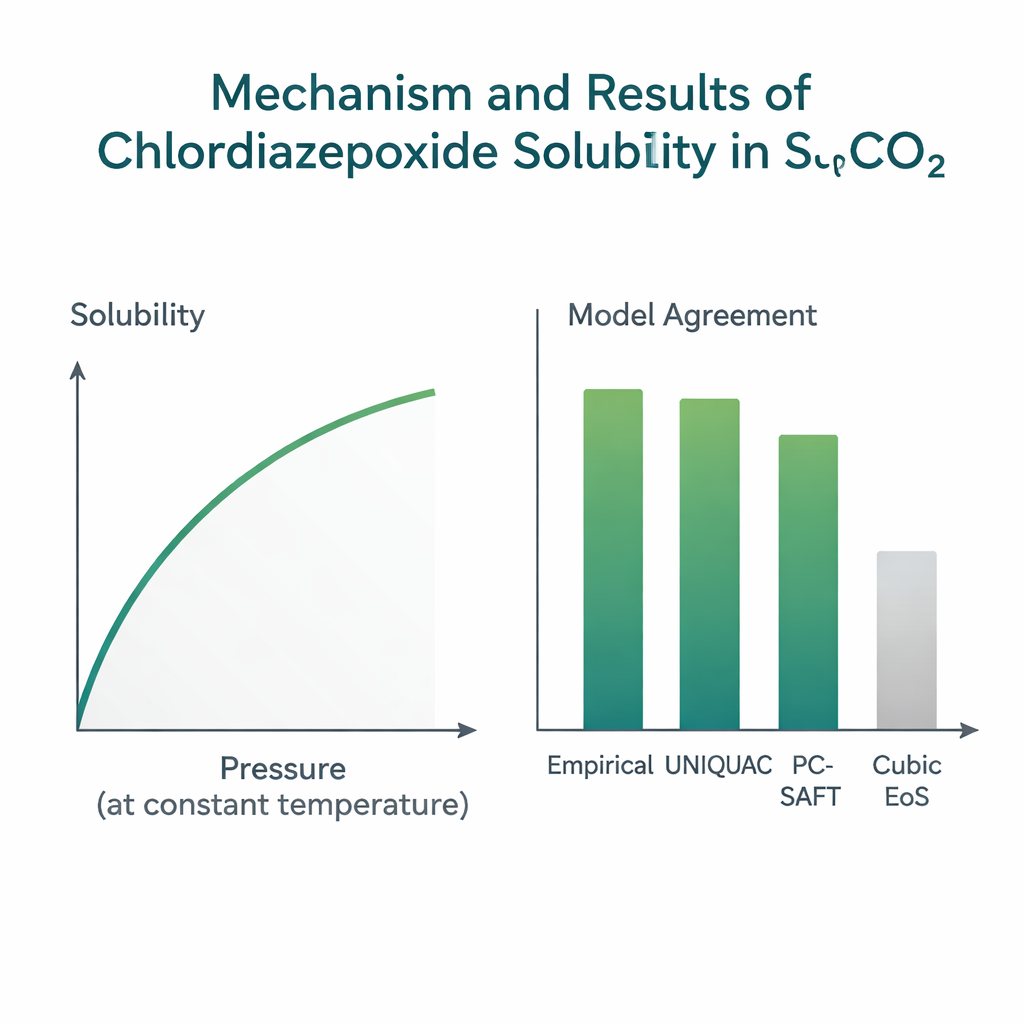
Modellen trainen om te voorspellen wat het lab ziet
Aangezien hogedrukexperimenten traag en kostbaar zijn, vertrouwen ingenieurs op wiskundige modellen om oplosbaarheid onder nieuwe condities of voor verwante geneesmiddelen te voorspellen. Het team testte verschillende modelgroepen met hun nieuwe dataset. Eenvoudige empirische formules "op basis van dichtheid", die oplosbaarheid direct koppelen aan CO₂-dichtheid en temperatuur met slechts enkele aanpassingsconstanten, presteerden het best. In het bijzonder kwam de lang gevestigde Chrastil-correlatie overeen met de data met een gemiddelde afwijking van ongeveer 5%, en andere vergelijkbare formules deden het ook goed. Een fysisch gedetailleerdere "expanded-liquid" benadering genaamd UNIQUAC, die rekening houdt met moleculaire grootte, vorm en interactie-energieën, behaalde vergelijkbare nauwkeurigheid, rond 6% afwijking. Daarentegen lieten algemeen gebruikte kubieke toestandsvergelijkingen—algemeen toepasbare formules voor fluïdumgedrag—afwijkingen rond 20% zien en misten ze fijne details van hoe dit specifieke geneesmiddel met CO₂ interageert.
Wat dit betekent voor toekomstige geneesmiddelenproductie
Simpel gezegd laat de studie zien dat chlordiazepoxide oplost in superkritische CO₂ onder technologisch relevante condities, en dat het gedrag zeer goed kan worden vastgelegd met relatief eenvoudige, goed gekozen modellen. Dit biedt een betrouwbaar kader voor het ontwerpen van groenere processen om nieuwe vaste vormen of nanodeeltjes van het geneesmiddel te maken, wat stabiliteit of opname in het lichaam kan verbeteren. In bredere zin levert het werk een zeldzame, zorgvuldig gemeten dataset voor een veelgebruikt medicijn en toont het welke modelleringshulpmiddelen het meest betrouwbaar zijn bij het plannen van processen met superkritische CO₂—informatie die schonere, efficiëntere productie van vele andere geneesmiddelen kan sturen.
Bronvermelding: Saadati Ardestani, N., Noubigh, A., Esfandiari, N. et al. Experimental investigation and thermodynamic correlation of chlordiazepoxide solubility in supercritical CO₂. Sci Rep 16, 6552 (2026). https://doi.org/10.1038/s41598-026-35623-1
Trefwoorden: superkritisch kooldioxide, oplosbaarheid van geneesmiddelen, chlordiazepoxide, groene farmaceutische verwerking, thermodynamische modellering