Clear Sky Science · nl
Trajectoire van de integriteit van stratum radiatum, lacunosum en moleculare in het continuüm van de ziekte van Alzheimer
Waarom dit ertoe doet voor geheugen en veroudering
Naarmate mensen langer leven, maken velen zich zorgen of normale vergeetachtigheid een vroeg teken van de ziekte van Alzheimer kan zijn. Artsen kunnen de hersenen scannen op krimp in geheugencentra, maar de huidige methoden missen vaak de allereerste veranderingen, juist wanneer behandeling en planning het meest kunnen helpen. Deze studie bekijkt een dunne, signaalvoerendelaag binnen het geheugencentrum van de hersenen — de hippocampus — om te bepalen of het uiterlijk daarvan op MRI Alzheimer mogelijk eerder kan onthullen en kan voorspellen wie sneller achteruit zal gaan.
Een nadere blik op het geheugencentrum van de hersenen
De hippocampus is een zeepaardvormige structuur diep in de hersenen die cruciaal is voor het vormen van nieuwe herinneringen. Binnenin bevindt zich een kwetsbare band van verbindingen die het stratum radiatum, lacunosum en moleculare (SRLM) wordt genoemd. Deze laag voert boodschappen naar een sleutelgebied van de hippocampus en is een van de eerste plaatsen die worden aangetast door de abnormale eiwitten die zich ophopen bij de ziekte van Alzheimer. Op bepaalde MRI-scans verschijnt het SRLM als een dunne donkere lijn. Eerder onderzoek suggereerde dat deze lijn vervaagt naarmate het weefsel beschadigd raakt, wat de mogelijkheid oproept dat de scherpte van deze lijn kan dienen als een eenvoudige visuele aanwijzing voor vroege ziekte.
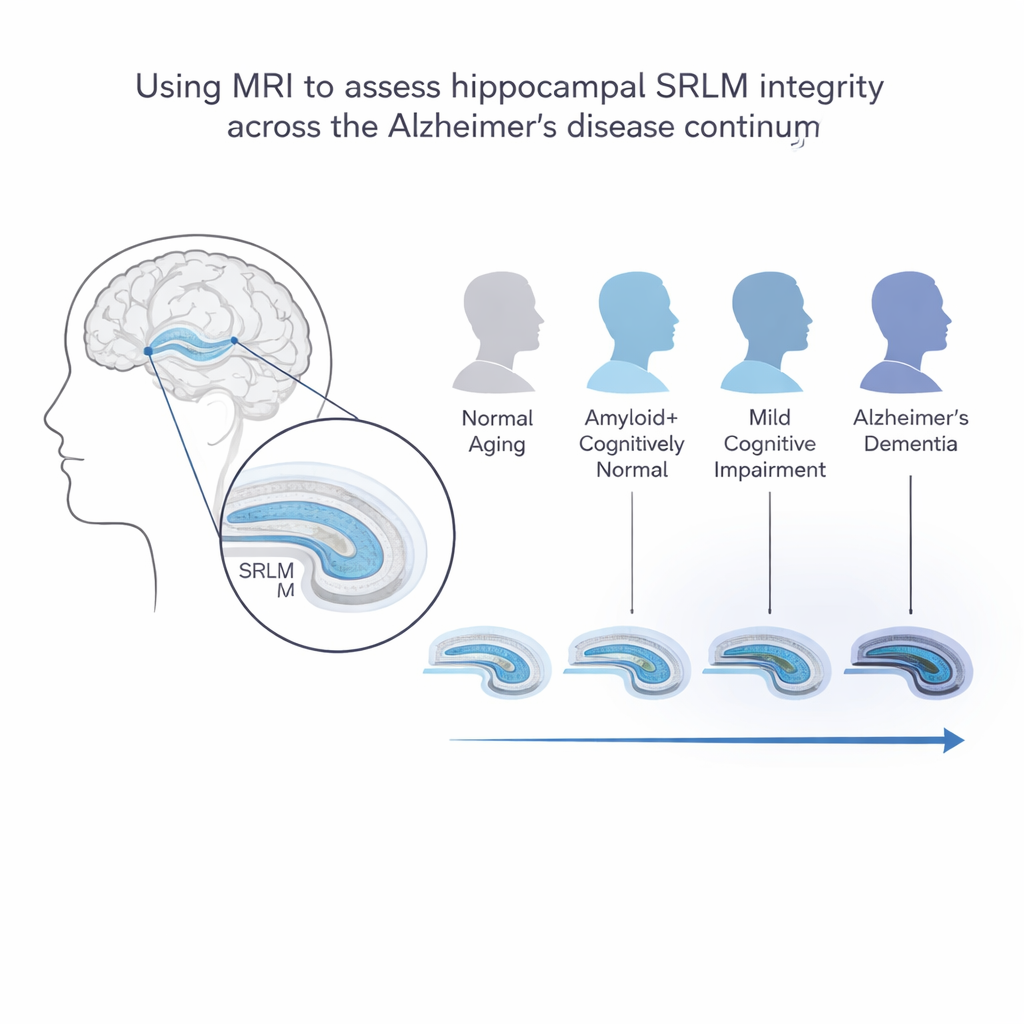
Mensen volgen langs het Alzheimer‑pad
Om dit idee te testen gebruikten de onderzoekers gegevens uit een grote Amerikaanse studie naar veroudering en dementie. Ze verdeelden 373 oudere volwassenen in vier stadia van het Alzheimer‑“continuüm” op basis van hersenscans op amyloïde, een van de kenmerkende eiwitten van de ziekte. De groepen waren: mensen met normaal denken en geen amyloïde, mensen met normaal denken maar wel amyloïde, mensen met milde geheugenproblemen plus amyloïde, en mensen met volle Alzheimer‑dementie plus amyloïde. Iedereen kreeg gedetailleerde MRI-scans, inclusief hoge-resolutiebeelden gericht op de hippocampus, en de meesten ondergingen vervolggeheugentests over ongeveer twee jaar.
Een vervagende lijn aflezen op MRI
Twee getrainde beoordelaars, die de diagnoses van de deelnemers niet kenden, beoordeelden het SRLM op de MRI van elke persoon met een vijfpuntsschaal: van een ontbrekende of nauwelijks zichtbare lijn tot een scherpe, doorlopende lijn. Ze beoordeelden ook de algemene hippocampuskrimp met een standaard visuele schaal en maten volumes van de hippocampus en aangrenzende structuren met geautomatiseerde software. Vergeleken met de gezonde, amyloïde‑negatieve groep lieten mensen die amyloïde‑positief waren maar nog normaal testten al significant lagere SRLM-scores zien. Daarentegen werden zichtbare hippocampuskrimp en volumeverlies vooral later gezien, bij degenen met milde cognitieve stoornis of dementie, wat suggereert dat veranderingen in het SRLM eerder verschijnen dan traditionele maten.
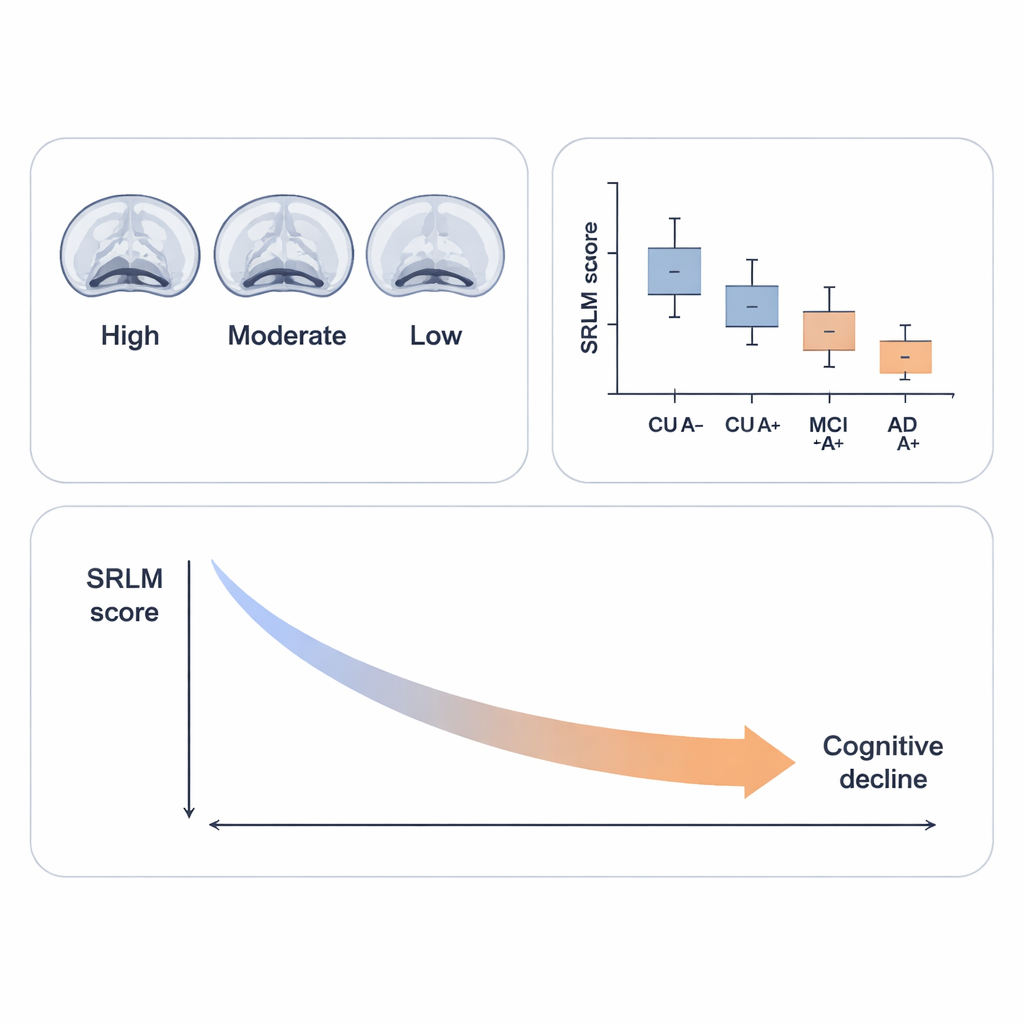
Hersenveranderingen koppelen aan denken en ziekte‑eiwitten
Over alle deelnemers waren lagere SRLM-scores, grotere hippocampuskrimp en kleinere hippocampusvolumes elk gekoppeld aan hogere niveaus van amyloïde en tau (een ander Alzheimer‑eiwit) en aan slechtere prestaties op tests voor geheugen, taal en denkvaardigheid. Onder mensen met amyloïde in de hersenen waren deze verbanden matig en consistent. Zelfs in de groep zonder amyloïde verschenen subtiele verbanden tussen SRLM-scores, tau‑niveaus en bepaalde denkvaardigheden. Belangrijk is dat, toen het team naar veranderingen in de tijd keek, degenen die aanvankelijk een slechtere SRLM‑integriteit hadden, meer kans hadden op snellere achteruitgang op standaard dementieschalen, zelfs na correctie voor leeftijd, geslacht en opleiding.
Wat dit kan betekenen voor patiënten en artsen
Voor leken suggereert dit werk dat artsen op een dag mogelijk een enkele dunne lijn op een routinematige MRI kunnen aflezen om zeer vroege tekenen van Alzheimer‑gerelateerde schade te herkennen. Omdat SRLM‑veranderingen eerder optreden dan duidelijke hersenkrimp en kunnen voorspellen wie waarschijnlijker zal achteruitgaan, zouden ze kunnen helpen om hoger‑risico‑individuen te identificeren voor nauwere monitoring, leefstijlinterventies of deelname aan klinische onderzoeken. De methode berust nog steeds op deskundig oordeel en scanners van hoge kwaliteit, en er zijn grotere studies nodig, maar het wijst op een toekomst waarin eenvoudige MRI‑kenmerken eerdere, nauwkeurigere waarschuwingssignalen voor geheugenstoornissen kunnen bieden.
Bronvermelding: Wang, K., Shao, B., Zeng, Q. et al. Trajectory of stratum radiatum, lacunosum and moleculare integrity in Alzheimer’s disease continuum. Sci Rep 16, 5796 (2026). https://doi.org/10.1038/s41598-026-35610-6
Trefwoorden: Ziekte van Alzheimer, hippocampus, hersenen MRI, vroegtijdige diagnose, geheugenverlies