Clear Sky Science · nl
Een proteomica- en roodox-proteomica-benadering om de heterogeniteit van ARDS te begrijpen
Waarom dit belangrijk is voor mensen op de intensive care
Acute Respiratory Distress Syndrome (ARDS) is een levensbedreigende vorm van longfalen die mensen met zware infecties, trauma of andere kritieke ziekten kan treffen. Veel patiënten met ARDS lijken aan het bed vergelijkbaar, maar sommigen herstellen terwijl anderen dat niet doen, en er is geen geneesmiddel dat bewezen het syndroom specifiek kan omkeren. Deze studie stelt een eenvoudige maar belangrijke vraag: als we nauwkeurig naar de eiwitten en chemische reacties in de longen en het bloed van ARDS-patiënten kijken, kunnen we dan verborgen biologische «types» van de ziekte ontdekken die verklaren waarom patiënten zo verschillend herstellen?
Kijken binnenin de longen, niet alleen in de bloedbaan
Om dit te onderzoeken volgden onderzoekers 16 volwassenen op een intensive care met ARDS die beademd werden. Binnen de eerste drie dagen na de diagnose namen ze bloed en een speciaal monster genaamd bronchoalveolar lavage (BAL)-vloeistof, een zachte spoeling van de longblaasjes. Waar mogelijk herhaalden ze deze afnames over meerdere dagen. Met hoogwaardige massaspectrometrie maten ze honderden eiwitten in elk monster (proteomica) en onderzochten ze, cruciaal, ook in welke mate sommige van deze eiwitten geoxideerd waren (roodox-proteomica), wat weerspiegelt hoeveel ze door reactieve zuurstofsoorten zijn beschadigd of gereguleerd—chemisch agressieve bijproducten van ontsteking.
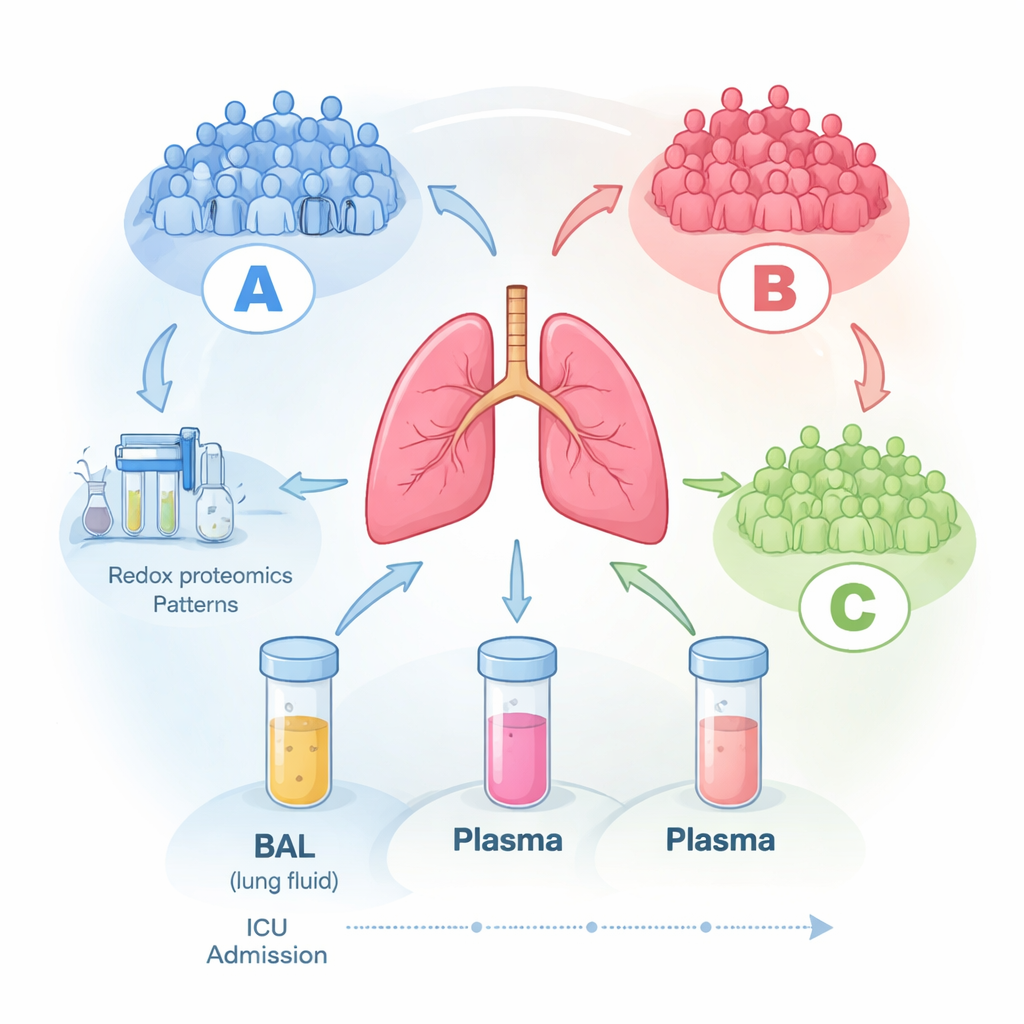
Drie verborgen patiëntengroepen komen naar voren
Toen het team de data onbevooroordeeld liet groeperen, zonder de computer iets over de patiënten te vertellen, verscheen er in de longvloeistofmonsters een duidelijk patroon: drie verschillende moleculaire groepen, aangeduid als A, B en C. Patiënten in groep A waren bij opname doorgaans ernstiger ziek, terwijl groepen B en C een mildere ziekte hadden. Opvallend genoeg bleven deze moleculaire signaturen grotendeels stabiel tot zes dagen op de ic, wat suggereert dat iedere patiënt eerder in een relatief consistent biologisch patroon valt dan willekeurig van dag tot dag te fluctueren. Standaard klinische meetwaarden—zoals zuurstofwaarden, ligduur of algemene ziektescoren—volgden deze moleculaire indelingen niet goed, wat erop wijst dat de gebruikelijke klinische hulpmiddelen belangrijke biologie in de longen missen.
Oxidatieve stress en de afweer van het lichaam
Een belangrijk thema in de data was de balans tussen schadelijke reactieve zuurstofsoorten en de antioxiderende verdediging van het lichaam. In groep A, de ernstigste groep, werden veel longeiwitten die betrokken zijn bij energieproductie en cellulair onderhoud op lagere niveaus aangetroffen. Nog veelzeggender was dat belangrijke antioxiderende enzymen zoals peroxiredoxinen, glutathion-geassocieerde eiwitten, thioredoxine en catalase significant verminderd waren. Daarentegen hadden groepen B en vooral C hogere niveaus van deze beschermende eiwitten, wat suggereert dat hun longen beter uitgerust waren om schadelijke oxidanten te ontgiften en bijkomende schade door ontsteking te beperken. Patronen in de oxidatietoestand van eiwitten voegden een extra laag toe, met verschillende subsets geoxideerde eiwitten die verrijkten in de meest en minst ernstige groepen.
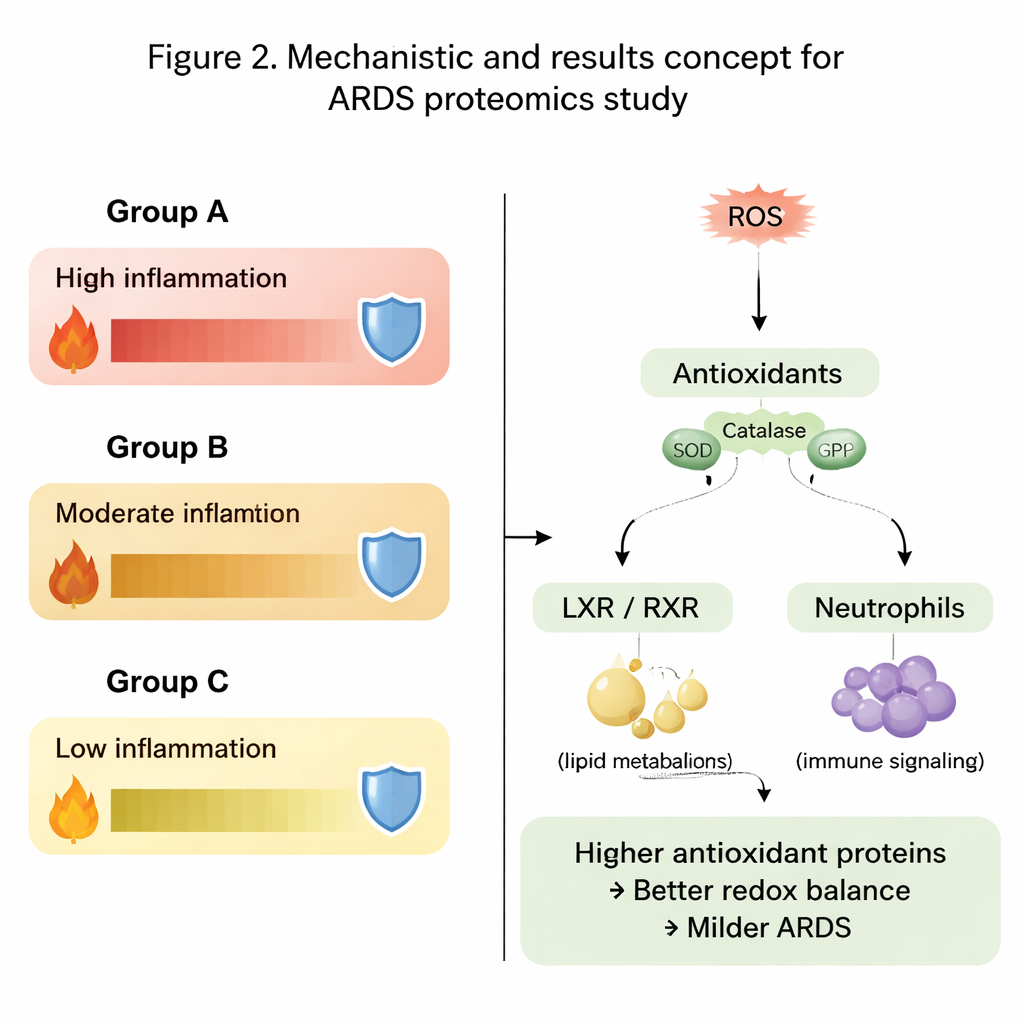
Signaleringsroutes die de ontsteking vormen
Naast afzonderlijke eiwitten onderzochten de auteurs volledige biologische routes. Ze ontdekten dat paden die samenhangen met ontsteking, cholesterol- en vetafhandeling, en immuuncelactiviteit zich anders gedroegen in de drie groepen. Signalen gekoppeld aan het liver X receptor–retinoid X receptor (LXR/RXR)-pad en een enzym genaamd DHCR24, die samen zowel het lipidenmetabolisme als immuunreacties helpen reguleren, waren bijzonder opvallend. In de meest ernstige groep werden deze routes voorspeld actiever te zijn, gecombineerd met verminderde signalering van de immuunboodschapper interleukine-12. Tegelijkertijd toonden paden die betrokken zijn bij reactieve zuurstofsoorten, hun ontgifting en neutrofiele (witte bloedcel) activiteit contrasterende patronen tussen longvloeistof en bloed, wat benadrukt dat wat lokaal in de long gebeurt kan verschillen van wat in de circulatie te zien is.
Wat dit zou kunnen betekenen voor toekomstige zorg
Deze kleine, verkennende studie verandert de behandeling vandaag niet, en de bevindingen moeten in veel grotere patiëntengroepen worden bevestigd. Ze toont echter aan dat we door eiwitten en hun roodox-toestand direct in longvloeistof te profileren—en niet alleen te vertrouwen op bloedtesten of bedrand-scores—biologisch betekenisvolle subtypes van ARDS kunnen onderscheiden. Deze subtypes verschillen in oxidatieve stress, antioxiderende capaciteit, metabolisme en immuunsignalisatie, en ze blijven relatief stabiel gedurende de eerste kritieke ziektedagen. In de toekomst zouden dergelijke moleculaire vingerafdrukken artsen kunnen helpen ARDS-patiënten in preciezere groepen te verdelen, gerichte therapieën op maat van elk patroon te kiezen en slimmere klinische onderzoeken te ontwerpen met een grotere kans om effectieve behandelingen te vinden.
Bronvermelding: Forshaw, T.E., Shukla, K., Wu, H. et al. A proteomics and redox proteomics approach to understanding ARDS heterogeneity. Sci Rep 16, 6034 (2026). https://doi.org/10.1038/s41598-026-35606-2
Trefwoorden: acute respiratory distress syndrome, proteomics, oxidative stress, bronchoalveolar lavage, critical care