Clear Sky Science · nl
Vergelijkende genomica van colistine‑niet‑gevoelige multiresistente Pseudomonas aeruginosa onthult opkomende lijnen in Thailand
Waarom deze ziekenhuisbacterie iedereen aangaat
Pseudomonas aeruginosa is een ziekenhuisbacterie die toeslaat wanneer mensen het zwakst zijn — na een operatie, aan beademingsapparatuur, of bij ernstige brandwonden of longziekten. Jarenlang vertrouwden artsen op een krachtig “laatste redmiddel”-antibioticum genaamd colistine wanneer andere middelen faalden. Deze studie onderzoekt stammen van Pseudomonas uit ziekenhuizen door heel Thailand die niet langer reageren op colistine of op veel andere antibiotica. Door het complete DNA van deze bacteriën te lezen, laten de onderzoekers zien hoe nieuwe, sterk medicijnresistente lijnen zich verspreiden en waarom dat patiënten, zorgverleners en zorgsystemen wereldwijd zou moeten verontrusten.
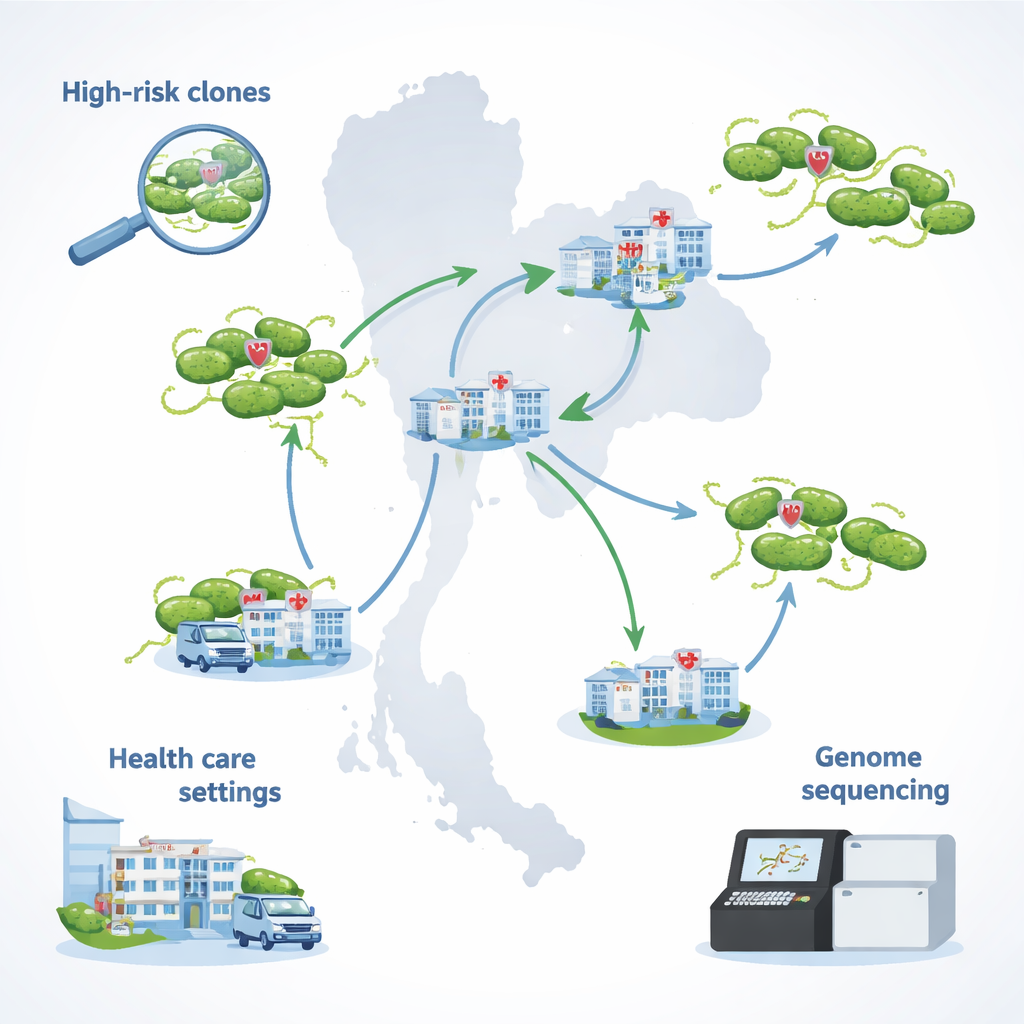
Een moeilijk te behandelen infectie volgen door Thailand
Het team concentreerde zich op 29 stammen van Pseudomonas aeruginosa die in 2021–2022 waren verzameld in ziekenhuizen die deelnemen aan Thailands nationale surveillanceprogramma voor antibioticaresistentie. Al deze stammen waren multiresistent: ze konden meerdere belangrijke klassen antibiotica weerstaan, waaronder middelen die gewoonlijk voor ernstige infecties worden gebruikt. Cruciaal is dat ze ook niet volledig gevoelig waren voor colistine, het middel dat vaak wordt bewaard voor levensbedreigende gevallen. De meeste monsters kwamen uit urine, maar anderen waren afkomstig uit bloed, sputum, pus en drainagevloeistoffen na operaties — wat de vele typen infecties weerspiegelt die deze bacterie bij opgenomen patiënten kan veroorzaken.
De genetische "vingerafdrukken" van de bacterie lezen
Met een combinatie van short‑read en long‑read DNA‑sequencing stelden de onderzoekers hoogwaardige genomen samen voor elke stam. Vervolgens vergeleken ze deze genomen om de bacteriën in genetische families te classificeren, bekend als sequence types. Er werden negen verschillende sequence types gevonden, wat op aanzienlijke diversiteit wijst. Eén type, aangeduid als ST5340, was nog nooit eerder beschreven. Het bleek nauwe verwantschap te hebben met een bekend internationaal hoogrisico‑kloon genaamd ST357, en verschilde slechts in één van de zeven standaard huishoudgenenen. Ondanks die nauwe relatie viel ST5340 op omdat al zijn isolaten resistent waren tegen alle geteste antibiotica, waarmee het zich ontpopte als een bijzonder zorgwekkende lijn.
Opkomende hoogrisicolijnen en hun verspreiding
Door kleine DNA‑verschillen, zogenaamde single‑nucleotide polymorphismen, op een rijtje te zetten over 108 Thaise Pseudomonas‑genomen (de 29 nieuwe plus 79 uit openbare databanken) bouwde het team een stamboom van de in het land circulerende stammen. Deze analyse benadrukte verschillende dominante clusters rond ST5340, ST357, ST654 en ST235 — lijnen die al bekend zijn, of nu opkomen, als “hoogrisico” omdat ze vaak multiresistent zijn en ziekenhuisuitbraken veroorzaken. ST5340 verscheen in het bijzonder in meerdere provincies en regio’s, wat suggereert dat het zich wijdverspreid verspreidt in plaats van beperkt te blijven tot één ziekenhuis. Andere wereldwijde hoogrisicoklonen, zoals ST654 en ST235, waren ook aanwezig, terwijl sommige wereldwijd belangrijke lijnen zoals ST244 ontbraken, waarschijnlijk omdat de studie alleen colistine‑niet‑gevoelige stammen omvatte.
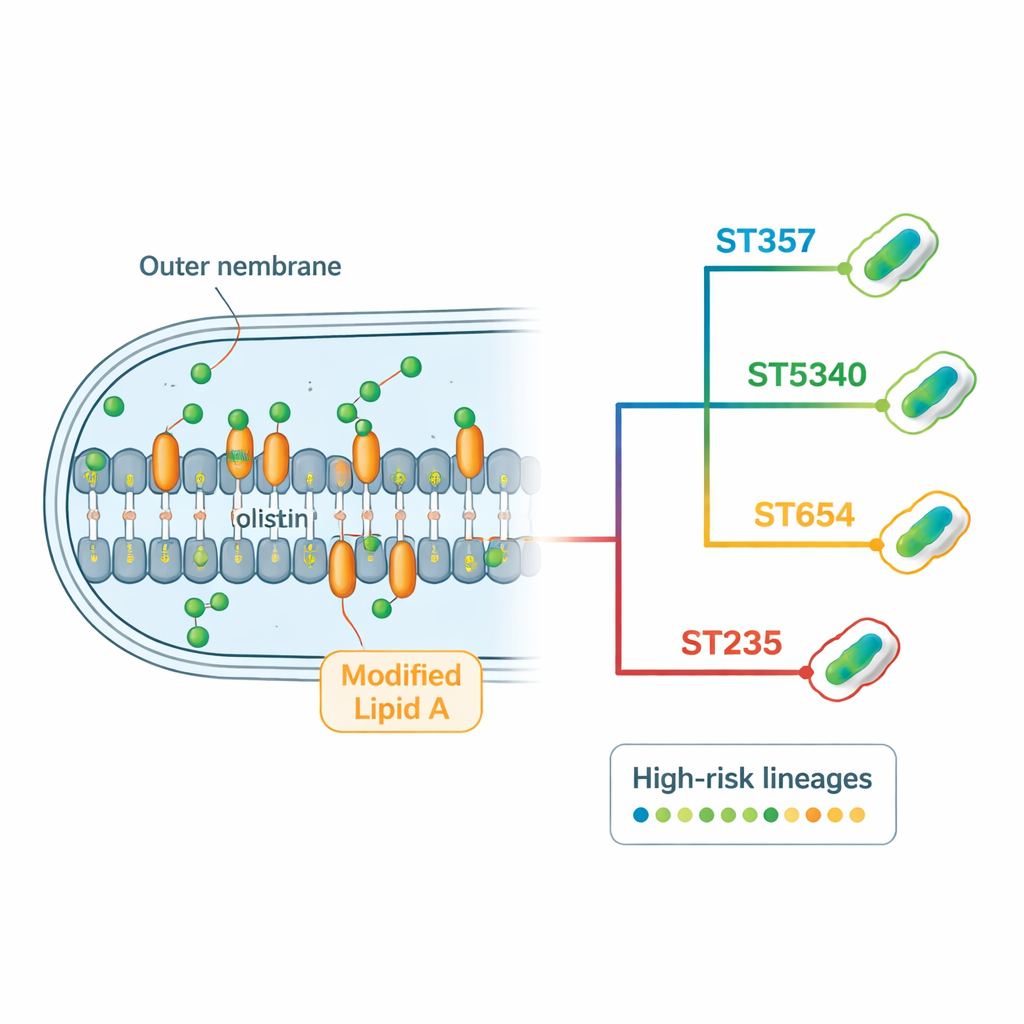
Hoe deze bacteriën antibiotica te slim af zijn
De genomische analyse toonde een bomvolle “resistoom” — de volledige set resistentiegenen en mutaties die elke stam draagt. Veel isolaten koderen meerdere typen beta‑lactamases, enzymen die veelgebruikte antibiotica zoals penicillines, cefalosporines en carbapenems afbreken. Het carbapenemasegen blaNDM‑1, geassocieerd met resistentie tegen enkele van de krachtigste ziekenhuisantibiotica, kwam in bijna alle stammen voor, soms in meerdere kopieën. De bacteriën droegen ook genen die aminoglycoside‑antibiotica chemisch modificeren, evenals krachtige effluxpompen die als moleculaire pompen functioneren om geneesmiddelen uit de cel te verwijderen. Voor colistine vond het team geen mobiele resistentiegenen, maar identificeerden ze herhaalde veranderingen in chromosomale genen die betrokken zijn bij het buitenste celmembraan en de regulatie daarvan. Bepaalde mutaties in regulerende eiwitten en in enzymen die lipid A opbouwen, waren sterk gelinkt aan colistine‑resistentie, vooral in de dominante ST357‑ en ST5340‑lijnen.
Wat dit betekent voor patiënten en ziekenhuizen
Door nationale surveillance te combineren met moderne genoomsequencing toont deze studie aan dat Thaise ziekenhuizen een groeiende dreiging ondervinden van een nieuw erkend hoogrisicokloon, ST5340, naast gevestigde wereldwijde probleemstammen. Deze bacteriën zijn niet alleen resistent tegen colistine maar ook tegen veel andere belangrijke middelen, waardoor behandelingsopties sterk worden beperkt wanneer patiënten ernstige infecties krijgen. Voor het algemene publiek is de boodschap duidelijk: antibioticaresistentie is geen abstract toekomstrisico maar een werkelijkheid van vandaag die de uitkomsten van operaties, intensivecare‑behandelingen en kankertherapie rechtstreeks kan beïnvloeden. De auteurs pleiten voor voortgezette genomische surveillance, strengere infectiepreventie en terughoudend antibioticagebruik om te voorkomen dat deze sterk resistente lijnen nog wijdverspreider en moeilijker te beheersen raken.
Bronvermelding: Wankaew, N., Arigul, T., Kruasuwan, W. et al. Comparative genomics of colistin-nonsusceptible multidrug-resistant Pseudomonas aeruginosa reveals emerging lineages in Thailand. Sci Rep 16, 5968 (2026). https://doi.org/10.1038/s41598-026-35520-7
Trefwoorden: Pseudomonas aeruginosa, antibioticaresistentie, colistine, genomische surveillance, ziekenhuisinfecties