Clear Sky Science · nl
Structurele en computationeel ondersteunde ontwikkeling van 2,5-gedisubstitueerde-1,3,4-oxadiazol-analoga als actieve LOX-, urease- en α-glucosidase-remmers
Nieuwe chemische hulpmiddelen om veelvoorkomende ziekten aan te pakken
Veel alledaagse gezondheidsproblemen — van zweren en nierstenen tot diabetes en chronische ontsteking — worden veroorzaakt door overactieve enzymen in ons lichaam. Deze studie onderzoekt een groep nieuw ontworpen kleine moleculen die als kleine remmen werken voor drie van zulke enzymen. Door hun structuren te verfijnen en ze zowel in het laboratorium als in computerstudies te testen, willen de onderzoekers een basis leggen voor effectievere en veiligere geneesmiddelen in de toekomst. 
Waarom deze enzymen belangrijk zijn
Het team richtte zich op drie enzymdoelen die elk een heel andere maar even belangrijke rol in de gezondheid spelen. Urease helpt ureum af te breken; wanneer het in bepaalde bacteriën of weefsels overactief wordt, kan het bijdragen aan maag- en urinewegaandoeningen, nierstenen en zelfs een verhoogde bloeddruk. Alpha-glucosidase zit op het oppervlak van darmcellen en knipt complexe koolhydraten in glucose; het remmen ervan is een gevestigde manier om de bloedsuiker bij type 2-diabetes te beheersen. Lipoxygenase (LOX) zet vetten om in signaalmoleculen die ontsteking, astma en sommige kankergerelateerde processen stimuleren. Geneesmiddelen die deze enzymen afremmen zonder andere systemen te schaden, worden daarom zeer gezocht.
Opbouw van een bibliotheek met kandidaat-moleculen
Om naar zulke geneesmiddelen te zoeken, bouwden de onderzoekers een reeks van 15 verwante verbindingen op basis van een ringsysteem dat 1,3,4-oxadiazool heet, gekoppeld aan een piperidine-eenheid. Dit chemische skelet komt al in meerdere moderne geneesmiddelen voor en staat bekend om zijn gunstige interacties met biologische doelwitten. Het team varieerde de “versieringen” die aan deze kern zijn bevestigd — kleine groepen zoals methyl, ethyl, methoxy, benzyl en cyclohexyl — op verschillende posities, en creëerde zo een kleine bibliotheek van kandidaten gelabeld 7a tot en met 7o. Ze bevestigden elke structuur met standaard analytische technieken zoals infrarood- en kernspinresonantiespectroscopie, om te verzekeren dat wat ze hadden gemaakt overeenkwam met hun ontwerpen.
Testen hoe goed de moleculen enzymen blokkeren
Elk verbinding werd vervolgens getest tegen gezuiverde LOX, urease en alpha-glucosidase om te bepalen hoe sterk het de activiteit van het enzym kon vertragen. Verschillende moleculen vielen op. Tegen alpha-glucosidase waren verbindingen 7a en 7n bijzonder effectief en presteerden in laboratoriumtests beter dan het standaard diabetesmiddel acarbose door hoge remmingspercentages te bereiken bij lage micromolaire concentraties. Voor LOX toonden verbindingen 7a, 7h en 7n zeer sterke activiteit, in sommige gevallen beter dan de natuurlijke referentie-remmer quercetine. In de urease-assays konden verbindingen 7a en vooral 7l wedijveren met of de standaardremmer thiourea licht overtreffen, wat suggereert dat ze mogelijk als leidende structuren voor anti-zweer- of anti-steentherapieën zouden kunnen dienen. 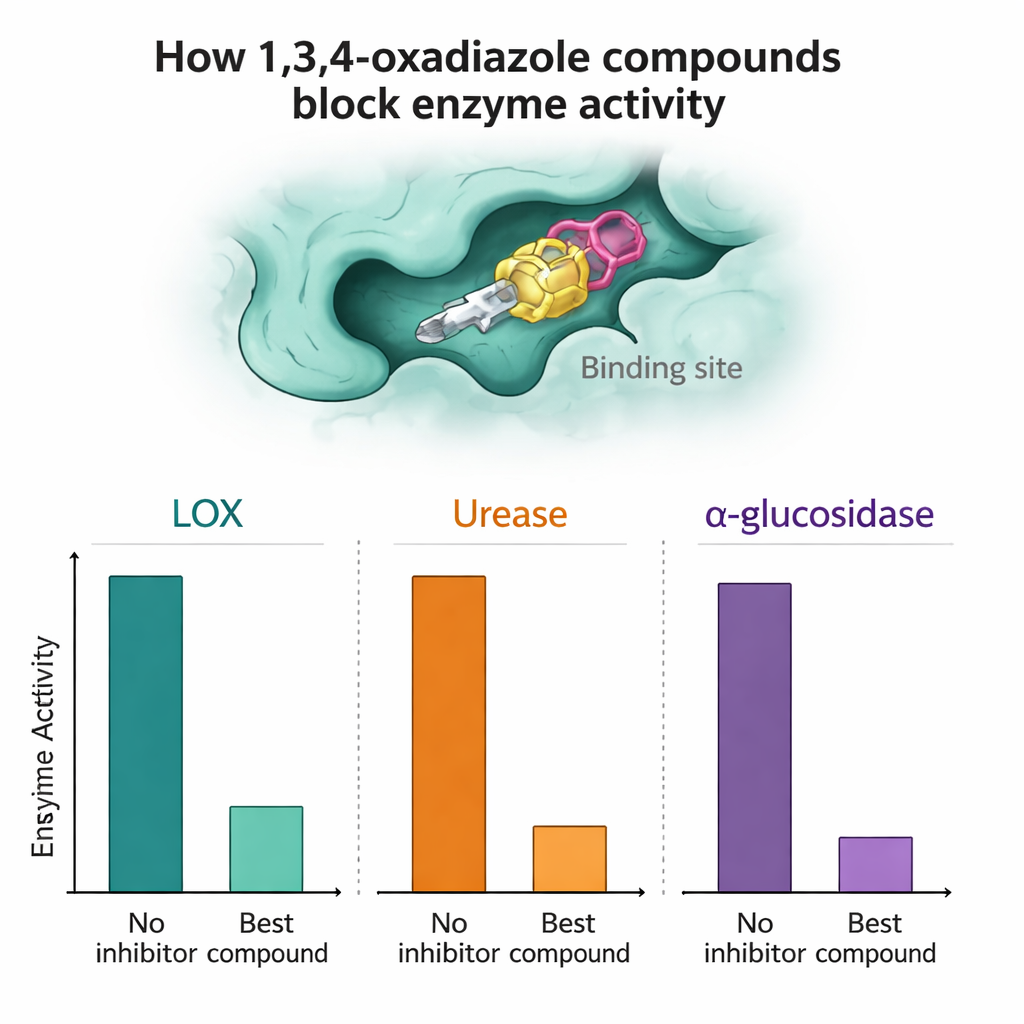
Structuur koppelen aan prestaties
Aangezien de enige verschillen tussen verbindingen 7a–7o kleine wijzigingen rond het kernringsysteem zijn, konden de onderzoekers beginnen eenvoudige structuur–activiteitsrelaties in kaart te brengen. Zo verbeterde het toevoegen van kleine koolstofrijke groepen op bepaalde “ortho”-posities van een aangehechte ring vaak het vermogen om alpha-glucosidase of LOX te remmen. Andere substituties, zoals bepaalde methoxy- of estergroepen op minder gunstige plaatsen, leken de activiteit juist te verzwakken. Om te begrijpen waarom gebruikte het team computersimulaties. Kwantumchemische berekeningen toonden aan dat alle moleculen thermodynamisch stabiel en flexibel genoeg waren om zich aan te passen aan enzympockets. Dockingstudies — het virtueel passend maken van elk molecuul in driedimensionale modellen van de enzymen — onthulden dat de meest actieve verbindingen strakkere contacten vormden via een mix van waterstofbruggen en hydrofobe (olie-achtige) interacties op sleutelplekken in de actieve centra, terwijl zwakkere kandidaten minder nauw aansloten of kritieke contactpunten misten.
Wat dit betekent voor toekomstige geneesmiddelen
Simpel gezegd identificeert de studie een handvol veelbelovende “sleutels” die goed passen in drie ziektegerelateerde “sloten” en begint uit te leggen op atomair niveau waarom sommige sleutels beter draaien dan andere. Geen van deze moleculen is echter klaar als geneesmiddel — ze hebben nog veiligheidsonderzoek, optimalisatie voor gedrag in het lichaam en proeven in dieren en mensen nodig. Maar het werk toont aan dat het 1,3,4-oxadiazool–piperidine-framework een vruchtbaar uitgangspunt is voor toekomstige behandelingen gericht op diabetes, ontstekingsaandoeningen en urease-gerelateerde stoornissen. De combinatie van zorgvuldige laboratoriummetingen met gedetailleerde computermodellering biedt een routekaart om deze kandidaten scherper te maken tot meer precieze en effectieve geneesmiddelen.
Bronvermelding: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
Trefwoorden: enzymremmers, geneesmiddelenontdekking, oxadiazoolverbindingen, diabetes en ontsteking, urease en lipoxygenase