Clear Sky Science · nl
SHP2 bevordert osteosarcoom via regulatie van STAT3/TET3/HOXB2-signaaltransductie
Waarom deze studie naar botkanker ertoe doet
Osteosarcoom is de meest voorkomende primaire botkanker bij kinderen en tieners, en ondanks moderne chemotherapie en chirurgie is de overleving voor patiënten met gevorderde of teruggekeerde ziekte decennialang nauwelijks verbeterd. Deze studie onderzoekt de interne bedrading van osteosarcoomcellen om te achterhalen welke moleculen als "hoofdschakelaars" fungeren die tumoren helpen groeien, uitzaaien en therapieresistentie ontwikkelen. Door een belangrijk regelpad te onthullen met het eiwit SHP2 in het middelpunt, wijst het werk op nieuwe geneesmiddeldoelen die osteosarcoomtherapieën mogelijk effectiever en gerichter kunnen maken.
De aanwijzingen volgen in tumorgene-activiteit
De onderzoekers begonnen met het behandelen van osteosarcoom als een data-analyseprobleem. Ze doorzochten openbare genexpressiedatasets die tumormonsters met normaal botweefsel vergeleken en gebruikten statistische instrumenten om genen te vinden die consequent hoger of lager tot expressie werden gebracht in kanker. Honderden genen verschilden, en veel daarvan waren gegroepeerd in bekende kankerpaden die celgroei, overleving en migratie aansturen. Onder deze genen sprong één eiwit eruit: SHP2, dat fungeerde als een knooppunt sterk verbonden met meerdere anderen: de signaalfactor STAT3, het DNA-bewerkende enzym TET3 en de ontwikkelingsregulator HOXB2. Dit suggereerde dat deze moleculen een verbonden keten zouden kunnen vormen die osteosarcoomcellen agressief laat gedragen. 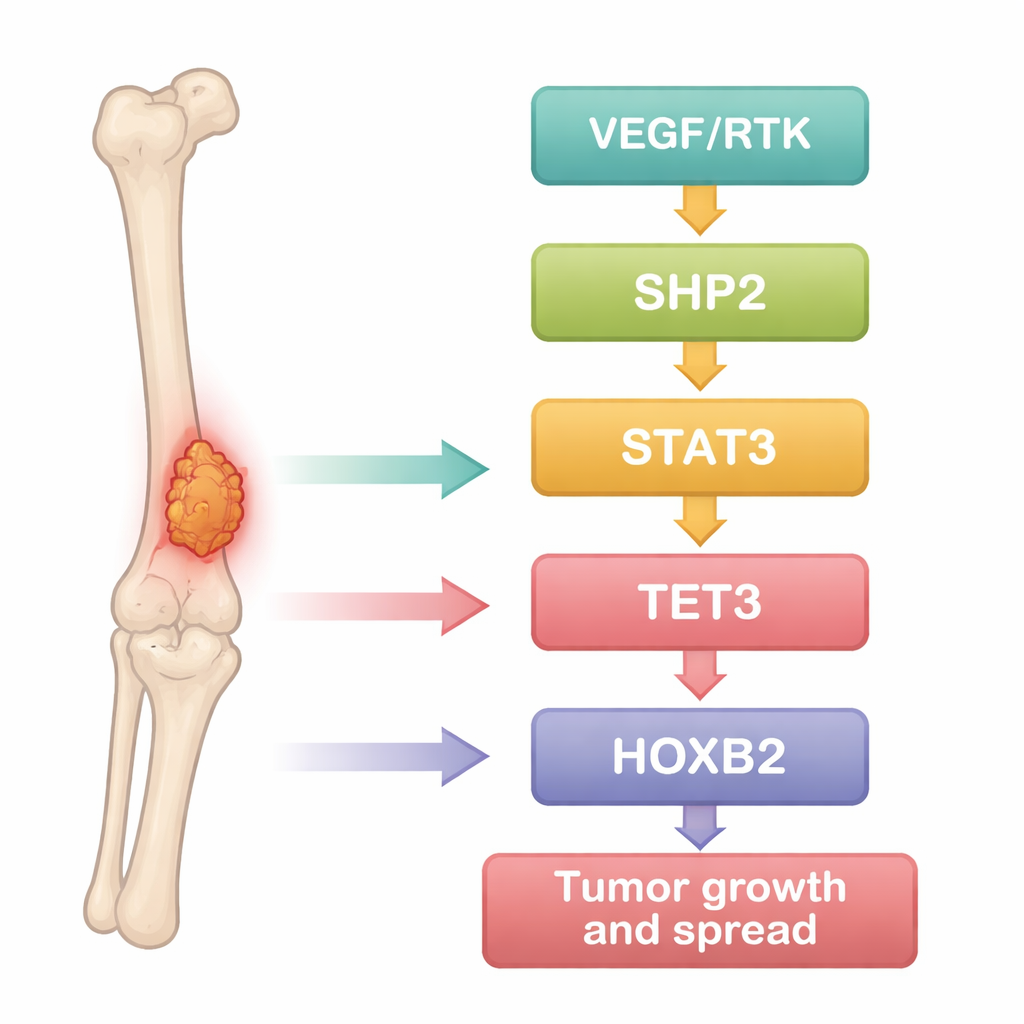
De rol van SHP2 in kankercellen testen
Om verder te gaan dan correlaties, manipuleerde het team humane osteosarcoomcelijnen (143B en MG63) zodat SHP2 ofwel werd verlaagd ofwel werd verhoogd. Wanneer ze SHP2 onderdrukten, daalde duidelijk de capaciteit van de cellen om zich te vermenigvuldigen, over een oppervlak te migreren en door een membraan heen te dringen. De niveaus van de eiwitten STAT3, TET3 en HOXB2, evenals kankergerelateerde merkers zoals c-Myc, NANOG en NUSAP1, namen ook af. Wanneer ze STAT3 opnieuw activeerden of HOXB2 overexpresseerden, werden veel van deze effecten teruggedraaid, wat aangeeft dat SHP2 bovenaan een keten staat die uiteindelijk invloed heeft op genen die celdeling, stamcelachtige eigenschappen en de machinerie van de mitose regelen.
Een stapsgewijs kankerpadoverzicht opbouwen
Aan de hand van de experimenten schetsen de auteurs een stapsgewijs model. In de tumoromgeving stimuleren hoge niveaus van vasculair endotheliale groeifactor (VEGF) receptor-tyrosinekinasen (RTKs) aan het celoppervlak. Deze activeren op hun beurt SHP2 in de cel. Actief SHP2 schakelt STAT3 in, een transcriptiefactor die naar de kern verhuist en helpt de productie van TET3 te verhogen. TET3 bewerkt vervolgens de chemische labels op DNA door methylgroepen van het HOXB2-genregio te verwijderen. Deze demethylatie werkt als het wegnemen van een rem, waardoor HOXB2 sterker tot expressie kan komen. HOXB2, een gen dat normaal ontwikkeling stuurt, verhoogt nu de activiteit van c-Myc, NANOG en NUSAP1, die samen onverzadigbare tumorgroei aanwakkeren, invasief gedrag versterken en eigenschappen ondersteunen die geassocieerd zijn met metastase.
Van petrischaal naar levende dieren
Om te beoordelen of dit pad relevant was in volledige tumoren, implanterden de wetenschappers gemodificeerde osteosarcoomcellen onder de huid van muizen. Tumoren die werden gevormd door cellen die te veel SHP2 produceerden, groeiden groter en zwaarder dan controletumoren. Toen TET3 in deze SHP2-rijke cellen werd uitgeschakeld, vertraagde de tumorgroei en daalden de niveaus van HOXB2, hoewel SHP2 en STAT3 actief bleven. Herintroductie van HOXB2 herstelde de vitale groei van de tumor. Doorlopend weerspiegelden eiwitmetingen in tumorweefsel de eerder gevonden kweekresultaten, wat het idee versterkt dat SHP2, STAT3, TET3 en HOXB2 een verbonden as vormen die osteosarcoom naar een meer kwaadaardig gedrag duwt. 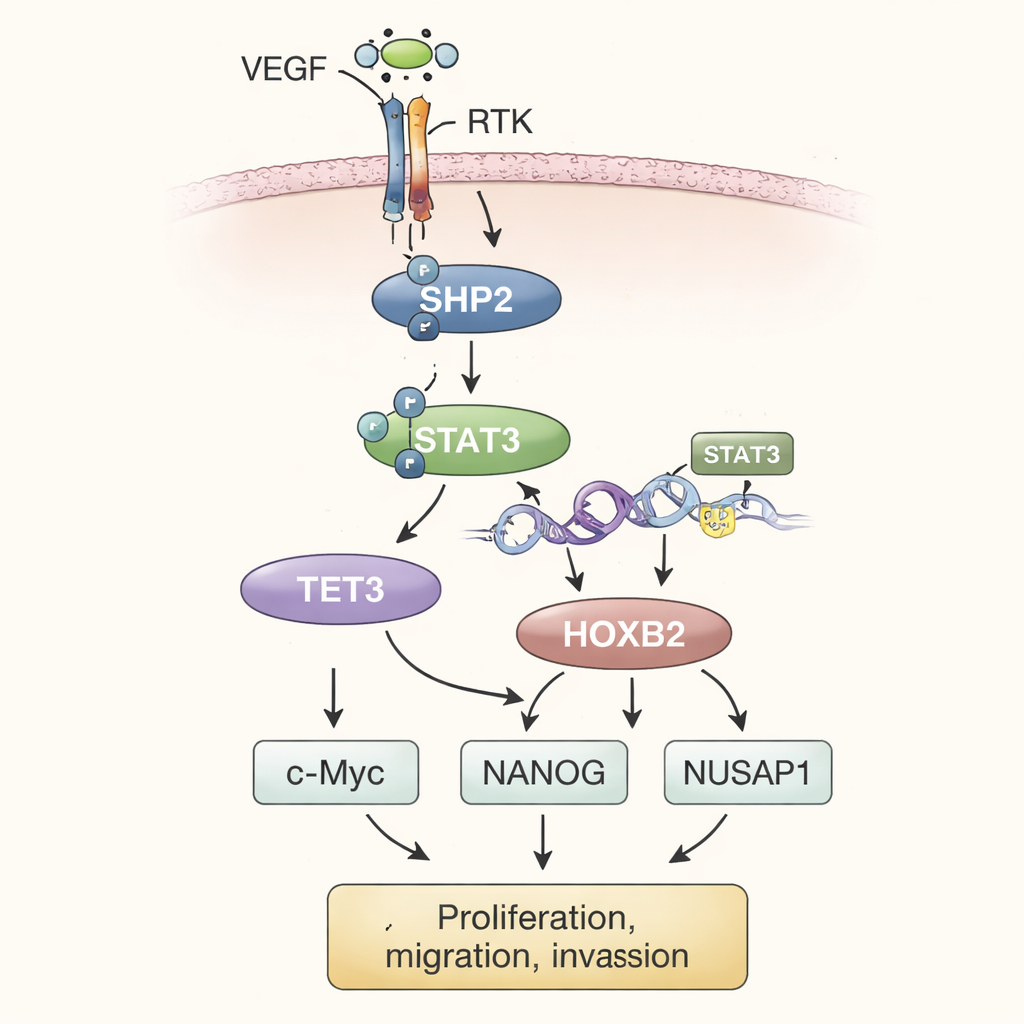
Wat dit betekent voor toekomstige behandelingen
Voor een niet-specialistische lezer is de kernboodschap dat de onderzoekers een duidelijk signaalpad in kaart hebben gebracht — van VEGF en zijn receptoren aan het celoppervlak, via SHP2 en STAT3, tot TET3, HOXB2 en meerdere krachtige groeigenen — dat helpt verklaren waarom osteosarcoom snel kan groeien en vroeg kan uitzaaien. Omdat SHP2 en STAT3 enzymen zijn die in principe met kleine-molecuulremmers kunnen worden geblokkeerd, en TET3 en HOXB2 latere stappen in hetzelfde traject markeren, biedt dit pad meerdere ingreeppunten waar toekomstige therapieën op kunnen mikken. Hoewel deze studie in cellijnen en muismodellen is uitgevoerd, levert het een gedetailleerde kaart die geneesmiddelenontwikkelaars kunnen gebruiken om combinatietherapieën te ontwerpen die de centrale schakelaars van de tumor uitschakelen in plaats van alleen de eindresultaten aan te vallen.
Bronvermelding: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
Trefwoorden: osteosarcoom, SHP2, STAT3-route, tumorsignaaltransductie, gerichte therapie