Clear Sky Science · nl
Op immunoinformatica gebaseerde ontwerp en evaluatie van een multi-epitoopvaccin tegen Vibrio fluvialis
Waarom een nieuw vaccin belangrijk is voor liefhebbers van zeevruchten
Vibrio fluvialis is een minder bekende verwant van de bacteriën die cholera veroorzaken, leeft in warme kustwateren en kan schaaldieren en drinkwater besmetten. Het veroorzaakt ernstige diarree en darminfecties en komt steeds vaker voor naarmate de oceanen opwarmen en antibiotica hun effectiviteit verliezen. Er bestaat echter nog geen vaccin voor mensen. Deze studie gebruikt geavanceerde computermethoden om een nieuw soort experimenteel vaccin te ontwerpen, opgebouwd uit zorgvuldig gekozen kleine fragmenten van de bacterie, met als langetermijndoel mensen te beschermen die worden blootgesteld via voedsel, water of door klimaatgedreven overstromingen.

Van verborgen dreiging naar duidelijk doelwit
Vibrio fluvialis wordt vaak verward met andere Vibrio-soorten, wat betekent dat zijn rol bij voedselovergedragen ziekten waarschijnlijk onderschat is. Uitbraken zijn gekoppeld aan besmette zeevruchten en vervuild water, en recente stormen en overstromingen hebben deze bacteriën landinwaarts gebracht, waardoor mensen ver van de kust ziek zijn geworden. Veel patiënten hebben ziekenhuiszorg nodig, en een verontrustend aantal stammen resistent tegen meerdere antibiotica. Omdat het oppervlak van de microbe vergelijkbaar is met dat van verwante bacteriën, kunnen artsen infecties verkeerd diagnosticeren, wat de juiste behandeling vertraagt. Dit alles creëert een sterke behoefte aan preventie in plaats van alleen op geneesmiddelen te vertrouwen.
Een vaccin ontwerpen binnen een computer
In plaats van hele bacteriën in het laboratorium te kweken, wendden de onderzoekers zich tot "immunoinformatica" — het gebruik van software om te voorspellen welke kleine stukjes van Vibrio fluvialis het meest waarschijnlijk door het menselijke immuunsysteem worden herkend en aangevallen. Ze concentreerden zich op twee membraaneiwitten die op het oppervlak van de bacterie zitten en belangrijk zijn voor zijn overleving en ziekteverwekkend vermogen. Uit deze eiwitten haalde het team tien korte segmenten, epitopen genoemd, die door zowel T-cellen als B-cellen kunnen worden herkend, de belangrijkste strijders van onze immuunverdediging. Vervolgens verbonden ze deze stukjes tot één keten van 246 aminozuren, voegden korte schakelstukjes toe zodat het immuunsysteem elk onderdeel goed kan verwerken, en een adjuvantsfragment om de algehele respons te versterken.
Controle op kracht, veiligheid en wereldwijde reikwijdte
Zodra het virtuele vaccin was opgebouwd, voerde het team een reeks tests volledig in silico uit, dat wil zeggen op computers in plaats van in dieren of mensen. Programma's voorspelden dat het gecombineerde construct sterk "zichtbaar" zou zijn voor het immuunsysteem maar onwaarschijnlijk allergieën of toxiciteit zou uitlokken. De gekozen epitopen kwamen overeen met veelvoorkomende varianten van immuungerelateerde genen uit de hele wereld, wat suggereert dat ongeveer 99,97 procent van de wereldbevolking zou kunnen reageren, inclusief mensen in zwaar getroffen regio's zoals Zuid- en Oost-Azië. Het vaccineiwit leek ook stabiel, voldoende hydrofiel om goed op te lossen, en geschikt voor efficiënte productie in standaard laboratoriumbacteriën, wat de uiteindelijke fabricage praktischer maakt.
Hoe het vaccin mogelijk bescherming opwekt
De onderzoekers vroegen zich vervolgens af of het ontworpen eiwit plausibel zou binden aan een echt immuunsensor. Met moderne structuurvoorspellingshulpmiddelen bouwden ze een driedimensionaal model van het vaccin en simuleerden ze hoe het mogelijk zou kunnen andocken op Toll-like receptor 2 (TLR2), een molecule op immuuncellen die bacteriële componenten detecteert. Computerdocking suggereerde een nauwe passing tussen het vaccin en TLR2, ondersteund door vele stabiliserende moleculaire contacten. Lange, gedetailleerde bewegingssimulaties over 100 nanoseconden gaven aan dat het vaccin‑receptorpaar stabiel en compact bleef in de tijd. Aanvullende immuunsysteem-simulaties voorspelden sterke golven van antilichamen en T-celactiviteit, samen met de vorming van geheugencellen die in principe blijvende bescherming tegen Vibrio fluvialis zouden kunnen bieden.
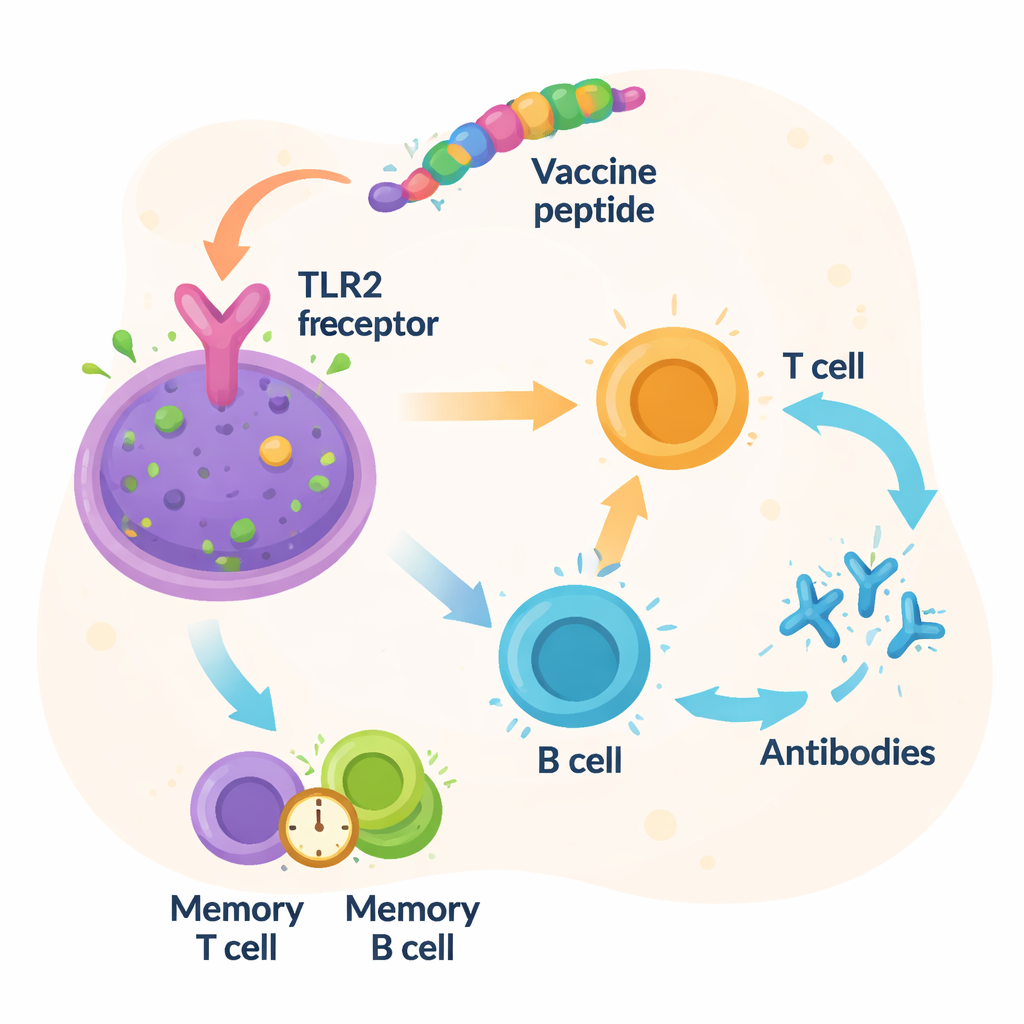
Van digitaal bouwplan naar praktische bescherming
In gewone bewoordingen biedt dit werk een digitaal "bouwplan" voor een toekomstig Vibrio fluvialis-vaccin opgebouwd uit slechts de belangrijkste fragmenten van de bacterie, zodanig gerangschikt dat het breed werkzaam en mogelijk veiliger is dan vaccins met hele cellen. De studie toont aan dat dit construct herkenbaar zou zijn voor de meeste menselijke immuunsystemen, goed zou binden aan een belangrijke immuunsensor en produceerbaar zou zijn met gangbare middelen. Al deze resultaten zijn echter afkomstig van computermodellen. De volgende stappen vereisen het produceren van het vaccin in het laboratorium, testen in cellen en dieren, en uiteindelijk klinische proeven om te bevestigen dat het inderdaad beschermt tegen infectie zonder schadelijke bijwerkingen. Als die testen slagen, zouden dergelijke multi-epitoopvaccins krachtige nieuwe middelen kunnen worden tegen voedselovergedragen bacteriën in een opwarmende, steeds dichter bevolkte wereld.
Bronvermelding: Naveed, M., Husnain, M., Aziz, T. et al. Immunoinformatics-based design and evaluation of a multi-epitope vaccine against Vibrio fluvialis. Sci Rep 16, 4100 (2026). https://doi.org/10.1038/s41598-026-35434-4
Trefwoorden: Vibrio fluvialis, multi-epitoopvaccin, voedselovergedragen infectie, immunoinformatica, antibioticaresistentie