Clear Sky Science · nl
Ontwikkeling van een wereldwijd screeningsysteem voor het detecteren van eiwit–eiwitinteracties via luminescentie-complementatie in Schizosaccharomyces pombe
Het verborgen leven van eiwitten verlichten
Elke hartslag, gedachte en ademhaling in ons lichaam berust op eiwitten die samenwerken in cellen. Deze subtiele partnerschappen, eiwit–eiwitinteracties genoemd, regelen alles van hoe genen worden afgelezen tot hoe cellen op stress reageren. Veel van die interacties zijn vluchtig of kwetsbaar, waardoor ze moeilijk te detecteren zijn met bestaande technieken. Deze studie beschrijft een nieuw, zeer gevoelig "lichtgebaseerd" screeningsysteem dat is opgebouwd in een eenvoudig modelorganisme, de klisjesgist (fission yeast), om zo duizenden van die verborgen eiwitverbindingen tegelijkertijd aan het licht te brengen.
Waarom eiwitpartnerschappen zo moeilijk te zien zijn
Eiwitten werken zelden alleen. Ze binden op verschillende momenten verschillende partners, soms slechts voor korte tijd, en hun gedrag kan worden gewijzigd door chemische aanpassingen of door hun locatie in de cel. Traditionele methoden om deze interacties te bestuderen halen eiwitten vaak uit hun natuurlijke omgeving of vertrouwen op genetische trucs die niet elke koppeling vangen. Daardoor zijn bestaande kaarten van wie met wie in de cel interacteert onvolledig. De auteurs wilden dit beeld verbeteren door een flexibeler, gevoeliger systeem te maken dat vrijwel elk eiwit in klisjesgist in levende cellen kan onderzoeken.
Van aanraking naar licht
De kern van de nieuwe benadering is een gespleten enzym dat licht afgeeft. Het ene deel, LgBiT genoemd, is gekoppeld aan een "aas"-eiwit dat de onderzoekers willen bestuderen. Het andere deel, SmBiT, is gekoppeld aan vele mogelijke "prooi"-partners, één per giststam. Op zichzelf interageren deze twee enzymonderdelen nauwelijks. Maar wanneer aas en prooi in de cel aan elkaar binden, klikken de twee stukjes in elkaar en vormen ze een werkend enzym dat oplicht in aanwezigheid van een chemische brandstof. Door te meten hoeveel licht elke giststam produceert, kan het team bepalen welke eiwitten daadwerkelijk in de cel elkaar ontmoeten en hoe sterk ze interageren. Om te voorkomen dat partners worden gemist omdat de tag de normale functie blokkeert, wordt het aas-eiwit in twee versies gemaakt, met LgBiT aan het ene of het andere uiteinde, waardoor de kans sterk toeneemt dat ten minste één oriëntatie werkt. 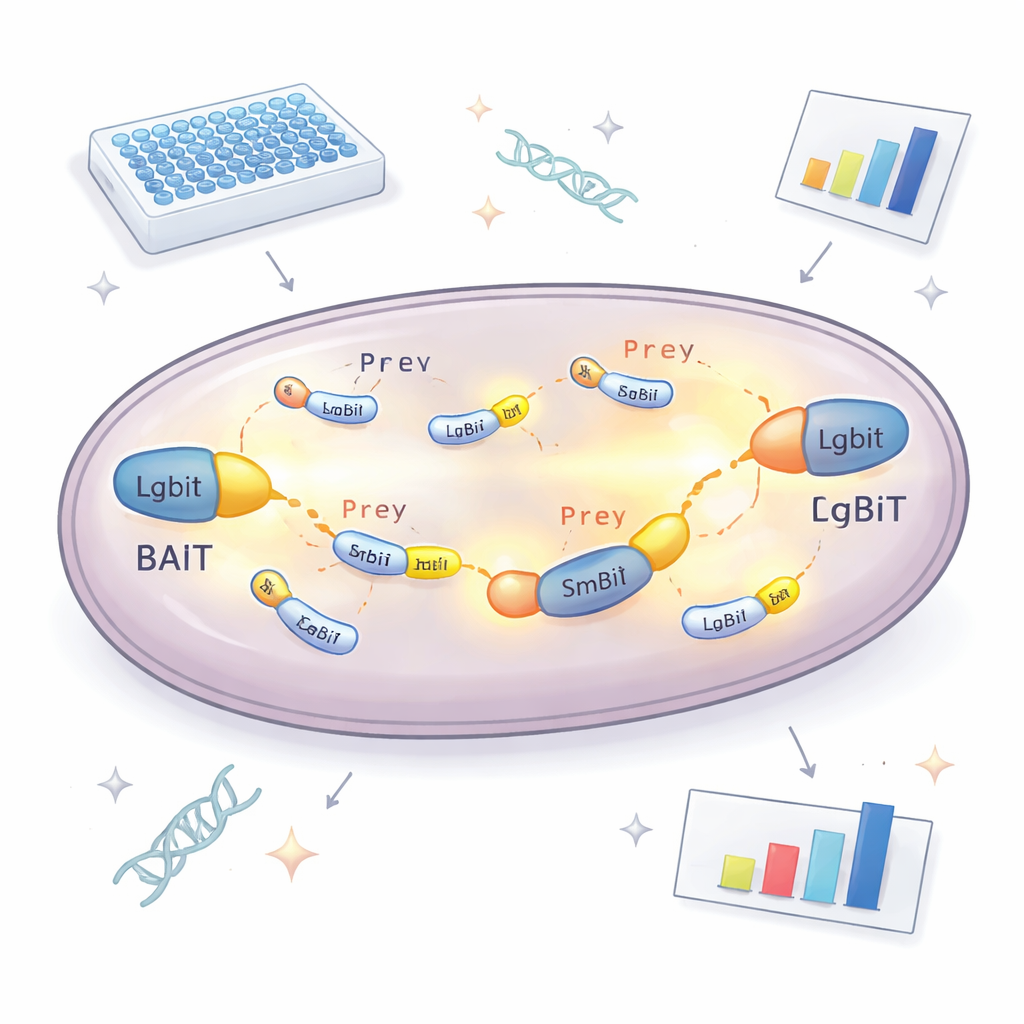
Het ontwerpen van een gistbibliotheek en stam-systeem
Het opbouwen van dit platform vereiste meer dan een slim enzym. De onderzoekers moesten ook duizenden prooi-eiwitten op een gecontroleerde, enkelvoudige manier in de gist introduceren. Ze ontwierpen een speciaal DNA-vector voor prooi-eiwitten dat in een gedefinieerde plek in het gistgenoom insereert en een rood fluorescerend merkteken draagt. De helderheid van dit rode signaal weerspiegelt hoeveel kopieën zijn ingebracht, waardoor het team eenvoudig kolonies met precies één kopie kan selecteren — essentieel voor betrouwbare vergelijkingen. Ze creëerden ook specifieke aas-vectoren die LgBiT aan het begin of het einde van het aas-eiwit plaatsen, gescheiden door flexibele linkers zodat het eiwit normaal kan vouwen en bewegen. Zorgvuldig geconstrueerde giststammen werden vervolgens gebouwd om twee aas-constructen en één prooi-construct tegelijk te herbergen, met behulp van voedingsmarkers zodat alleen correct gecombineerde cellen overleven.
Het systeem op de proef stellen
Om te controleren of hun ontwerp de detectie daadwerkelijk verbeterde, onderzochten de wetenschappers eerst eiwitten met goed bekende partners. Ze bevestigden dat de signaalsterkte sterk afhing van waar de lichtgevende tag was bevestigd: sommige interacties verschenen alleen wanneer LgBiT aan het ene uiteinde van het aas zat, en niet aan het andere. Het tegelijk tot expressie brengen van beide versies verhoogde de lichtopbrengst, wat bewijst dat de dubbele-aasstrategie zwakke of oriëntatiegevoelige interacties beter vangt. Het systeem detecteerde ook contacten waarbij membraangebonden eiwitten betrokken waren, een klasse die berucht moeilijk is voor traditionele yeast two-hybrid-methoden. Met deze validatie schaarden ze zich vervolgens achter een genoomwijde screen, waarbij ze een transcriptiegerelateerd eiwit genaamd Tfs1 als aas gebruikten. Bij het screenen van meer dan 4.600 prooi-eiwitten vonden ze 31 sterke kandidaten, waaronder enkele reeds bekende partners en veel nieuwe, sommige gelokaliseerd buiten de kern in gebieden zoals mitochondriën en het celoppervlak. 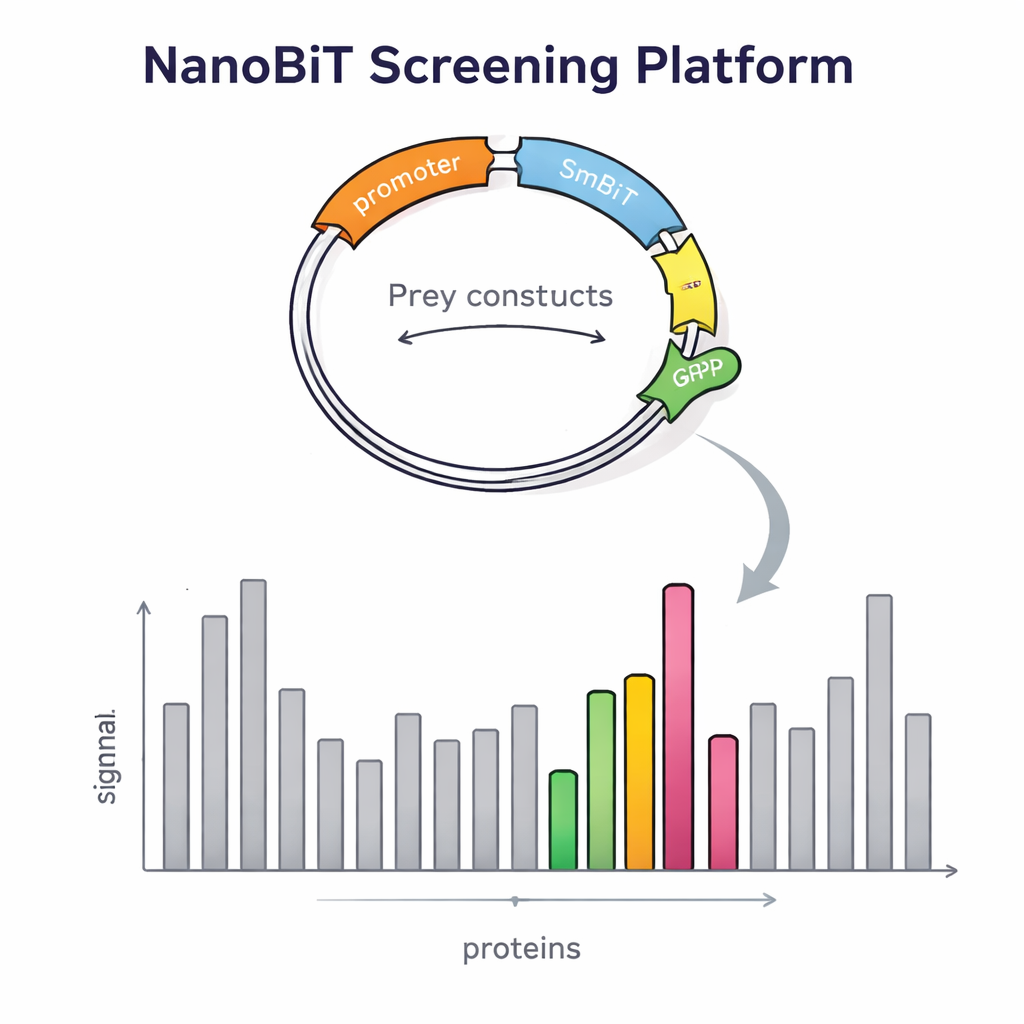
Wat dit betekent voor biologie en geneesmiddelontwikkeling
Voor niet-specialisten is de kernboodschap dat de auteurs een gevoeliger "interactieradar" binnen gistcellen hebben gebouwd. Door vluchtige eiwit-handdrukken om te zetten in meetbare lichtflitsen, en door de genetica zo te rangschikken dat drie getagde eiwitten samen kunnen worden uitgedrukt, onthult hun systeem zowel bekende als eerder onzichtbare eiwitpartners. Hoewel verdere bevestiging met andere technieken nog nodig is om elk nieuw paar te verifieren, vult dit platform belangrijke leemtes in onze kaarten van cellulaire netwerken. Omdat de stammen ook zodanig zijn geconstrueerd dat ze gevoeliger zijn voor kleine moleculen, kan dezelfde opzet worden aangepast om te zoeken naar geneesmiddelen die schadelijke eiwitpartnerschappen verstoren of gunstige partnerschappen stabiliseren, wat een krachtig nieuw hulpmiddel biedt voor zowel fundamentele biologie als vroege fase geneesmiddelontdekking.
Bronvermelding: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Trefwoorden: eiwitinteracties, schizosaccharomyces pombe, luminescentie-assay, hoge doorvoerscreening, hulpmiddelen voor geneesmiddelonderzoek