Clear Sky Science · nl
Sequentiële platina‑ en PARP‑remming verbetert PD1‑immunotherapie bij muizen met BRCA2‑gemuteerde alvleesklierkanker
Waarom dit onderzoek belangrijk is voor patiënten
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker, en zelfs wanneer artsen weten dat een tumor een behandelbare kwetsbaarheid heeft — zoals een mutatie in het BRCA2‑gen — houden huidige behandelingen de ziekte zelden langdurig onder controle. Deze studie gebruikt een realistisch muismodel om een praktische vraag te onderzoeken die veel patiënten en oncologen nu bezighoudt: kan het toevoegen van moderne immunotherapie na krachtige chemotherapie en een PARP‑remmer de overleving betekenisvol verlengen, en waarom komt de tumor zo vaak terug?
Een hardnekkige kanker met een genetische zwakke plek
Pancreasductaal adenocarcinoom is berucht moeilijk te behandelen, met een vijfjaarsoverleving die nog steeds in de enkelcijferige percentages ligt. Een kleine groep patiënten draagt erfelijke of tumor‑specifieke defecten in BRCA2, een gen dat nodig is voor het herstel van gebroken DNA. Deze tumoren zijn ongewoon gevoelig voor DNA‑schadende middelen, zoals platina‑gebaseerde chemotherapie, en voor PARP‑remmers, die het vermogen van kankercellen om DNA te repareren verder aantasten. De huidige standaardzorg voor gevorderde BRCA‑gemuteerde alvleesklierkanker bestaat uit maanden platina‑chemotherapie gevolgd door onderhoudsbehandeling met een PARP‑remmer. Toch verlengde deze strategie in de belangrijke POLO‑klinische studie de totale overleving niet, wat de noodzaak onderstreept om resistentie te begrijpen en betere onderhoudsbenaderingen te ontwerpen.
Een levensechter muismodel bouwen
Veel bestaande laboratoriummodellen ontdoen tumoren van de immuun‑ en stromacomponenten die echte tumoren bij patiënten omringen. Om dit te vermijden, creëerden de auteurs muizen die BRCA2‑deficiënte alvleesklier tumoren ontwikkelen in de context van een volledig functionerend immuunsysteem. Uit deze spontane tumoren derivereerden ze klonale cellijnen die geïmplanteerd konden worden in genetisch gematchte muizen. Deze Brca2‑gemuteerde tumoren leken en gedroegen zich sterk als menselijke alvleesklierkankers: ze waren dicht fibrotisch, sloten grotendeels T‑cellen uit en vertoonden hoge niveaus van spontane DNA‑schade. Cruciaal was dat de tumoren zeer gevoelig waren voor een veelgebruikte platina‑combinatie (gemcitabine plus cisplatine), terwijl behandeling met een PARP‑remmer alleen in dieren slechts bescheiden en kortstondige effecten had, ondanks sterke activiteit tegen dezelfde cellen in kweek. 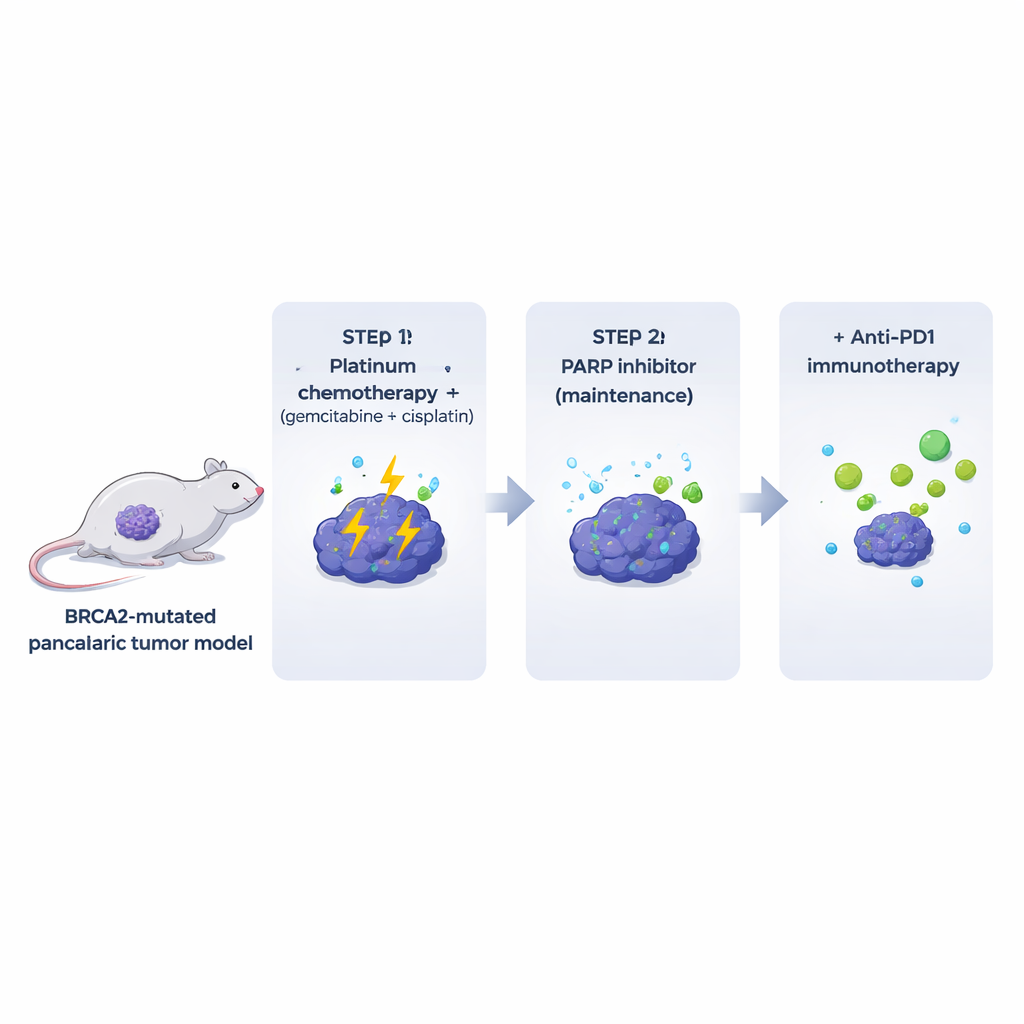
Chemotherapie hervormt de tumoromgeving
Het team vroeg vervolgens wat er in de tumor gebeurt na platina‑chemotherapie. Tien dagen na behandeling waren de tumoren gekrompen maar niet uitgeroeid. Genexpressie‑analyses toonden een opvallende verschuiving naar immuungerelateerde activiteit: routes gekoppeld aan T‑celactivatie en adaptieve immuniteit werden geactiveerd. Meer T‑cellen werden aangetroffen in de behandelde tumoren, en veel van deze T‑cellen droegen uitputtingsmarkers — aanwijzingen dat ze geactiveerd waren maar minder effectief werden. Vergelijkbare patronen van verhoogde T‑celaanwezigheid werden waargenomen in menselijke alvleesklierkankers met BRCA‑ of aan PALB2 gerelateerde mutaties nadat patiënten vóór operatie platina‑gebaseerde chemotherapie hadden gekregen. Tegelijkertijd verhoogden tumorcellen het niveau van PD‑L1, een oppervlakte‑eiwit dat T‑cellen kan uitschakelen door de PD‑1‑receptor te activeren, wat suggereert dat de tumoren zich verdedigden tegen deze nieuwe immuundruk.
Waarom PARP alleen niet genoeg is — en waar resistentie ontstaat
In navolging van de klinische praktijk kregen de muizen eerst een kuur gemcitabine en cisplatine, gevolgd door onderhoud met de PARP‑remmer olaparib. Deze volgorde verbeterde tumorcontrole en overleving vergeleken met alleen chemotherapie, wat bevestigt dat voorafgaande chemotherapie tumoren gevoeliger kan maken voor PARP‑remming. Geen enkele muis werd echter genezen: tumoren groeiden uiteindelijk terug tijdens PARP‑onderhoud. Resistente tumoren vertoonden een meer gedifferentieerd uiterlijk en sterk verhoogde niveaus van de ontwikkelingsregulator CDX2. Dit suggereert dat resistentie in dit model niet eenvoudigweg voortkomt uit herstel van het oorspronkelijke DNA‑hersteldefect, maar kan samenhangen met een verschuiving in de cellulaire identiteit van de tumor. CDX2 zou mogelijk als biomarker kunnen dienen om opkomende resistentie bij patiënten te signaleren.
Immunotherapie ontsluiten met de juiste volgorde
Immuuncheckpointmiddelen zoals anti‑PD1‑antilichamen hebben de behandeling van meerdere kankersoorten getransformeerd, maar alvleesklierkanker bleef grotendeels ongevoelig. In overeenstemming hiermee hielp anti‑PD1 (met of zonder een tweede checkpointmiddel, anti‑CTLA4) niet wanneer het werd gegeven aan onbehandelde BRCA2‑gemuteerde tumoren, en het voegde ook weinig toe wanneer het simpelweg aan PARP‑remmertherapie werd toegevoegd. Het beeld veranderde toen de volledige volgorde werd toegepast: eerst platina‑chemotherapie, daarna PARP‑remming plus anti‑PD1 als onderhoud. In deze opzet krompen de tumoren dieper en leefden de muizen langer dan bij chemotherapie plus PARP‑remmer of anti‑PD1 alleen. Het toevoegen van anti‑CTLA4 aan PARP‑onderhoud gaf niet dezelfde voordelen, wat suggereert dat de door chemotherapie geprimede tumoromgeving specifiek ontvankelijk is voor PD‑1‑blokkade. 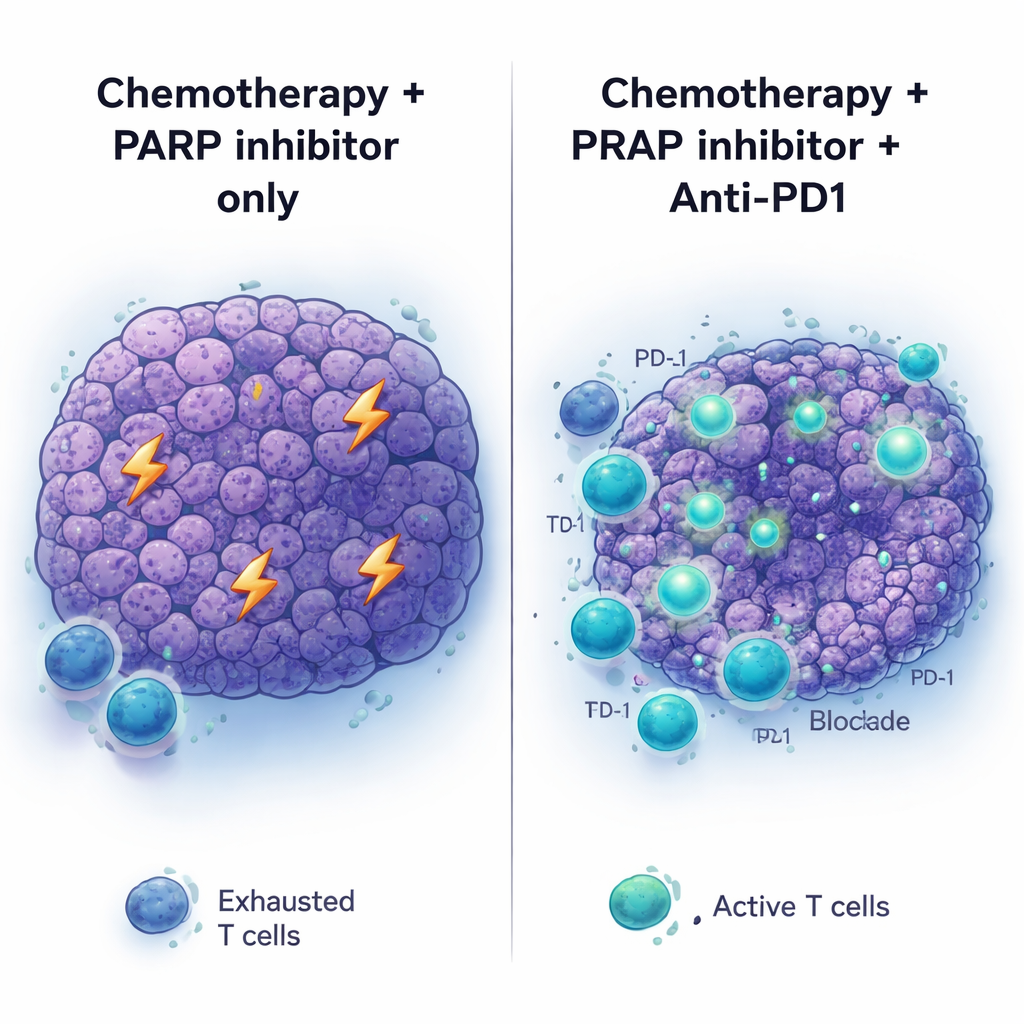
Wat dit kan betekenen voor toekomstige zorg
Samengevat pleit de studie ervoor dat bij BRCA‑gemuteerde alvleesklierkanker de volgorde en combinatie van therapieën sterk van belang zijn. Krachtige DNA‑beschadigende chemotherapie valt niet alleen tumorcellen direct aan, maar wekt ook een immuunreactie op, zelfs als die aanvankelijk verzwakt is door uitputting en PD‑L1‑verdediging. PARP‑remmers kunnen het voordeel verlengen maar zullen waarschijnlijk op zichzelf niet curatief zijn en kunnen tumoren sturen naar een resistente, CDX2‑hoge staat. Door anti‑PD1‑immunotherapie te stapelen op PARP‑onderhoud na platina‑chemotherapie, zou het mogelijk zijn deze kortstondig ontstoken, uitgeputte immuunsituatie om te zetten in een effectievere en duurzamere antitumorale reactie. Lopende klinische studies die PARP‑remmers combineren met immunotherapie bij BRCA‑gerelateerde alvleesklierkanker zullen cruciaal zijn om te bepalen of deze zorgvuldig getimede strategie kan leiden tot langere, betere levens voor patiënten.
Bronvermelding: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Trefwoorden: alvleesklierkanker, BRCA2‑mutatie, platina‑chemotherapie, PARP‑remmer, PD‑1‑immunotherapie