Clear Sky Science · nl
Indirubine-behandeling werd geassocieerd met modulatie van de PI3K/AKT- en MAPK-routes en inductie van apoptose en autophagie
Een nieuwe wending in de behandeling van baarmoederhalskanker
Baarmoederhalskanker blijft een van de belangrijkste oorzaken van kankerdoden bij vrouwen wereldwijd, en huidige behandelingen zoals chirurgie, chemotherapie en bestraling kunnen zwaar zijn en soms onvoldoende effectief bij gevorderde ziekte. Deze studie onderzoekt of indirubine, een natuurlijk verbinding afgeleid van een middel uit de traditionele Chinese geneeskunde, de groei van baarmoederhalskanker kan vertragen en kankercellen kan doden terwijl het werkt via bekende intracellulaire overlevingsschakelaars in tumoren. Voor lezers biedt het een inkijkje in hoe een oud middel mogelijk kan worden omgevormd tot een moderne, meer gerichte kankertherapie.
Waarom een plantaardig pigment de aandacht van wetenschappers trok
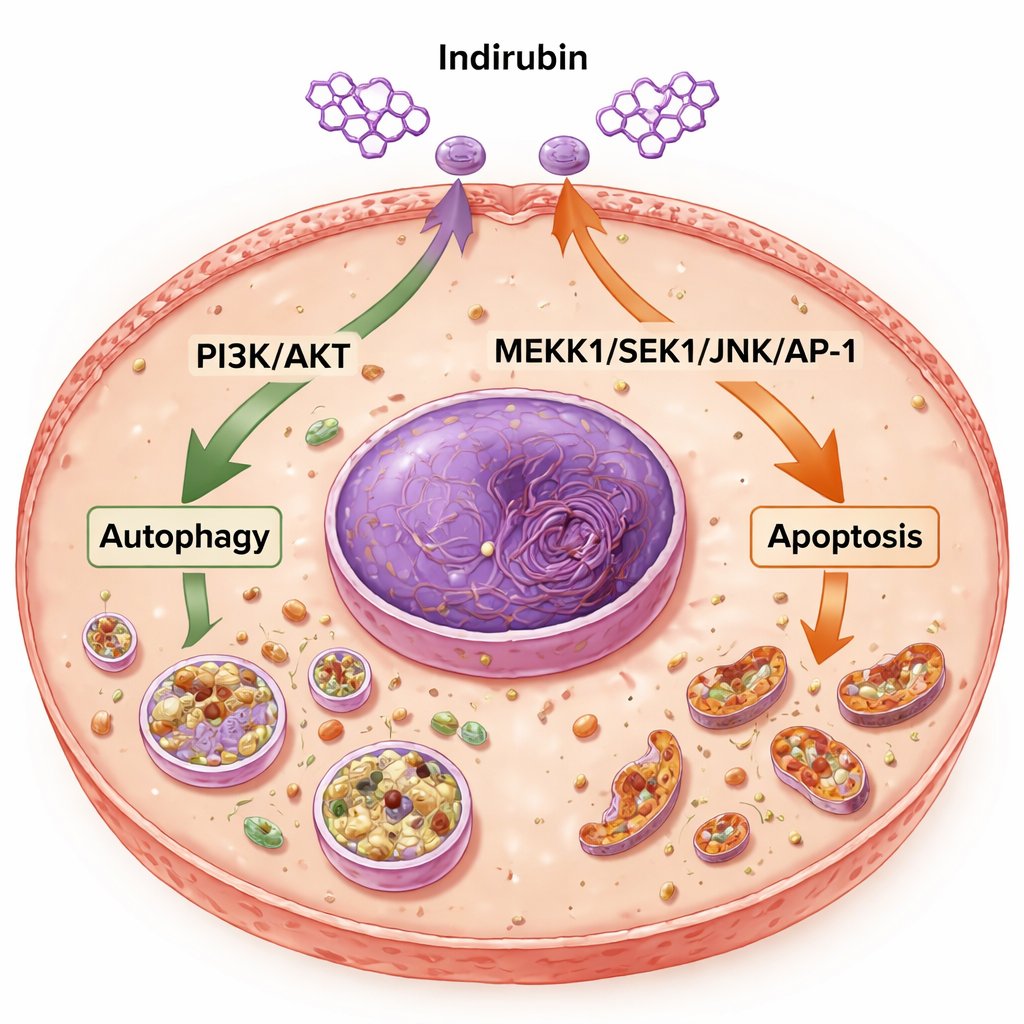
Indirubine is een pigment dat voorkomt in indigo naturalis, een bereiding die lang gebruikt wordt in de traditionele Chinese geneeskunde. Eerder onderzoek toonde aan dat het de groei van verschillende soorten kankercellen kan remmen, maar hoe het werkt bij baarmoederhalskanker was niet goed begrepen. De auteurs richtten zich op twee belangrijke controlesystemen in cellen. De ene is de PI3K/AKT-route, vaak beschreven als een groeien overlevings-"aan"-schakelaar in veel tumoren. De andere behoort tot de MAPK-familie van routes, specifiek een keten genaamd MEKK1/SEK1/JNK/AP-1, die helpt cellen te laten beslissen of ze zich aanpassen aan stress of afsterven. Door deze schakelaars te onderzoeken, hoopte het team te zien of indirubine baarmoederhalskankercellen van overleving kon afbrengen en naar zelfvernietiging kon duwen.
Indirubine testen in muizen en menselijke kankercellen
Om de effecten van indirubine te onderzoeken voerden de onderzoekers twee hoofdseries experimenten uit. Bij muizen implanteren zij baarmoederhalskankercellen onder de huid en behandelden de dieren met verschillende doses indirubine of met standaard chemotherapiemedicijnen. In het laboratorium behandelden ze HeLa-cellen — een goed vastgestelde baarmoederhalskankercellijn — met stijgende concentraties indirubine en maten vervolgens hoeveel cellen overleefden, hoeveel in geprogrammeerde celdood (apoptose) gingen, en hoe goed de cellen hun interne "zelfschoonmaak"-proces activeerden, bekend als autophagie. Ze volgden ook het gewicht van de muizen en hielden strikt rekening met dierenwelzijnsregels om te verzekeren dat eventuele antitumoreffecten niet simpelweg door algemene toxiciteit werden veroorzaakt.
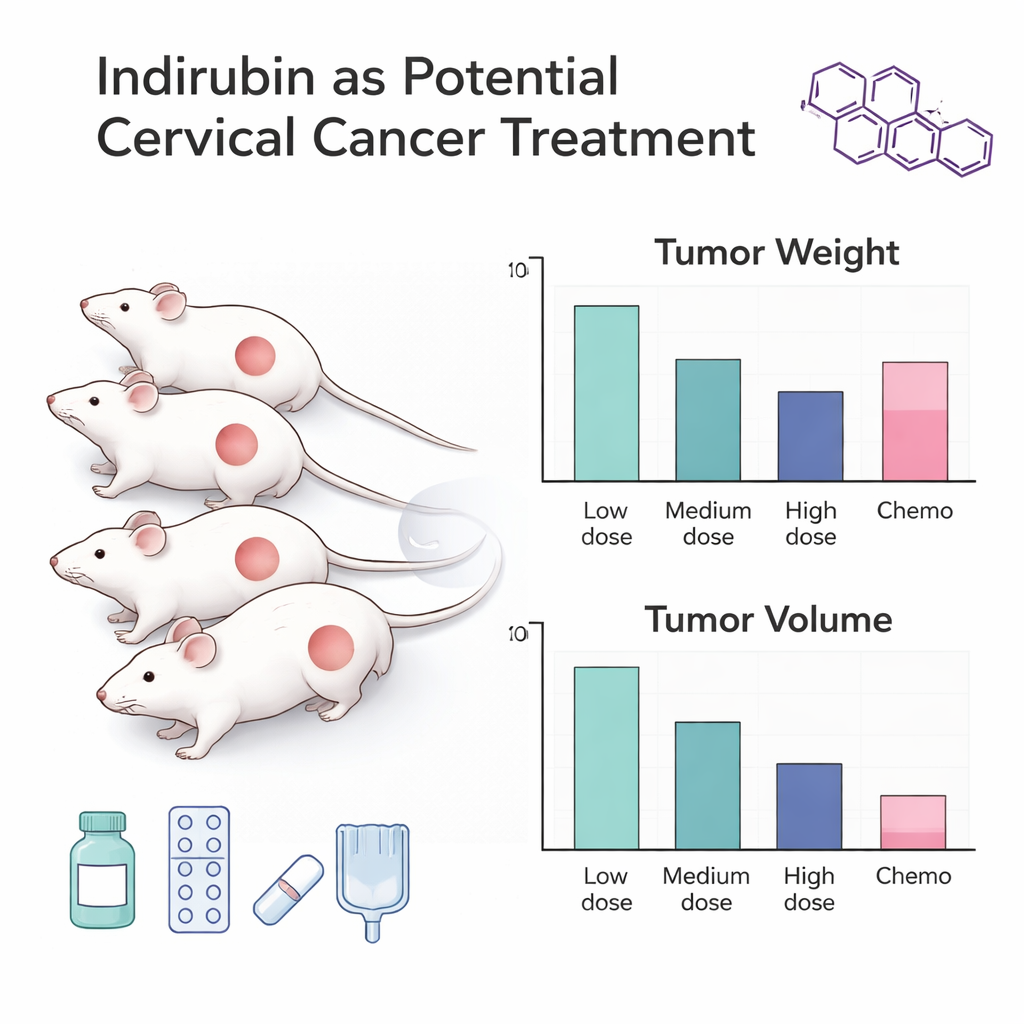
Tumoren vertragen en celsuïcide uitlokken
Bij muizen verkleinden tumoren duidelijk onder invloed van indirubine in een dosisafhankelijke manier: hogere doses leidden tot veel lichtere en kleinere tumoren, terwijl de dieren hun normale lichaamsgewicht behielden, wat suggereert dat het middel geen ernstige systemische schade veroorzaakte. In celkweek verminderde indirubine het aantal levende HeLa-cellen in de tijd en bij toenemende doses. Bij de hoogste geteste concentraties doodde indirubine meer baarmoederhalskankercellen dan standaard chemotherapieagentschappen zoals cisplatine en ifosfamide. Flowcytometrie, een techniek die cellen sorteert en telt, toonde aan dat indirubine-behandelde cellen veel vaker in vroege of late stadia van apoptose verkeerden, wat betekent dat de verbinding sterk aanmoedigde dat kankercellen gecontroleerd zelfvernietigden in plaats van door te delen.
De overlevingscircuits van de cel herschakelen
Dieper gravend toonde het team aan dat indirubine de balans van sleutelproteïnen die het cel lot bepalen veranderde. Het verhoogde markers van autophagie, wat aangeeft dat het recyclemechanisme van de cellen actiever was, terwijl het de niveaus van p62 verlaagde, een eiwit dat doorgaans afneemt wanneer dit proces op gang komt. Tegelijk dempte indirubine de activiteit van de PI3K/AKT-route — zowel op het niveau van genboodschappen als via verminderde fosforylering, het chemische "aan"-signaal op deze eiwitten. Het middel verlaagde ook de niveaus van BCL2, een eiwit dat celdood blokkeert, en verhoogde de niveaus van Bax, een pro-dood partner, waardoor de balans naar apoptose werd gekanteld. In tumorweefsels van muizen onderdrukte indirubine vergelijkbaar de MEKK1/SEK1/JNK/AP-1-route, wat suggereert dat het ook een andere stressrespons-route afzwakte die tumoren gebruiken om te overleven en zich te verspreiden.
Wat dit zou kunnen betekenen voor toekomstige patiënten
Voor niet-specialisten is de belangrijkste boodschap dat indirubine, een verbinding geworteld in traditionele geneeskunde, in staat was de groei van baarmoederhalskanker te vertragen en kankercellen te stimuleren tot zelfreiniging en zelfvernietiging door krachtige interne overlevingsschakelaars uit te schakelen. Het deed dit zowel in diermodellen als in gekweekte cellen, en het deed dit zonder duidelijke schade bij de muizen. Hoewel deze bevindingen nog preklinisch zijn en ver van routinematig gebruik in de kliniek, vormen ze een wetenschappelijke basis voor vervolgonderzoek en uiteindelijk menselijke proeven. Als toekomstig onderzoek de veiligheid en werkzaamheid bevestigt, zouden indirubine of verwante verbindingen op een dag een plaats kunnen krijgen in het arsenaal van gerichte behandelingen die de therapie van baarmoederhalskanker preciezer en minder belastend maken.
Bronvermelding: Xie, X., Liu, C., Liu, X. et al. Indirubin treatment was associated with modulation of the PI3K/AKT and MAPK pathways and induction of apoptosis and autophagy. Sci Rep 16, 5155 (2026). https://doi.org/10.1038/s41598-026-35382-z
Trefwoorden: baarmoederhalskanker, indirubine, traditionele Chinese geneeskunde, celsignaleringsroutes, apoptose en autophagie