Clear Sky Science · nl
Ontregeling van intracellulaire ijzerhomeostase door mitochondriale disfunctie geassocieerd met onderdrukking van ATP13A2-expressie
Waarom ijzer binnen hersencellen ertoe doet
De ziekte van Parkinson is vooral bekend om tremoren en stijve bewegingen, maar diep in de aangetaste hersencellen speelt zich een ander schouwspel af: ijzer, een essentieel metaal, hoopt zich op waar het niet thuishoort. Deze studie stelt een eenvoudige maar belangrijke vraag: hoe ontstaat die ijzerophoping, en hoe kan dat schade toebrengen aan de kleine energiecentrales en recyclingcentra binnen neuronen? Door deze vraag te beantwoorden, biedt het werk aanwijzingen waarom bepaalde hersengebieden degenereren bij Parkinson en verwante aandoeningen, en wijst het op nieuwe behandelrichtingen die verder gaan dan alleen het vervangen van dopamine.
Een nadere blik op een zeldzame genetische aanwijzing
De onderzoekers richten zich op een zeldzame erfelijke vorm van de ziekte van Parkinson, PARK9 genoemd, veroorzaakt door defecten in een gen dat ATP13A2 heet. Dit gen codeert voor een eiwit dat in lysosomen zit, de afvalverwerkende en recycleende compartimenten van de cel. Mensen met ATP13A2-mutaties kunnen ook een aandoening ontwikkelen die gekenmerkt wordt door ijzerafzettingen in de hersenen. Die koppeling maakte ATP13A2 tot een ideaal startpunt om te bestuderen hoe de ijzerbalans ontspoort. Met behulp van een humaan neuron-achtig cellijn dat te veel van het Parkinson-eiwit alfa-synucleïne produceert, gebruikten de onderzoekers korte RNA-fragmenten om ATP13A2 te onderdrukken en volgden ze vervolgens hoe ijzer, energieproductie en celgezondheid veranderden.
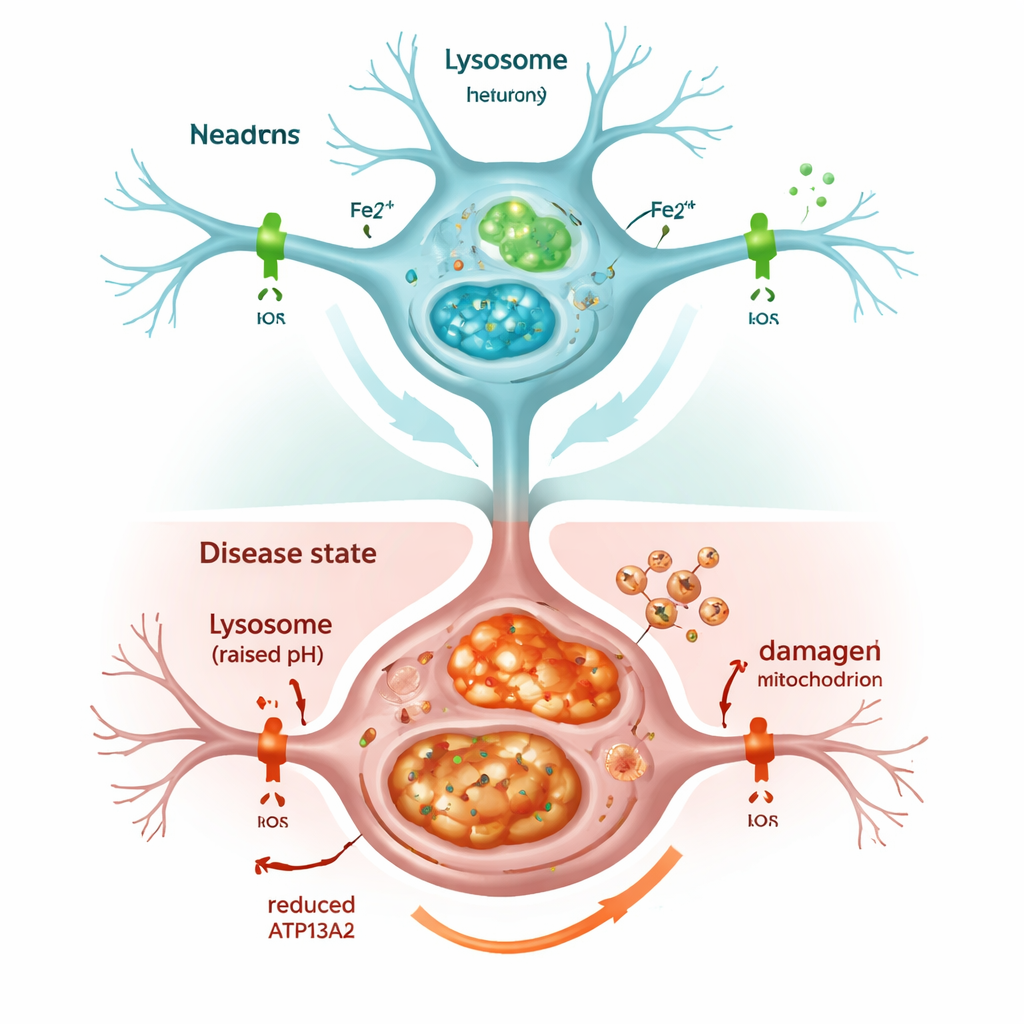
Wanneer het recyclingsysteem van de cel hapert
Het uitschakelen van ATP13A2 verzwakte lysosomen snel. Hun interne zuurgraad, cruciaal voor het afbreken van afvalstoffen, daalde, en markeringsstoffen van het opruimproces autophagie stapelden zich op in plaats van te worden afgebroken. Daardoor liep ook alfa-synucleïne op, wat echo’s van wat in Parkinson-hersenen wordt gezien weerspiegelt. De cellen vertoonden bovendien meer ijzer in het algemeen, en in het bijzonder meer van de chemisch actieve vorm Fe2+ binnen zowel lysosomen als mitochondriën. De cel reageerde door meer ferritine te produceren, een eiwit dat ijzer opslaat, maar dat bleek niet voldoende om problemen te voorkomen: de overbelaste mitochondriën produceerden overtollige reactieve zuurstofmoleculen en de levensvatbaarheid van de cellen nam af. Behandeling van de cellen met een ijzerbindend medicijn, vergelijkbaar met sommige klinisch gebruikte middelen, verminderde deze oxidatieve stress en herstelde gedeeltelijk de celoverleving, wat benadrukt dat overtollig ijzer zelf een belangrijke veroorzaker van schade was.
Ijzersensoren luisteren niet meer naar het metaal
Normaal gesproken hebben cellen een terugkoppelingssysteem dat merkt wanneer ijzerniveaus stijgen en daarop reageert door de ijzerinvoer te verminderen. Een eiwit genaamd IRP2 voelt ijzer aan, deels via een heme-afhankelijke signaalstroom afkomstig van mitochondriën, en past vervolgens de productie aan van ijzerdragende eiwitten op het celoppervlak. In de ATP13A2-deficiënte cellen faalde deze veiligheidsvoorziening. Transporters die ijzer de cel in brengen bleven hoog, ook al was het ijzergehalte al verhoogd. De IRP2-eiwitniveaus veranderden amper, en het toevoegen van extra ijzer van buitenaf zette niet zijn normale afbraak in gang. Het team bracht deze tekortkoming terug tot de mitochondriën: beschadigde mitochondriën ademden minder efficiënt, vertoonden tekenen van gebrekkige kwaliteitscontrole (mitofagie), en, cruciaal, verloren het vermogen om heme te maken, het ijzerhoudende molecuul dat IRP2 helpt ijzer waar te nemen. Zonder voldoende heme ontving IRP2 het signaal “te veel ijzer” niet en bleef ijzer ongestoord naar binnen stromen.
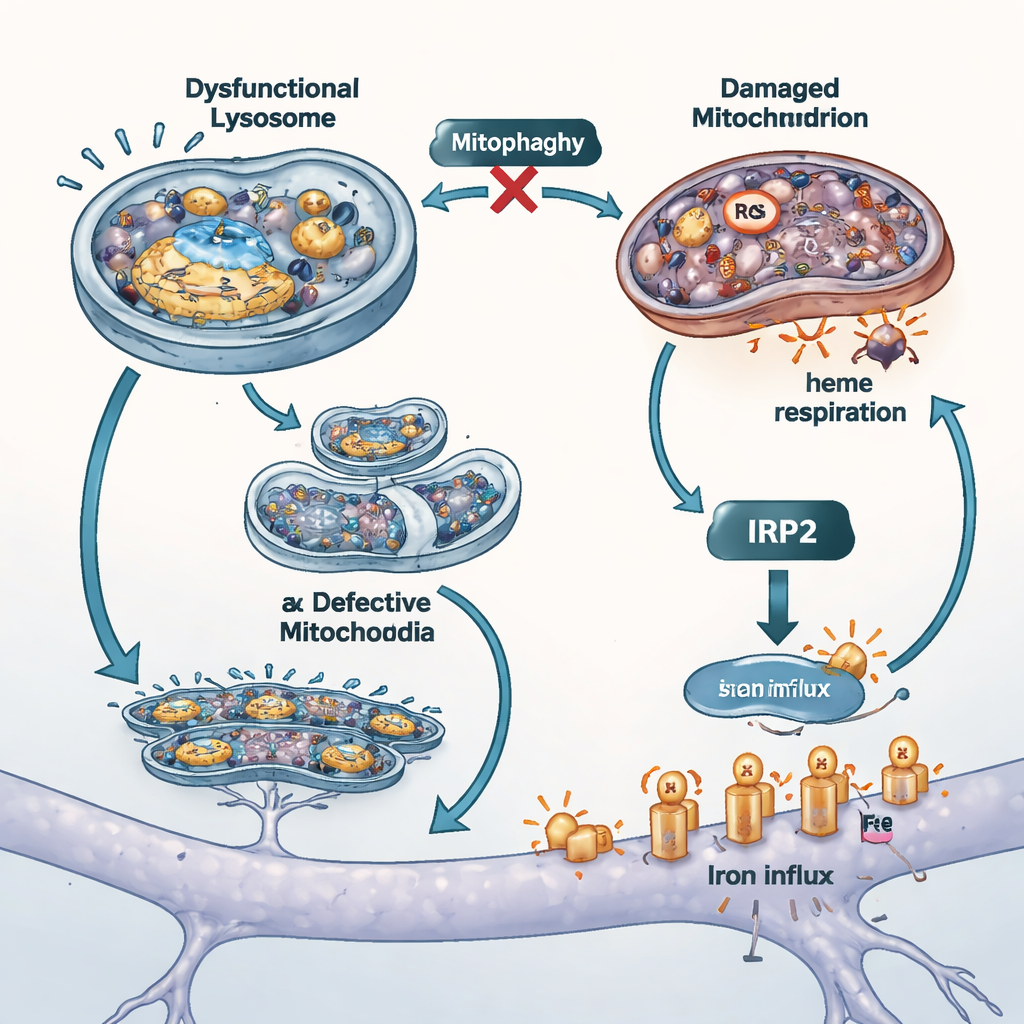
De ijzertap dichtdraaien en andere modellen testen
Om te onderzoeken hoeveel deze ongecontroleerde ijzerinflux bijdroeg aan celbeschadiging, blokkeerden de wetenschappers twee belangrijke ijzeropnameroutes. Ze gebruikten een ijzervrije versie van het bloedproteïne transferrine om te concurreren voor één invoer, en een kleine stof om de activiteit van een andere transporteur, DMT1, te remmen. Beide ingrepen verlaagden het totale en vrije ijzer in de cellen, verminderden mitochondriale oxidatieve stress en verbeterden de overleving, wat suggereert dat oppervlaktespecifieke ijzerkanalen belangrijke versterkers van schade zijn wanneer ATP13A2 verloren gaat. De onderzoekers herhaalden ook cruciale experimenten in cellen die een andere Parkinson-gekoppelde genfunctie, PINK1, misten, dat bekendstaat om het verstoren van mitofagie. Deze cellen toonden dezelfde combinatie van ijzerophoping en verzwakte hemeproductie, wat de gedachte ondersteunt dat mitochondriale kwaliteitscontrole en ijzerbalans nauw met elkaar verweven zijn in verschillende vormen van de ziekte.
Wat dit betekent voor Parkinson en toekomstige behandelingen
Kort gezegd schetst de studie een vicieuze cirkel. Wanneer ATP13A2 wordt onderdrukt, slagen lysosomen er niet in beschadigde onderdelen te verwijderen, waaronder defecte mitochondriën. Deze verzwakte mitochondriën produceren vervolgens minder energie en minder heme, waardoor het ijzer-sensorsysteem van de cel verzwakt raakt. IJzer blijft via superficiale transporters binnenstromen, hoopt zich op in kwetsbare compartimenten en voedt toxische reacties die de mitochondriën verder beschadigen. In de loop van de tijd kan deze lus helpen verklaren waarom bepaalde neuronen afsterven bij Parkinson en aanverwante hersenaandoeningen met ijzerophoping. De bevindingen suggereren dat toekomstige therapieën niet alleen overtollig ijzer zouden kunnen verwijderen, maar ook de juiste lysosomale functie, mitochondriale kwaliteitscontrole en hemeproductie herstellen — de oorzaak aanpakken in plaats van alleen het metaal nadien op te ruimen.
Bronvermelding: Murakami, T., Ohuchi, K., Kiuchi, M. et al. Disruption of intracellular iron homeostasis through mitochondrial dysfunction associated with suppression of ATP 13A2 expression. Sci Rep 16, 5007 (2026). https://doi.org/10.1038/s41598-026-35368-x
Trefwoorden: Ziekte van Parkinson, hersenijzer, mitochondriën, lysosomen, heme-synthese