Clear Sky Science · nl
Onderzoek naar functionele hot-spotresiduen van een enzym door realtime monitoring van de enzymatische reactie met NMR en computationele benaderingen
Waarom dit belangrijk is voor toekomstige antivirale middelen
Favipiravir is een pil die al wordt gebruikt tegen influenza en getest is voor COVID-19, maar het bestrijdt virussen niet in de vorm waarin we het innemen. Onze eigen cellen moeten het eerst omzetten in een actieve, virusremmende molecule. Deze studie ontleedt, bijna atoom voor atoom, hoe één menselijk enzym een cruciale activeringsstap uitvoert en welke kleine onderdelen van het enzym als “hot spots” fungeren die bepalen hoe snel en hoe goed het geneesmiddel geactiveerd wordt. Inzicht in deze details kan het ontwerp van volgende generatie antivirale middelen sturen, die zowel krachtiger als voorspelbaarder in patiënten zijn.
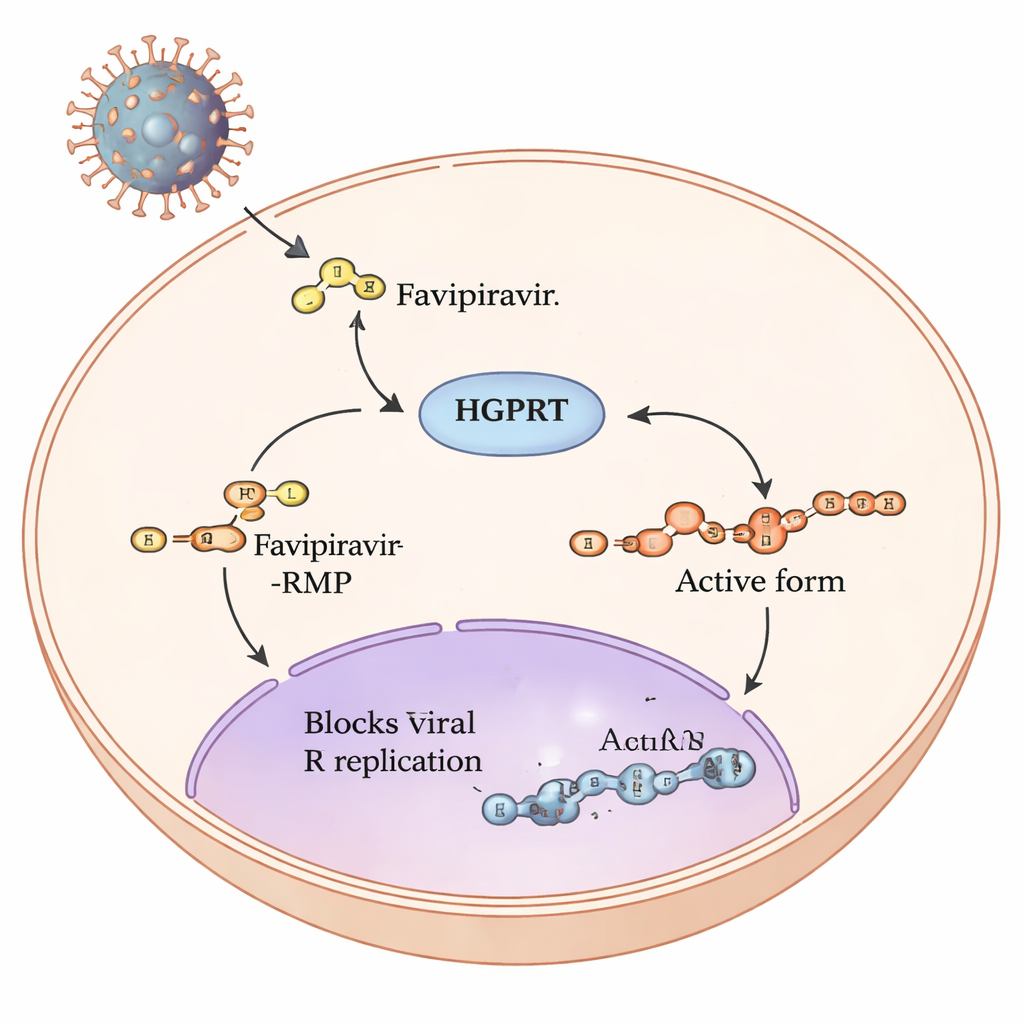
De reis van een prodrug binnen onze cellen
Favipiravir is een zogeheten prodrug: zodra het menselijke cellen binnendringt, wordt het door een reeks chemische stappen omgevormd tot een vorm die het kopieermechanisme van RNA‑virussen zoals influenza en SARS‑CoV‑2 kan blokkeren. De eerste en traagste stap in dit pad wordt uitgevoerd door een menselijk enzym genaamd hypoxanthine‑guanine phosphoribosyltransferase, of HGPRT. HGPRT voegt een kleine suiker‑fosfaatgroep toe aan favipiravir, waardoor favipiravir‑RMP ontstaat. Pas na deze stap kunnen andere enzymen de volledig actieve triphosfaatvorm opbouwen die rechtstreeks interfereert met het virale RNA‑polymerase. Omdat deze eerste door HGPRT gedreven stap als een knelpunt werkt voor hoeveel actief geneesmiddel er wordt geproduceerd, wilden de auteurs vaststellen welke onderdelen van HGPRT het belangrijkst zijn voor de verwerking van favipiravir.
Chemie in realtime volgen met NMR
Uniek is dat favipiravir een fluoratoom bevat dat zich in een magneetveld gedraagt als een kleine radiosignaalgever. Het team maakte hiervan gebruik door fluor‑19 nucleaire magnetische resonantie (NMR) spectroscopie toe te passen om in realtime te volgen hoeveel favipiravir en hoeveel favipiravir‑RMP aanwezig waren in een reageerbuis terwijl de reactie vorderde. Omdat alleen het geneesmiddel fluor bevat, zijn de NMR‑signalen schoon en eenvoudig te volgen. Door herhaaldelijk spectra op te nemen gedurende 12 uur konden de onderzoekers het verdwijnen van het begingeneesmiddel en het opkomen van het gewijzigde product volgen, en vervolgens standaard kinetische grootheden afleiden zoals hoe snel de reactie verloopt en hoe sterk het enzym ogenschijnlijk aan het geneesmiddel bindt.
Sleutelposities in het enzym afstemmen
Eerdere röntgenopnames van HGPRT gebonden aan favipiravir‑RMP suggereerden een handvol aminozuren die het geneesmiddel in een zakje omhullen. Het nieuwe werk test drie van deze posities door precieze eênletterwijzigingen in het eiwit aan te brengen en elk gemuteerd enzym met het natuurlijke te vergelijken. Eén verandering, aangeduid T138A, maakte het enzym onverwacht ongeveer vier tot zes keer sneller in het omzetten van favipiravir, ondanks dat daarmee een chemische groep werd verwijderd die verondersteld was het geneesmiddel vast te houden. Een tweede wijziging, K140M, vertraagde de reactie licht en verzwakte de schijnbare binding iets. Een derde wijziging, D193N, schafte de capaciteit van het enzym om favipiravir‑RMP te maken volledig af, hoewel het gewijzigde eiwit nog wel geproduceerd kon worden en het product kon binden. Samen tonen deze resultaten aan dat niet alle contactpunten gelijk zijn: sommige fungeren als subtiele snelheidsregelaars, terwijl andere essentiële schakelaars zijn.
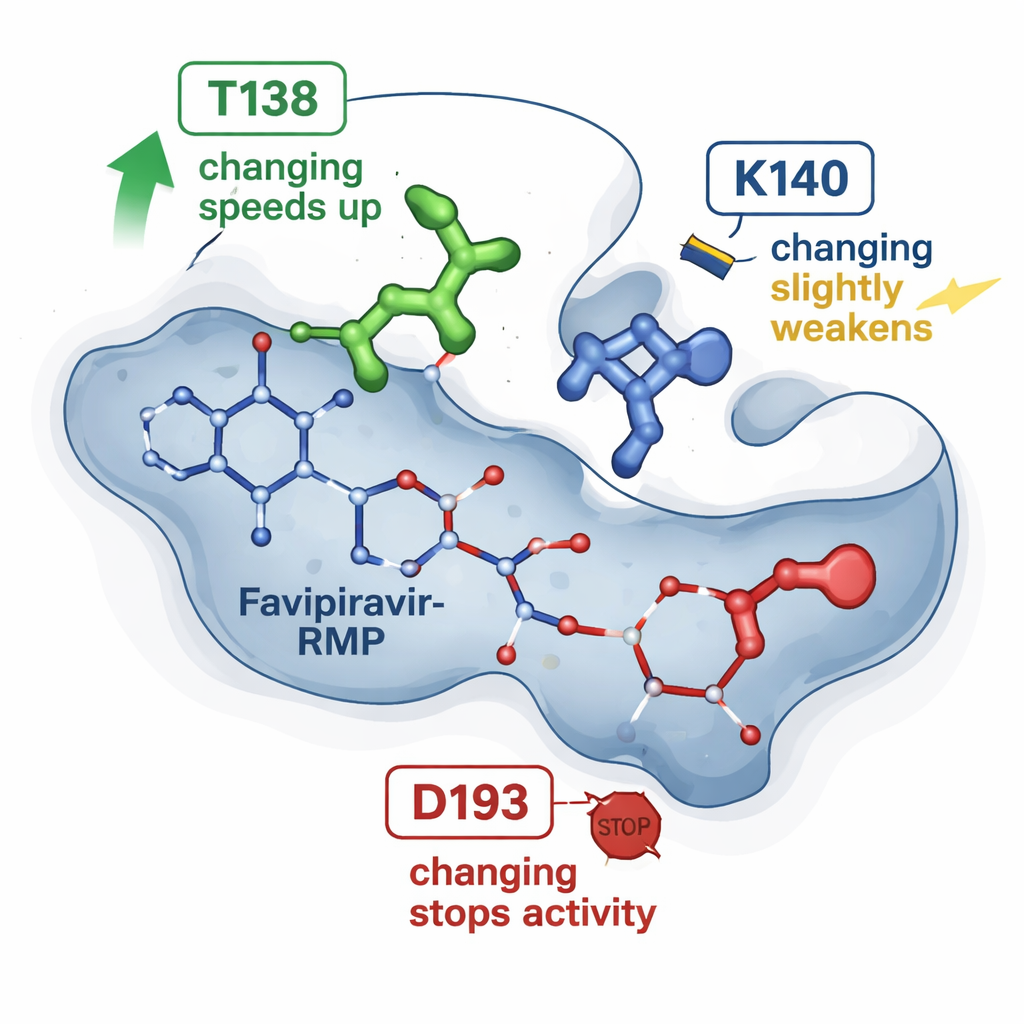
De bewegende onderdelen op een computer simuleren
Om verder te kijken dan statische structuren wendden de onderzoekers zich tot moleculaire simulaties. Uitgaande van de bekende driedimensionale structuur van HGPRT met favipiravir‑RMP, gebruikten ze gevestigde computationele hulpmiddelen om te schatten hoe sterk het geneesmiddel in elk mutant bindt en om veel korte moleculaire dynamicasimulaties uit te voeren. Deze simulaties volgen hoe de atomen trillen en elkaar beïnvloeden over tientallen nanoseconden. De berekeningen kwamen overeen met de trends afgeleid uit NMR: het T138A‑variant hield over het algemeen favipiravir‑RMP gunstiger vast maar vertoonde ook episoden waarin het geneesmiddel naar een “ontsnappings”pad bewoog, geleid door een ander residu (K140) dat de fosfaatgroep tijdelijk verankert vóór vrijkomst. Daarentegen hield de D193N‑variant het product nog vast, maar faalde waarschijnlijk in een eerdere katalytische stap die een magnesiumion vereist, wat verklaart waarom het activiteit verloor ondanks stabiele binding.
Een routekaart voor slimmer antiviraal ontwerp
Door realtime NMR‑metingen te combineren met gedetailleerde computermodellen, brengt deze studie de functionele hot spots in HGPRT in kaart die bepalen hoe efficiënt favipiravir wordt geactiveerd. Voor niet‑specialisten is de kernboodschap dat onze eigen enzymen sterk kunnen beïnvloeden hoeveel actief antiviraal middel zich in cellen ophoopt, en dat het aanpassen van zowel de vorm van het geneesmiddel als de pocket van het enzym dat resultaat dramatisch kan veranderen. De hybride strategie van de auteurs biedt een algemeen stappenplan om te onderzoeken hoe andere medicijnen met hun doeleiwitten interageren, wat mogelijk de ontwikkeling van nieuwe antivirale verbindingen kan versnellen die beter aansluiten op de activatiemechanismen van het lichaam.
Bronvermelding: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
Trefwoorden: favipiravir, activering van antivirale middelen, HGPRT-enzym, NMR-spectroscopie, geneesmiddelontwerp