Clear Sky Science · nl
Onzekerheid in voorspellingen van centraalkanaalstenose kwantificeren in SpineNet met conformal prediction
Waarom slimmere wervelkolomscans ertoe doen
Lage rugpijn brengt elk jaar miljoenen mensen naar de huisarts, en MRI-scans van de wervelkolom zijn een belangrijk hulpmiddel om te bepalen wie een operatie nodig heeft en wie conservatiever kan worden behandeld. Steeds vaker helpen computers radiologen door automatisch in te schatten hoe vernauwd het wervelkanaal is — een aandoening die centraal kanaalstenose wordt genoemd. Maar artsen vragen terecht een cruciale vraag: hoe zeker is de computer van zijn antwoord? Deze studie laat zien hoe je een black-box wervelkolom-AI-systeem, genaamd SpineNet, kunt ombouwen zodat het niet alleen zegt wat het denkt, maar ook hoe onzeker het is — en zo een eerlijkere en klinisch nuttigere second opinion levert.
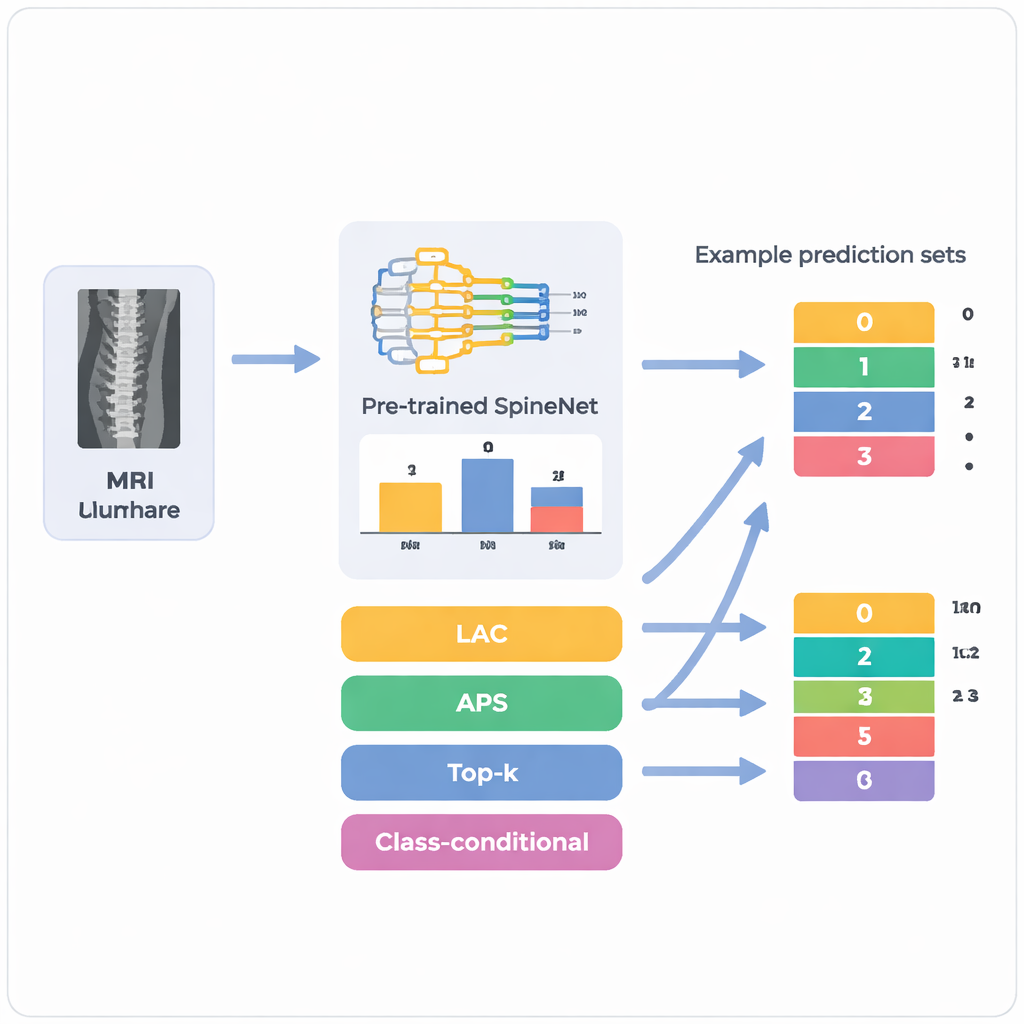
Van één gok naar eerlijke reeksen
De meeste kunstmatige-intelligentiesystemen die in de geneeskunde worden gebruikt, gedragen zich als zeer zelfverzekerde studenten die altijd één antwoord geven, ook wanneer ze onzeker zijn. SpineNet bekijkt bijvoorbeeld MRI-scans van de lumbale wervelkolom en kent elk schijfniveau één van vier gradaties toe — normaal, mild, matig of ernstig stenose. Wat het niet zegt, is wanneer meer dan één gradatie plausibel lijkt. De auteurs passen een statistisch kader toe dat conformal prediction heet; dat legt zich over een bestaand model heen en zet de ruwe confidentiescores om in kleine sets met mogelijke antwoorden. In plaats van simpelweg “mild” te zeggen, kan het systeem “mild of matig” aangeven en er een garantie aan koppelen dat, over veel gevallen, de werkelijke gradatie in dat bereik ligt in ten minste 85–95% van de gevallen, afhankelijk van hoe strikt clinici willen zijn.
De aanpak testen op echte patiënten
Het team begon met 340 oudere volwassenen met symptomen van lumbale spinale stenose die MRI hadden ondergaan in een Zwitsers ziekenhuis. SpineNet classificeerde automatisch tot vijf wervelniveaus per persoon, wat in totaal 1.689 schijfniveaus opleverde. Voor elk niveau haalden de onderzoekers de interne waarschijnlijkheden van het model voor de vier stenosegradaties op en pasten vervolgens vier varianten van conformal prediction toe. Ze splitsten de data herhaaldelijk duizend keer in calibratie- en testsubsets en varieerden hoeveel fout ze bereid waren te tolereren. Deze intensieve herbemonstering liet hen niet alleen zien hoe vaak de werkelijke gradatie binnen elke predictieset viel, maar ook hoe groot die sets doorgaans waren, zowel in het algemeen als voor elke ernstgraad afzonderlijk.
De gulden middenweg vinden tussen veiligheid en bruikbaarheid
Alle vier methoden konden worden afgestemd zodat hun algemene dekkingsgraad overeenkwam met het gewenste doel, maar ze verschilden sterk in hoe informatief ze waren. Een eenvoudige “top-k”-methode bereikte perfecte dekking bij strikte instellingen door bijna altijd alle vier gradaties te noemen, wat wiskundig veilig is maar in de praktijk bijna nutteloos. Een ander paar methoden, ontworpen om de predictieset adaptief te laten groeien, worstelde vaak met de lastige matige en ernstige gevallen en miste de gewenste dekking ondanks dat ze grote sets produceerden. De duidelijke winnaar was een klasse-conditionele methode die voor elke gradatie een aparte onzekerheidsdrempel leert. Die raakte betrouwbaar de gevraagde dekking terwijl de predictiesets zo klein mogelijk bleven — vaak slechts één of twee gradaties voor veelvoorkomende normale en milde gevallen, en alleen iets grotere sets voor minder frequente matige en ernstige stenose, waar menselijke experts zelf ook vaak van mening verschillen.
Waar het model moeite mee heeft in de wervelkolom
Door wervel voor wervel te kijken toonden de auteurs aan dat de onzekerheid van het systeem overeenkomt met klinische moeilijkheid in de praktijk. In hogere lumbale niveaus, waar gevallen meestal normaal of licht vernauwd zijn, waren de predictiesets klein en betrouwbaar. Op niveaus zoals L3/L4 en L4/L5, waar ernstige vernauwing vaker voorkomt maar nog steeds relatief zeldzaam is, nam de onzekerheid toe: predictiesets voor ernstige gevallen waren groter en de dekking variabeler. Dit weerspiegelt zowel de ongelijke verdeling van de aandoening als het feit dat het onderliggende SpineNet-model minder nauwkeurig is voor milde en matige gradaties dan voor duidelijk normale of duidelijk ernstige gevallen. Belangrijk is dat de conformale laag die zwakte blootlegt in plaats van te verbergen, en precies die gevallen markeert waarin een radioloog extra voorzichtig zou moeten zijn.

Wat dit betekent voor patiënten en clinici
Voor patiënten vervangt het werk de radioloog niet; het maakt geautomatiseerde hulpmiddelen betrouwbaarder. In plaats van het oordeel van een spine-AI als alles-of-niets te accepteren, kunnen clinici nu zien wanneer het algoritme op stevig terrein staat en wanneer het tussen aangrenzende gradaties aarzelt. Die transparantie maakt het makkelijker te beslissen wanneer op het model te vertrouwen, wanneer een tweede mening gewenst is en hoe beeldvorming tegen symptomen moet worden afgewogen bij het bespreken van chirurgie. Omdat de conformale predictielaag aan veel bestaande systemen kan worden toegevoegd zonder ze opnieuw te trainen, biedt deze aanpak een praktische weg naar AI die niet alleen spine-MRI’s leest, maar ook haar eigen grenzen kent — en die duidelijk communiceert.
Bronvermelding: Cina, A., Monzon, M., Galbusera, F. et al. Quantifying central canal stenosis prediction uncertainty in SpineNet with conformal prediction. Sci Rep 16, 4963 (2026). https://doi.org/10.1038/s41598-026-35343-6
Trefwoorden: spinale stenose, medische AI, MRI-beelden, schatting van onzekerheid, conformal prediction