Clear Sky Science · nl
Geïnformeerde ruimtelijk bewuste patronen voor gemultiplexte immunofluorescentiegegevens
Waarom de buurt van tumorcellen ertoe doet
Pancreaskanker behoort tot de dodelijkste vormen van kanker, deels omdat tumoren zich bevinden in een complexe “buurt” van immuun- en ondersteunende cellen die de kanker kunnen bestrijden of juist helpen verbergen. Deze studie introduceert een nieuwe manier om de ruimtelijke ordening van die cellen in microscoopbeelden te lezen, en onthult hoe het immuunsysteem zich anders gedraagt in agressieve pancreatische ductale adenocarcinomen (PDAC) vergeleken met de voorstadiaachtige intraductale papillair-mucineuze neoplasie (IPMN). Het begrijpen van deze verborgen patronen kan wijzen op betere diagnostiek en slimmer, gerichter behandelaanpak.
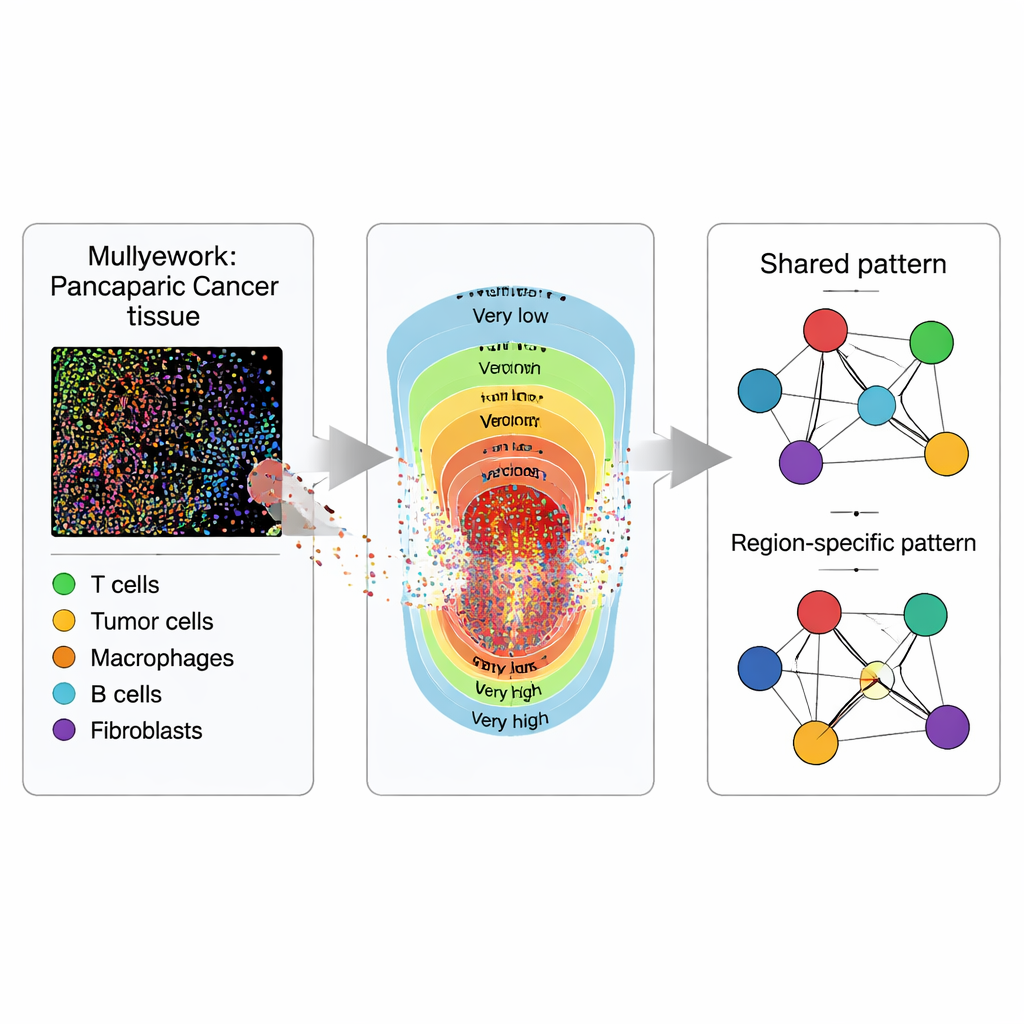
Weefsels zien als kaarten, niet alleen als afbeeldingen
In plaats van een tumorplakje als een vlak beeld te behandelen, beschouwen de onderzoekers het als een kaart vol punten. Met gemultiplexte immunofluorescentie Kleuren zij weefselmonsters van 119 PDAC- en 53 IPMN-patiënten zodat verschillende celtypen in verschillende kleuren oplichten. Gespecialiseerde software zet elke zichtbare cel om in een stip met coördinaten en een label: tumor (epitheliale) cellen, meerdere typen T-cellen die kunnen aanvallen of immuunreacties reguleren, en antigeen-presenterende cellen die tumorfragmenten aan T-cellen tonen. De kernvraag is niet alleen hoeveel van elk celtype aanwezig is, maar waar ze zich ten opzichte van elkaar bevinden in het weefsel.
De tumor opdelen in zones
Om vast te leggen hoe tumoren van het centrum naar buiten veranderen, wordt elk weefselmonster opgedeeld in vijf zones op basis van hoe dicht opeengepakt de tumorcellen zijn, van “zeer laag” tot “zeer hoog” tumorintensiteitsniveau. Deze zones representeren een gradiënt van tumorbelasting en cellulaire dichtheid die pathologen vaak onder de microscoop zien maar zelden kwantificeren. Binnen elke zone schat het team gladde “intensiteitskaarten” voor elk celtype, waarbij verspreide stippen in wezen worden omgezet in continue warmtekaarten van waar elk celtype neigt te clusteren. Deze zonering laat hen niet alleen cellulaire interacties in het algemeen vergelijken, maar ook hoe die interacties verschuiven van schaars naar dichtbevolkte tumorgebieden.
Celbuurten omzetten in netwerken
Vervolgens vertalen de onderzoekers de ruimtelijke patronen naar netwerken, waarbij elk celtype een knooppunt is en verbindingen aangeven hoe sterk twee celtypen de neiging hebben samen voor te komen, rekening houdend met alle andere typen. Met een Bayesiaans statistisch kader dat ze ISPat (Informed Spatially aware Patterns) noemen, scheiden ze kenmerken die in alle zones gedeeld worden van die zonespecifiek zijn. ISPat kan ook voorafgaande biologische kennis inbrengen wanneer die beschikbaar is, wat helpt om schattingen te stabiliseren in complexe gegevens. Simulatie-experimenten tonen dat ISPat bekende patronen betrouwbaar kan terugvinden en dat dit veel sneller gaat dan traditionele methoden, waardoor het praktisch toepasbaar is voor grootschalige beeldstudies.
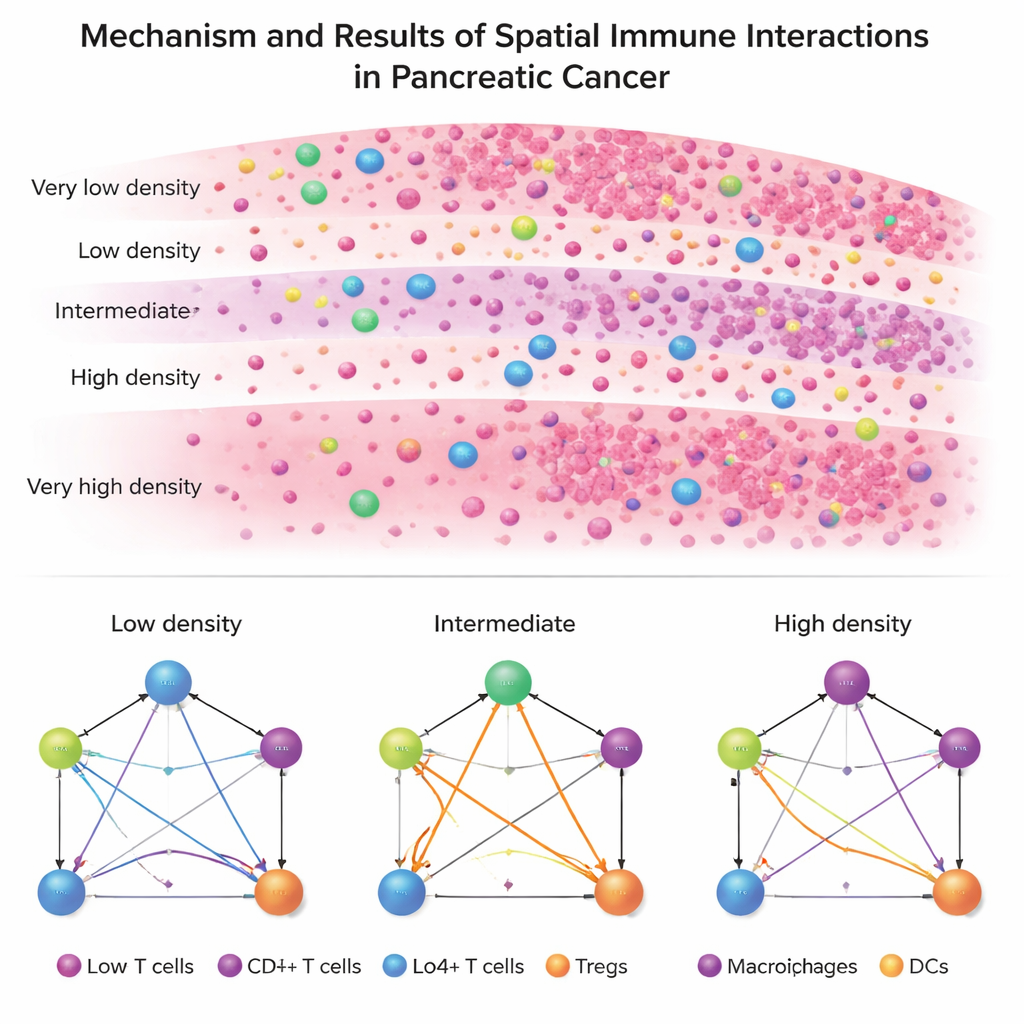
Twee ziekten, twee immuunarchitecturen
Wanneer ze ISPat toepassen op echte patiëntgegevens, ontstaat een opvallend contrast tussen PDAC en IPMN. PDAC vertoont een starre, uniforme immuunarchitectuur: in vrijwel alle zones laten tumorcellen, helper-T‑cellen, cytotoxische (killer) T‑cellen, regulatoire T‑cellen en antigeen‑presenterende cellen bijna hetzelfde patroon van onderlinge relaties zien. Dit wijst op een stabiele, ingesleten immunosuppressieve omgeving die moeilijk te doorbreken is. Daarentegen toont IPMN veel meer variatie van zone tot zone, vooral in hoe regulatoire T‑cellen verbindingen met andere immuuncellen vormen. In IPMN vertonen zones met een middelhoog dichtheidsniveau—noch volledig vol met tumorcellen, noch vrijwel tumorvrij—de meest ingrijpende herschikking van immuuninteracties.
Hotspots voor immuunontwijking en therapie
Dieper gravend identificeert de studie specifieke paren van celtypen waarvan de interacties consequent verschillen tussen PDAC en IPMN, met name in die zones met middeldichtheid. Veel van deze verschillen betreffen regulatoire T‑cellen, die immuuraanvallen kunnen afremmen, en antigeen‑presenterende cellen en killer T‑cellen, die anti-tumorreacties opstarten en uitvoeren. Opmerkelijk is dat interacties die antigeenpresentatie en directe tumorvernietiging aansturen, evenals die welke immuunsuppressie bekrachtigen, het meest sterk uiteenlopen in deze overgangsgebieden, niet in de meest extreme tumorgedeeltes. Dit patroon suggereert dat het beslissende strijdperk voor immuuncontrole ligt in de zones waar tumor en immuunsysteem nog actief onderhandeling voeren.
Wat dit betekent voor patiënten
Voor niet‑specialisten is de conclusie dat waar cellen zich bevinden in een tumor even belangrijk is als welke cellen er zijn. PDAC lijkt een stabiele, onderdrukkende immuun“indeling” vast te leggen, terwijl het immuunspectrum van IPMN flexibeler en regiogebonden blijft. Deze ruimtelijke vingerafdrukken zouden biomarkers kunnen worden om gevaarlijke tumoren te onderscheiden van voorkankerachtige laesies en om te voorspellen welke patiënten baat kunnen hebben bij specifieke immunotherapieën. Het ISPat‑kader biedt een algemeen hulpmiddel om dergelijke ruimtelijke codes in vele ziekten te lezen, en ondersteunt een toekomst waarin kankerbehandeling niet alleen wordt gestuurd door genetica en celtypen, maar ook door de fijnmazige geografie van cellen binnen de tumor van elke patiënt.
Bronvermelding: Bhadury, S., Peruzzi, M., Acharyya, S. et al. Informed spatially aware patterns for multiplexed immunofluorescence data. Sci Rep 16, 5015 (2026). https://doi.org/10.1038/s41598-026-35341-8
Trefwoorden: pancreaskanker, tumormicro-omgeving, ruimtelijke beeldvorming, immuuninteracties, precisie-oncologie