Clear Sky Science · nl
Een lysinevrij REC-tag-systeem voor toepassingen met nabijheids-biotinylering
Waarom kleine tags op eiwitten ertoe doen
In elke cel werken eiwitten zelden alleen — ze vormen veranderende samenwerkingsverbanden die gezondheid en ziekte sturen. Om deze partnerschappen te bestuderen, plakken onderzoekers vaak kleine “naambordjes” op eiwitten zodat ze gevolgd, uit een mengsel gehaald of onder een microscoop gezien kunnen worden. Een populaire methode, nabijheids-biotinylering, stelt onderzoekers in staat te achterhalen wie zich in de buurt van wie bevindt in de cel, maar heeft een verborgen probleem: veel van deze naambordjes worden chemisch gemodificeerd en verdwijnen effectief juist op het moment dat ze het meest nodig zijn. Deze studie introduceert een nieuw type tag, de REC-tag, ontworpen om zichtbaar te blijven onder deze veeleisende omstandigheden.
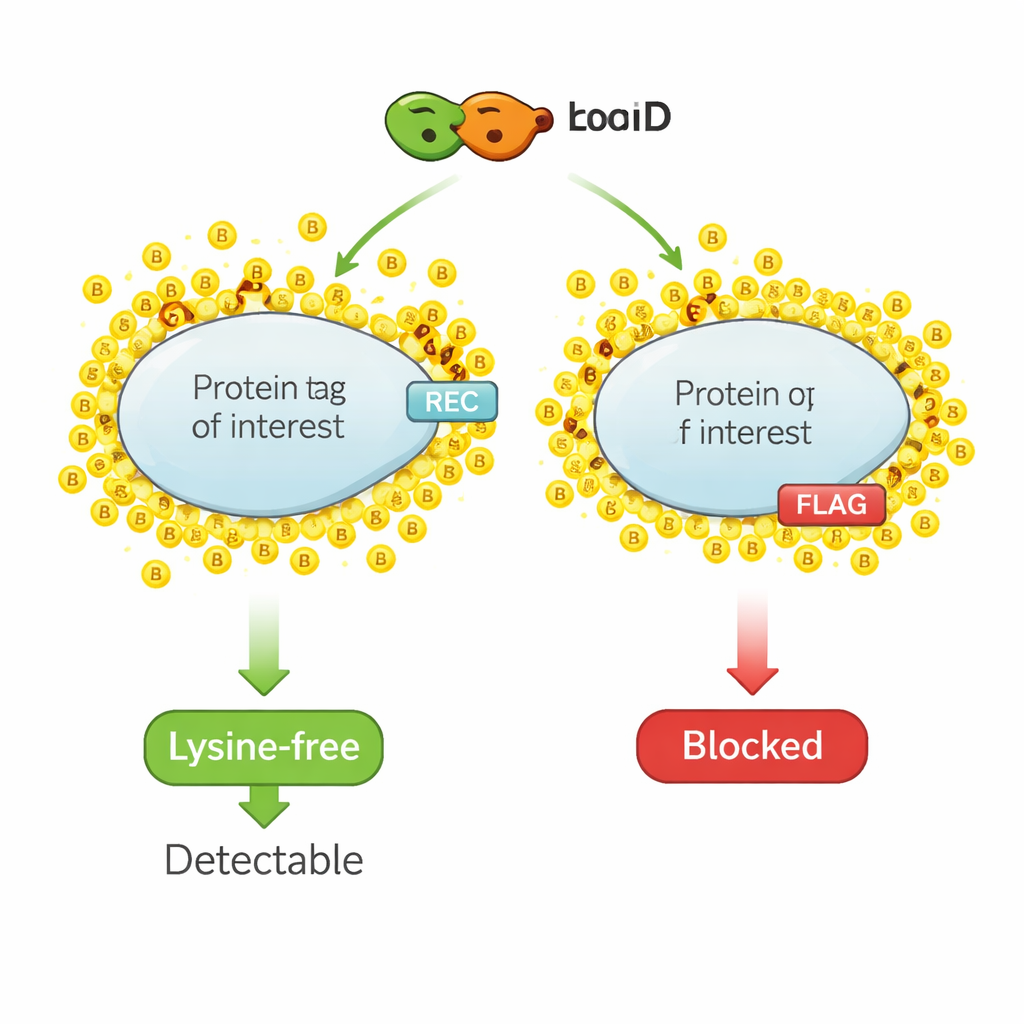
Een chemische markeerstift voor eiwitburen
Nabijheids-biotinylering werkt als een moleculaire markeerstift. Een geïngineerd enzym, zoals TurboID, wordt gefuseerd met een eiwit van interesse. Wanneer biotine — een klein vitaminemolecuul — wordt toegevoegd, hecht TurboID snel biotinemoleculen aan nabije eiwitten. Onderzoekers vissen vervolgens alle biotine-gemarkeerde eiwitten op en identificeren ze, waardoor ze een momentopname krijgen van de lokale omgeving van het eiwit. Dezelfde chemie die nabije eiwitten labelt, richt zich echter ook op de kleine epitooptags die gewoonlijk voor detectie worden gebruikt, omdat die tags vaak lysine bevatten, een aminozuur dat het belangrijkste aanhechtingspunt voor biotine is. Wanneer lysines in de tag met biotine worden bedekt, kunnen antilichamen de tag niet langer herkennen en daalt of verdwijnt het signaal in standaard detectiemethoden.
Een tag ontwerpen die modificatie weigert
Om dit op te lossen, gingen de auteurs aan de slag om een nieuwe tag te ontwikkelen die volledig vrij is van lysine. Ze startten vanaf een fragment van een malariaparasiet-eiwit genaamd PfRipr5, dat weinig gelijkenis vertoont met humane eiwitten, waardoor het risico op ongewenste kruisreacties kleiner wordt. Met een microchip-gebaseerde screeningsmethode in konijnen genereerden ze 22 monoklonale antilichamen tegen PfRipr5 en identificeerden ze er één, aangeduid als kloon nr. 6, met bijzonder sterke en specifieke binding. Door het PfRipr5-fragment systematisch te verkleinen en te muteren, konden ze het doel van het antilichaam terugbrengen tot een reeks van 11 aminozuren. Deze minimale sequentie bevatte slechts één lysine, die ze vervingen door een verwant aminozuur, arginine. Opmerkelijk genoeg bleef het antilichaam even goed binden. Deze geoptimaliseerde, lysinevrije sequentie werd REC-tag genoemd, en het bijpassende antilichaam het REC-antilichaam.
De REC-tag op de proef stellen
Het team testte vervolgens of de REC-tag kon dienen als vervanging voor veelgebruikte tags zoals FLAG in gangbare laboratoriumtechnieken. Wanneer gefuseerd met fluorescerende of signalerende eiwitten en geproduceerd in celvrije systemen en in zoogdiercellen, werden REC-getagde eiwitten gemakkelijk gedetecteerd door immunoblotting, een hoge-gevoeligheids lichtgebaseerde plaatassay genaamd AlphaScreen, en immunokleuring in cellen. De detectiekracht was vergelijkbaar met die van de FLAG-tag en van een ander lysinevrij tagsysteem (AGIA), en het REC-antilichaam vertoonde zeer weinig achtergrondruis in verschillende menselijke en apencellijnen. Belangrijk is dat de tag werkte zowel wanneer deze aan het begin als aan het einde van een eiwit werd geplaatst, en op eiwitten die zich in diverse cellulaire compartimenten bevinden, waaronder de kern, mitochondriën, het endoplasmatisch reticulum en het celmembraan.
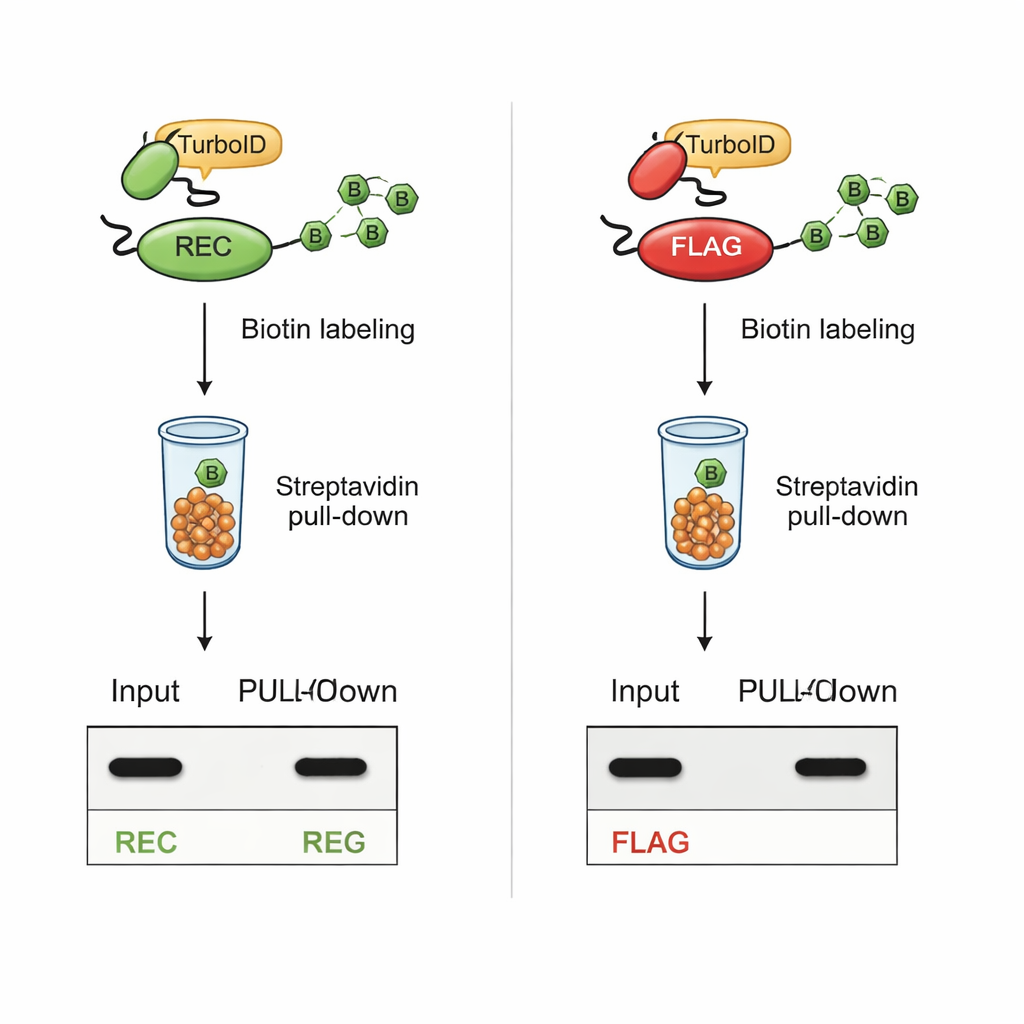
Zichtbaar blijven tijdens intensieve labeling
De kritieke proef was of REC detecteerbaar zou blijven na TurboID-gebaseerde biotinylering. In cellen waarin TurboID was gefuseerd aan bekende interactiepartners, bleven eiwitten met de REC-tag duidelijk zichtbaar in zowel hele cel-extracten als in de gezuiverde, biotine-gelabelde fractie. Daarentegen verloren eiwitten met de klassieke FLAG-tag hun FLAG-signaal zodra TurboID actief werd, ook al waren de eiwitten zelf nog steeds aanwezig. Aanvullende experimenten met synthetische peptiden toonden aan dat TurboID rechtstreeks de lysines in de FLAG-sequentie biotinylering en zo fysiek de toegang voor antilichamen blokkeert. De REC-tag, die geheel geen lysine bevatte, bleef onaangeroerd door TurboID en bleef gemakkelijk te detecteren.
Wat dit betekent voor toekomstige experimenten
Voor onderzoekers die eiwitnetwerken in levende cellen verkennen, biedt de REC-tag een praktisch nieuw hulpmiddel: hij gedraagt zich als bekende tags in alledaagse assays maar werkt doorlopend zelfs wanneer krachtige nabijheids-labelende enzymen actief zijn. Dat betekent dat wetenschappers betrouwbaarder kunnen bevestigen dat hun getagde eiwitten aanwezig en correct gevangen zijn, en dat ze andere lysine-gebaseerde modificaties — zoals ubiquitinering en acetylatie — kunnen bestuderen zonder dat de tag zelf stoort. Kortom, REC is een kleine ontwerpwijziging met grote impact, die helpt complexe eiwitkartografische experimenten helderder en betrouwbaarder te maken.
Bronvermelding: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Trefwoorden: proteïnetagging, nabijheids-biotinylering, TurboID, proteïne-interacties, epitooptags