Clear Sky Science · nl
EEG-gebaseerde classificatie van de ziekte van Alzheimer en frontotemporale dementie met behulp van functionele connectiviteit
Waarom hersengolfpatronen ertoe doen
Dementie treft miljoenen families, maar zelfs artsen hebben soms moeite om verschillende vormen van elkaar te onderscheiden. De ziekte van Alzheimer en frontotemporale dementie lijken in de kliniek vaak op elkaar, terwijl ze verschillende zorgplannen en onderzoeksopzetten vereisen. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen we met een snelle, niet-invasieve hersentest — elektro-encefalografie, of EEG — de communicatiemodi van de hersenen in rust aflezen en daarmee deze aandoeningen onderscheiden van gezond ouder worden, en van elkaar?
Kijken naar hersengesprekken, niet alleen naar hersenactiviteit
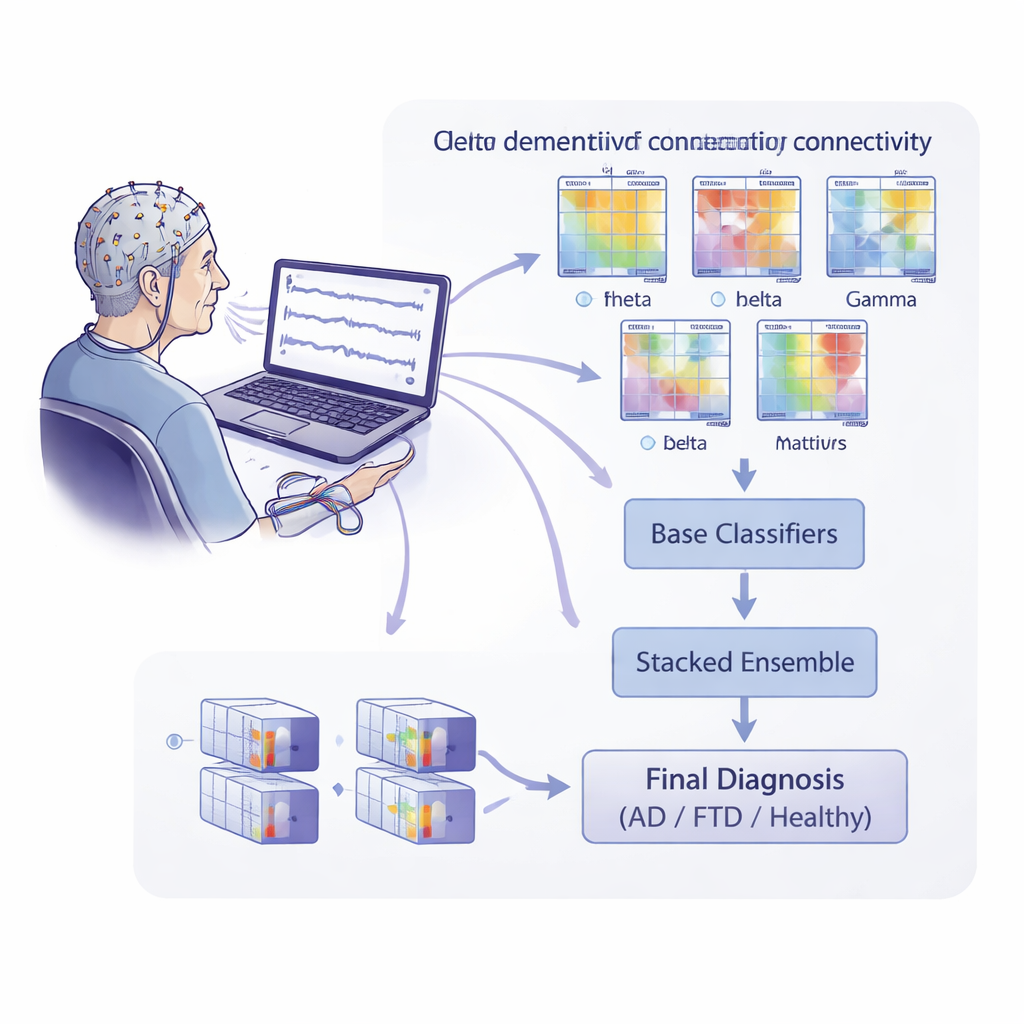
EEG meet meestal hoe sterk hersengolven zijn in verschillende frequentiebanden, zoals langzame delta- of snellere alpha-golven. De onderzoekers gingen hier een stap verder en onderzochten hoe verschillende delen van de hersenen “met elkaar praten”. Ze gebruikten opnamen van 88 personen: 36 met de ziekte van Alzheimer, 23 met frontotemporale dementie en 29 gezonde oudere volwassenen. Met 19 slaapelektroden registreerden ze hersenactiviteit in rust met gesloten ogen, en verdeelden elke opname vervolgens in veel korte tijdsegmenten. Voor elk segment en voor meerdere frequentiebanden berekenden ze een reeks connectiviteitsmaatregelen — wiskundige beschrijvingen van hoe sterk verschillende EEG-kanalen in tijd, frequentie en fase met elkaar verbonden zijn.
Algoritmes trainen om dementiepatronen te herkennen
Om deze connectiviteitskaarten om te zetten in voorspellingen trainde het team een groot aantal basis-machine-learningmodellen, waarbij elk model zich richtte op een combinatie van frequentieband en connectiviteitsmaat. Deze basismodellen gebruikten gespecialiseerde wiskundige middelen om connectiviteitspatronen tussen individuen te vergelijken. De uitkomsten van alle basismodellen werden vervolgens gevoed aan een hoger niveau ‘‘gestapeld’’ model dat probeerde te leren welke combinaties van kenmerken het meest informatief waren. Cruciaal is dat de onderzoekers de prestatie evalueerden op het niveau dat klinisch telt: één diagnose per persoon. Ze gebruikten een strikt testschema waarbij de gegevens van één persoon altijd volledig gescheiden werden gehouden van de trainingsdata, waardoor het risico op te optimistische resultaten door subtiele datalekken werd verkleind.
Wat de hersengolven onthulden — en wat niet
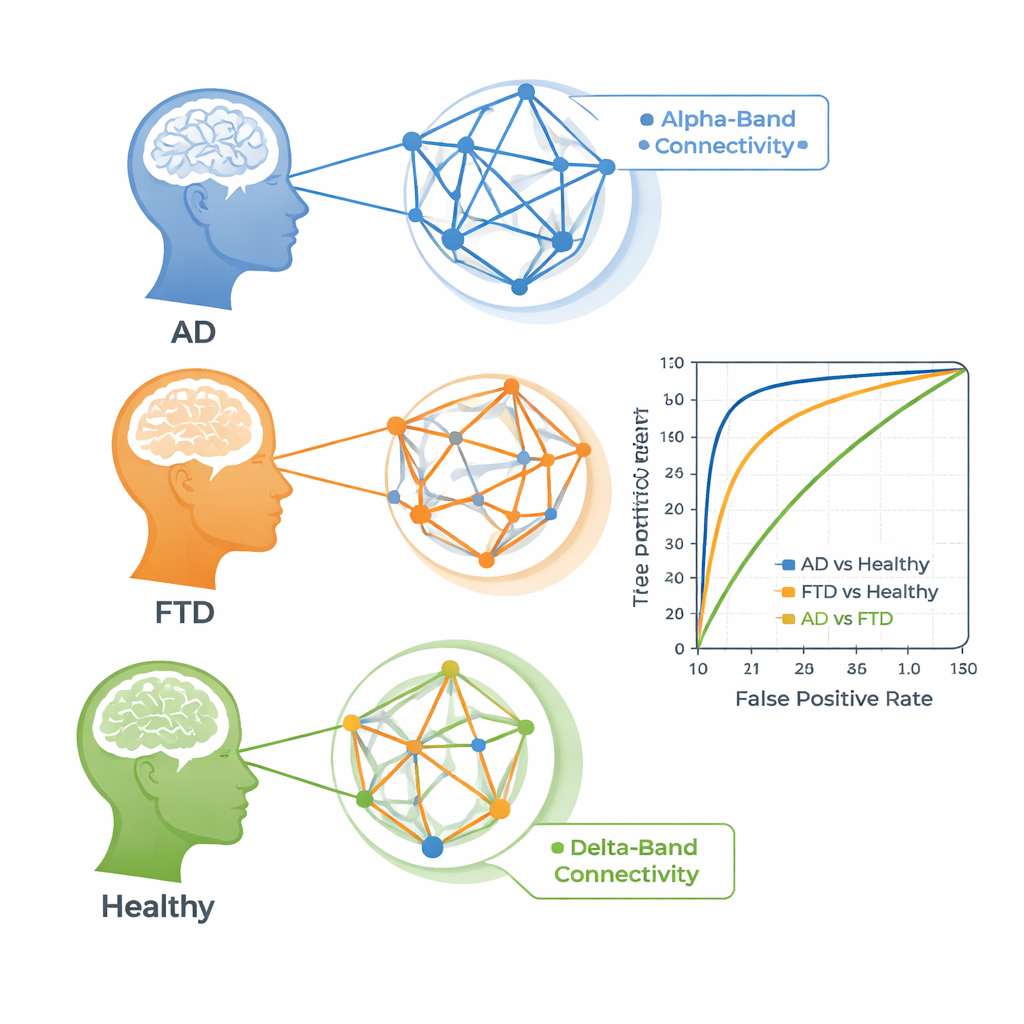
De connectiviteitspatronen hielpen om mensen met dementie te scheiden van gezonde vrijwilligers. Voor Alzheimer versus gezonde controles behaalden sommige individuele connectiviteitskenmerken een area-under-the-curve-score boven 85%, wat betekent dat ze redelijk goed waren in het rangschikken van wie de ziekte had. Hetzelfde gold, zij het iets zwakker, voor frontotemporale dementie versus gezond ouder worden. De meest informatieve signalen in beide gevallen kwamen uit de alpha-band, een ritme dat gekoppeld is aan ontspannen waakzaamheid en dat vaak verstoord is bij dementie. Daarentegen bleek het veel moeilijker om Alzheimer en frontotemporale dementie van elkaar te onderscheiden. De beste maten voor die taak kwamen uit de langzame delta-band en bereikten slechts bescheiden nauwkeurigheid, wat suggereert dat beide ziekten veel van dezelfde grootschalige netwerkafwijkingen delen in deze EEG-opnamen.
Wanneer meer complexiteit geen betere antwoorden oplevert
Een van de hoop van ensemblemethoden is dat het combineren van vele zwakke voorspellers een sterker, betrouwbaarder model kan opleveren. In deze studie presteerde het gestapelde ensemble echter niet beter dan de beste enkele connectiviteitskenmerken. Sterker nog: de beste op zichzelf staande modellen waren vaak iets beter. Verdere analyses toonden aan dat veel basismodellen vergelijkbare soorten fouten maakten, waardoor het ensemble beperkte echt nieuwe informatie had om te benutten. De auteurs testten ook verschillende manieren om afstanden tussen connectiviteitsmatrices te meten, inclusief geavanceerde „manifold”-geometriemethoden, maar vonden weinig voordeel ten opzichte van eenvoudigere benaderingen voor dit diagnostische probleem tussen personen.
Wat dit betekent voor patiënten en clinici
Voor mensen die geheugen- of gedragsveranderingen ervaren, bieden deze bevindingen voorzichtige optimisme. Rust-EEG, een snelle, goedkope en algemeen beschikbare test, legt betekenisvolle handtekeningen van dementie vast in hoe hersengebieden met elkaar verbonden zijn. Tegelijk benadrukt het werk dat slimme wiskunde alleen niet volledig onderscheid kan maken tussen nauw verwante ziekten wanneer de gegevens beperkt zijn en hersenveranderingen overlappen. De auteurs betogen dat zorgvuldig gekozen, interpreteerbare EEG-kenmerken, beoordeeld met strikte subjectniveau-tests, betrouwbaarder kunnen zijn dan zeer complexe modellen. Toekomstige vooruitgang, suggereren zij, zal waarschijnlijk komen door EEG-connectiviteit te combineren met andere biomarkers zoals hersenscans, bloedtesten en cognitieve profielen, om meer precieze en betrouwbare hulpmiddelen te bouwen voor het diagnosticeren van verschillende vormen van dementie.
Bronvermelding: Mlinarič, T., Van Den Kerchove, A., Barinaga, Z.I. et al. EEG-based classification of alzheimer’s disease and frontotemporal dementia using functional connectivity. Sci Rep 16, 4903 (2026). https://doi.org/10.1038/s41598-026-35316-9
Trefwoorden: EEG, functionele connectiviteit, ziekte van Alzheimer, frontotemporale dementie, machine learning