Clear Sky Science · nl
Interactie tussen ELMO1-DNA-methylering en Med31 bevordert door H. pylori geïnduceerde maagkanker-EMT en intestinale metaplasie via M2-polarisatie
Waarom bacteriën in de maag van belang zijn voor kankerrisico
De meesten van ons dragen miljarden bacteriën in ons spijsverteringsstelsel, en een daarvan — Helicobacter pylori — kan decennialang stil in de maag verblijven. Bij sommige mensen is die infectie onschadelijk, maar bij anderen vormt ze de eerste stap richting maagkanker, een van de dodelijkste vormen van kanker wereldwijd. Deze studie onderzoekt hoe een kleine chemische wijziging aan DNA in maagcellen helpt om een langdurige infectie om te zetten in voorstadia van kanker en uiteindelijk in een omgeving waarin tumorvorming wordt gefaciliteerd.
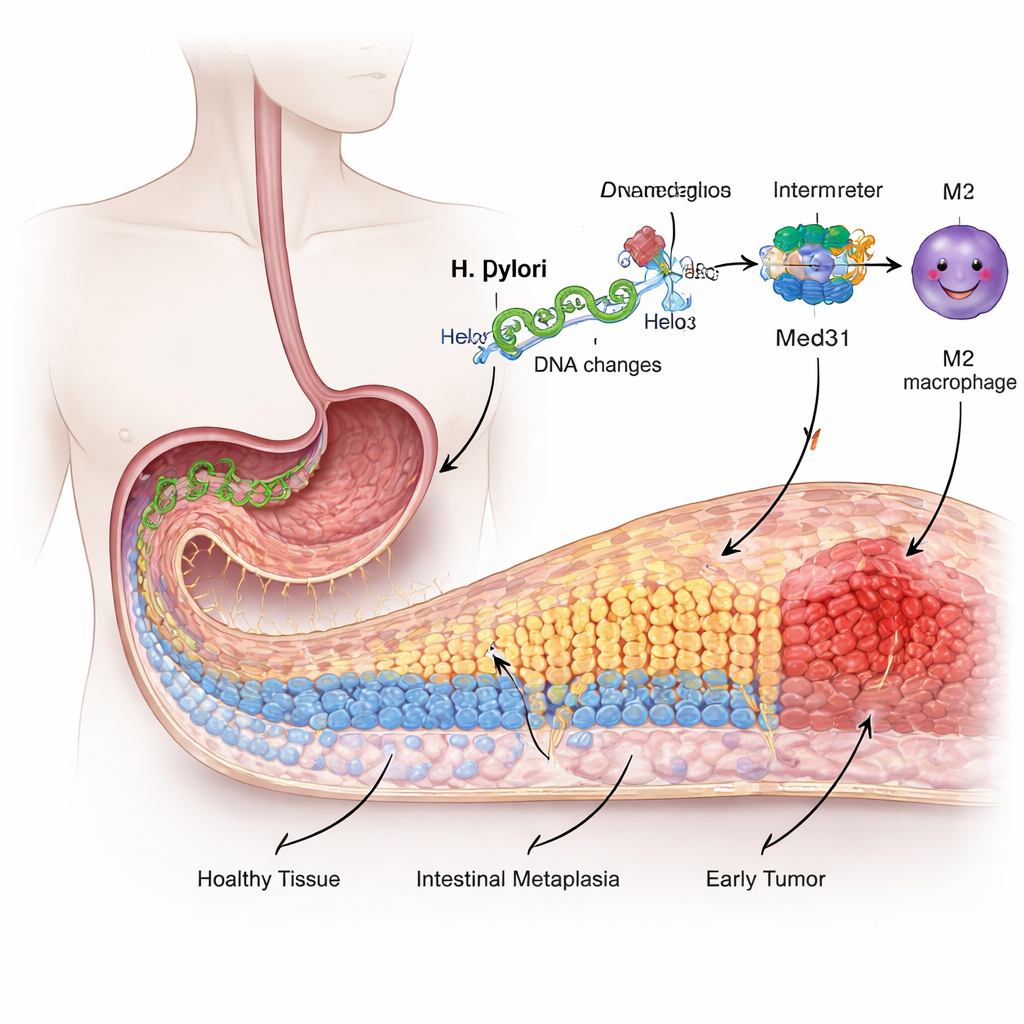
Van beschermende bekleding naar risicovolle transformatie
De binnenkant van de maag is bekleed met gespecialiseerde cellen die zijn aangepast om met sterke zuurheid om te gaan, en niet om voedsel te verteren zoals de dunne darm. Na jaren van irritatie en ontsteking door H. pylori beginnen sommige van deze maagcellen zich te “herinrichten” en trekken ze kenmerken van darmcellen aan in een proces dat intestinale metaplasie wordt genoemd. Deze verandering wordt beschouwd als een voorstadium van kanker. De onderzoekers gebruikten een menselijke maagcellijn om infectie na te bootsen en vonden dat blootstelling aan H. pylori deze cellen sneller deed groeien, makkelijker liet bewegen en intestine‑type merkers activeerde — allemaal tekenen dat de bekleding afwijkt van haar normale identiteit.
Kleine chemische labels met grote gevolgen
Ons DNA kan worden voorzien van kleine chemische labels die methylgroepen worden genoemd; die werken als aan‑/uit‑schakelaars voor genen zonder de genetische code zelf te veranderen. Het team richtte zich op een gen genaamd ELMO1, dat al bekendstaat als betrokken bij celbeweging en tumorverspreiding. Ze toonden aan dat H. pylori-infectie de methylering van het ELMO1-gen verhoogde en, enigszins tegenintuïtief, de activiteit en eiwitniveaus ervan in maagcellen deed toenemen. Wanneer ze een middel gebruikten dat deze methylgroepen verwijdert, verloren de cellen veel van de door de infectie veroorzaakte veranderingen: ze deelden minder, bewogen minder en toonden minder signalen van intestinale metaplasie. Dit wijst erop dat ELMO1-methylering een cruciale schakel is die door de bacterie wordt omgezet.
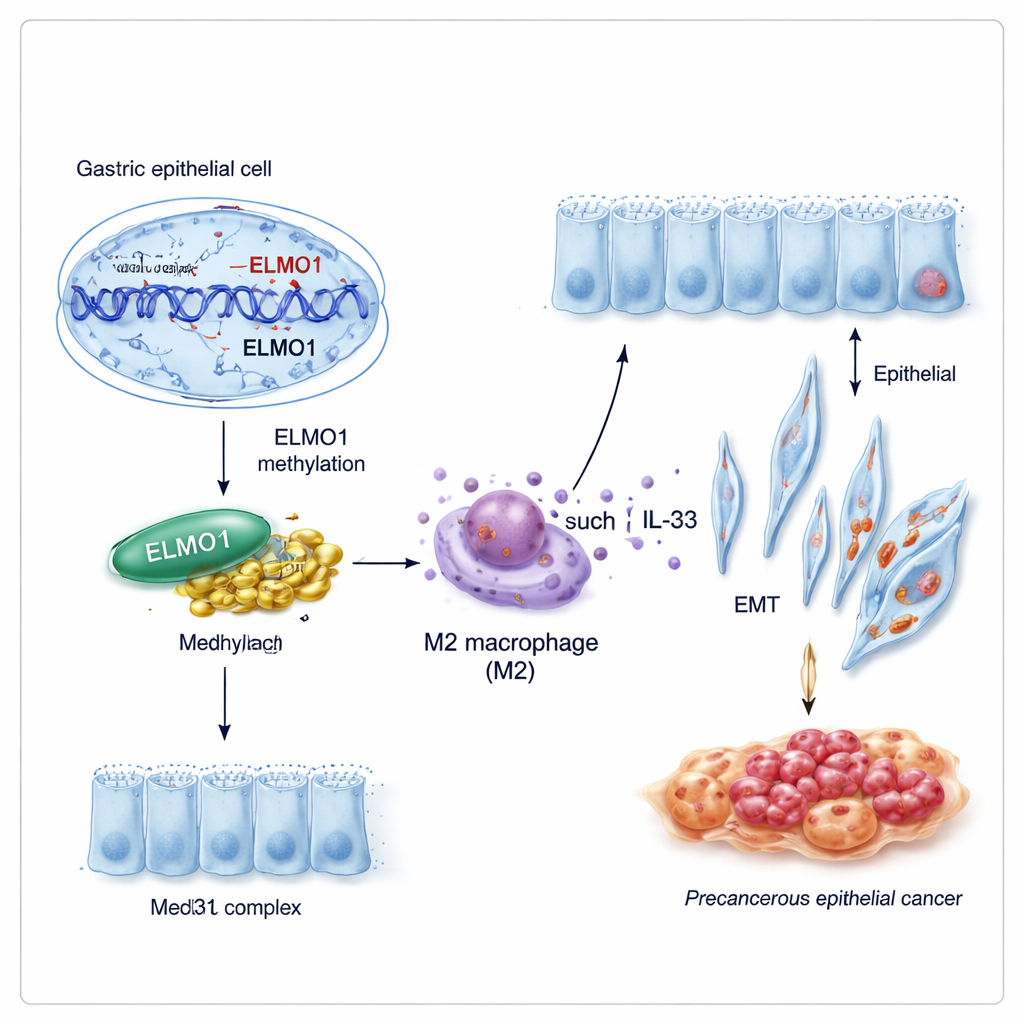
Een nieuw partnerschap dat celgedrag herprogrammeert
Genen werken zelden alleen. De onderzoekers ontdekten dat gemethyleerd ELMO1 de voorkeur geeft aan een partnerschap met een ander eiwit, Med31, dat deel uitmaakt van een groot “bedieningspaneel” dat helpt te bepalen welke genen een cel aanzet. Onder condities die methylering bevorderen, stegen ELMO1- en Med31-niveaus, en binden de twee fysiek aan elkaar, terwijl een eerder bekende partner van ELMO1, DOCK10, op de achtergrond raakte. Dit nieuwe ELMO1–Med31‑team lijkt het genexpressieprogramma van maagcellen te verschuiven op een manier die hen aanmoedigt intestine kenmerken aan te nemen en agressiever te gedragen.
Hoe immuuncellen worden aangestuurd om de tumor te helpen
Kanker ontwikkelt zich niet in isolatie; ze groeit binnen een complex buurtje van immuun- en ondersteunende cellen. De studie toont aan dat geïnfecteerde maagcellen met gemethyleerd ELMO1 hogere niveaus van IL‑33 vrijgeven, een signaal dat nabije immuuncellen, macrophagen genaamd, in een tumor‑vriendelijke “M2”‑toestand duwt. Met behulp van een co‑kweekmodel vonden de auteurs dat macrophagen blootgesteld aan deze signalen sterk de neiging kregen naar het M2‑type en op hun beurt factoren uitscheiden die verse maagcellen aanspoorden mobieler, invasiever en meer op intestinecellen te lijken. Merkers van epitheel‑mesenchymale transitie — wanneer stationaire bekledingscellen veranderen in rondzwervende, invasievaardige cellen — namen scherp toe onder invloed van deze M2‑macrophagen.
Wat dit betekent voor het voorkomen van maagkanker
Gezamenlijk schetst het werk een keten van gebeurtenissen: H. pylori-infectie verandert DNA‑methylering van ELMO1, dit aangepaste ELMO1 vormt een team met Med31, geïnfecteerde cellen zenden signalen uit die nabije immuuncellen in M2‑helpers omzetten, en deze helpers drijven zowel intestinale metaplasie als een invasievere celtoestand aan. Voor niet‑specialisten is het kernidee dat een veelvoorkomende maagbacterie zowel de maagbekleding als de lokale immuunrespons kan hervormen via omkeerbare chemische labels op DNA. Inzicht in deze route kan deuren openen naar nieuwe bloedtests die risicovolle methyleringspatronen vroeg detecteren, evenals geneesmiddelen die de ELMO1–Med31–M2‑as onderbreken voordat een chronische infectie uitgroeit tot maagkanker.
Bronvermelding: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
Trefwoorden: maagkanker, Helicobacter pylori, DNA-methylering, intestinale metaplasie, tumormicro-omgeving