Clear Sky Science · nl
Automatische segmentatie en classificatie voor detectie van baarmoederhalskanker op basis van deep learning met een verbeterde U-Net en ensemblemethoden
Waarom Pap-tests nog steeds een digitale helpende hand nodig hebben
Baarmoederhalskanker is een van de weinige kankers die sterk te voorkomen is wanneer deze vroeg wordt opgespoord, maar toch sterven veel vrouwen omdat gevaarlijke celveranderingen worden gemist of te laat worden ontdekt. De bekende Pap-test redt al levens, maar het beoordelen van duizenden celafbeeldingen met het blote oog is traag en vermoeiend werk en zelfs deskundigen kunnen van mening verschillen. Dit artikel onderzoekt hoe moderne kunstmatige intelligentie kan fungeren als onvermoeibare assistent door automatisch baarmoederhalscellen in Pap‑smear afbeeldingen te vinden en te sorteren, zodat artsen waarschuwingssignalen sneller en betrouwbaarder kunnen zien.
Computers leren probleemcellen te zien
De onderzoekers wilden een computersysteem bouwen dat twee kerntaken kan uitvoeren: ten eerste elke baarmoederhalscel uit de achtergrond van een Pap‑smear afbeelding halen, en ten tweede bepalen of de cel er normaal uitziet of afwijkingen vertoont die met kanker samenhangen. Hiervoor gebruikten ze deep learning, een vorm van AI die patronen rechtstreeks leert uit grote aantallen voorbeeldafbeeldingen in plaats van uit handgeschreven regels. Hun systeem richt zich op de gehele cel—zowel het donkere centrum (kern) als het omringende materiaal (cytoplasma)—omdat veranderingen in grootte, vorm en textuur over de hele cel heen op ziekte kunnen wijzen.
Een slimmer manier om cellen te omlijnen
Het hart van het systeem is een verbeterde versie van een populair medisch beeldmodel genaamd U‑Net, dat bijzonder goed is in het nauwkeurig omlijnen van objecten in afbeeldingen. De auteurs pasten U‑Net aan zodat het beelddetails op meerdere schalen tegelijk kan bekijken en stabiel blijft, zelfs wanneer het op kleine batches gegevens wordt getraind—een veelvoorkomende beperking in medisch onderzoek. Dit opgewaardeerde netwerk leert een eenvoudige maskerlaag over elke afbeelding te tekenen: wit waar een cel aanwezig is, zwart voor de achtergrond. Door alleen de celgebieden te isoleren, kunnen latere stappen in de verwerkingsketen zich concentreren op wat het belangrijkst is in plaats van te worden afgeleid door vlekken, vuil of lege ruimte.
Meer trainingsvoorbeelden uit het niets maken
Een grote uitdaging in de geneeskunde is dat hoogwaardige, gelabelde afbeeldingen schaars en kostbaar zijn om te verkrijgen. Om dit aan te pakken gebruikte het team een generatief model genaamd RES_DCGAN, dat leert realistische synthetische Pap‑smear afbeeldingen te creëren op basis van de echte afbeeldingen. Deze extra “gemaakt maar overtuigende” afbeeldingen worden in het trainingsproces gemengd, zowel vóór de celomlijning als daarna, in de classificatiestap. Door veel meer variaties van cellen te zien—including zeldzame en subtiele patronen—wordt de AI robuuster en minder geneigd om te overfitten op een kleine set patiënten of beeldomstandigheden.
Van omtrekken naar vroege waarschuwingen
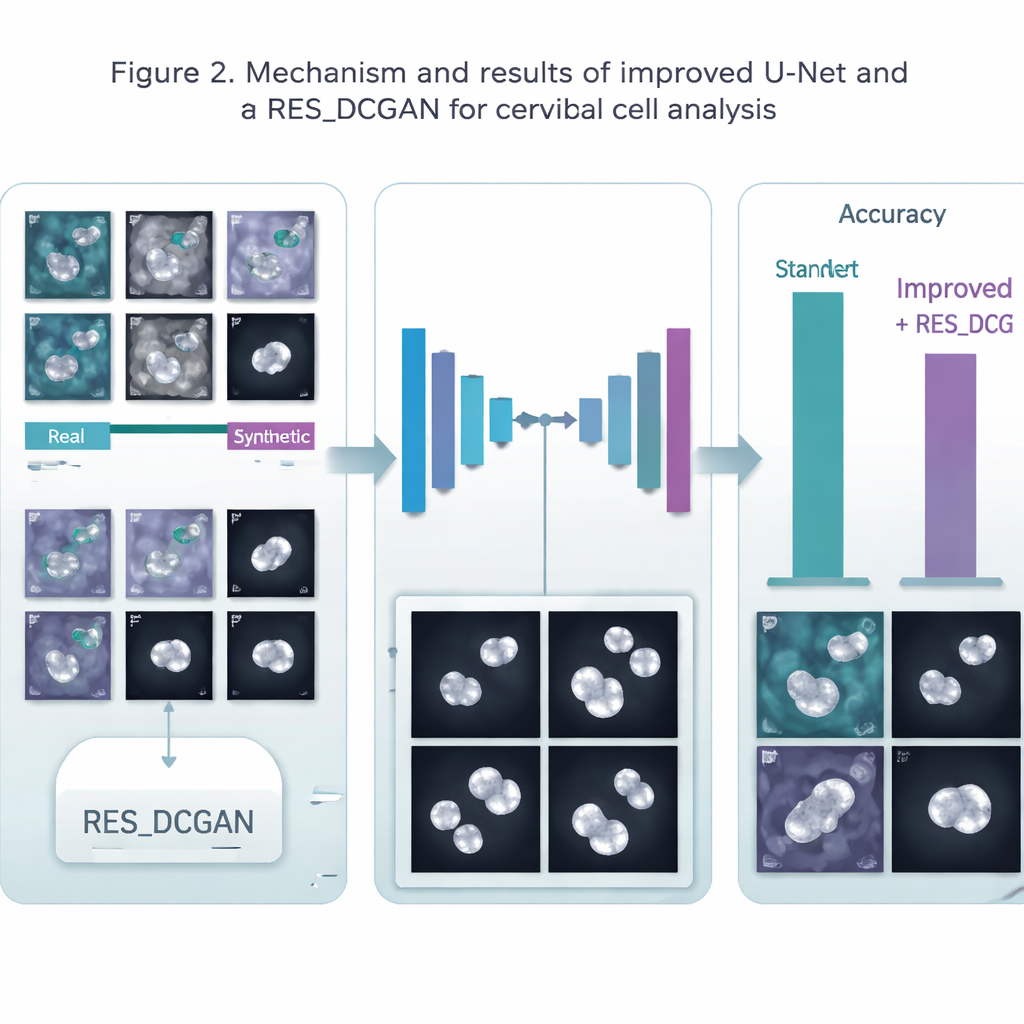
Zodra de cellen zijn gesegmenteerd, neemt een tweede groep deep learning‑modellen het over om elke cel te classificeren als normaal of behorend tot verschillende abnormale categorieën. De auteurs gebruikten een sterk beeldherkenningsmodel genaamd ResNet50V2 en combineerden het met meerdere andere bekende netwerken in een "ensemble", waarbij meerdere modellen gezamenlijk stemmen over de uiteindelijke beslissing. Ze testten zes verschillende verwerkingspijplijnen op drie datasets uit Polen (Pomeranian), Denemarken (Herlev) en Griekenland (SIPaKMeD), die zowel eenvoudige normaal‑tegen‑abnormaal gevallen als meer gedetailleerde multiclass‑problemen besloegen. In al deze tests verbeterde het eerst segmenteren van de cellen de classificatienauwkeurigheid consequent, en het toevoegen van synthetische afbeeldingen duwde de prestaties doorgaans nog iets omhoog, vooral voor het omlijnen van de cellen.
Hoe goed presteerde de digitale assistent?
Het systeem behaalde zeer hoge scores. Voor het omlijnen van cellen bereikte de nauwkeurigheid ongeveer 99,5% op één dataset en rond 98% op een andere, waarmee het ruimschoots een standaard U‑Net overtrof. Voor het bepalen van het celtype labelde het ensemble van modellen ongeveer 95–96% van de cellen correct bij de complexere taken en tot 99% bij eenvoudigere ja/nee‑beslissingen over kankerrisico. Deze resultaten evenaren of overtreffen veel eerdere studies, en tonen bovendien aan dat een enkele, uniforme pijplijn over verschillende laboratoria en databronnen kan werken. De verbeteringen waren gematigder bij één bijzonder gevarieerde dataset, wat benadrukt dat reële diversiteit nog steeds uitdagingen vormt.
Wat dit betekent voor patiënten en artsen
In gewone bewoordingen laat dit werk zien dat een AI‑assistent kan leren baarmoederhalscellen zorgvuldig te omlijnen en ze consistent in risicogroepen te sorteren. Het vervangt de patholoog niet, maar het kan diavooronderzoek vooraf uitvoeren, verdachte cellen markeren en de kans verkleinen dat vroege signalen over het hoofd worden gezien in drukke klinieken of in regio's met weinig specialisten. Met verder testen op grotere, complexere monsters en door experts gevalideerde maskers, zouden systemen als deze betrouwbare screening op baarmoederhalskanker aan meer vrouwen wereldwijd kunnen brengen, gevaarlijke veranderingen vroeger opsporen en de kans op succesvolle behandeling vergroten.
Bronvermelding: Wubineh, B.Z., Rusiecki, A. & Halawa, K. Deep learning-based automatic segmentation and classification for cervical cancer detection using an improved U-Net and ensemble methods. Sci Rep 16, 5184 (2026). https://doi.org/10.1038/s41598-026-35299-7
Trefwoorden: screening op baarmoederhalskanker, Pap‑smear afbeeldingen, deep learning, medische beeldsegmentatie, computerondersteunde diagnose