Clear Sky Science · nl
Beoordeling van de biochemische basis van resistentie tegen systemische amyloïdose
Wanneer kleine eiwitveranderingen een dodelijke ophoping blokkeren
Veel chronische ontstekingsziekten, van reumatoïde artritis tot tuberculose, kunnen een zeldzame maar vaak dodelijke complicatie veroorzaken die systemische AA-amyloïdose wordt genoemd. Bij deze aandoening hoopt een normaal bloed-eiwit zich op als stijve vezels die organen verstoppen. Deze studie stelt een verrassend hoopvolle vraag: kunnen kleine, natuurlijke veranderingen in dat eiwit sommige dieren grotendeels immuun maken voor de ziekte — en zo ja, hoe?
De verborgen dreiging van eiwitophopingen
AA-amyloïdose begint met een ontstekingssignaal in het bloed genaamd serum amyloïd A (SAA). Tijdens ernstige of langdurige ontsteking kunnen de SAA-niveaus tot duizenden keren hoger worden dan normaal. Bij sommige mensen en dieren vouwt een deel van dit eiwit verkeerd en stapelt zich op tot lange vezels, bekend als amyloïde fibrillen, die zich door organen als milt en nieren verspreiden. Na verloop van tijd ondermijnen deze vezels de orgaanfunctie. Toch krijgt niet ieder individu met hoge SAA-waarden amyloïdose, en bepaalde muizenstammen blijven verrassend resistent, zelfs wanneer ze in het laboratorium richting de ziekte worden geduwd. Begrijpen waarom kan wijzen op nieuwe strategieën om amyloïdeophoping bij mensen te voorkomen.
Resistente muizen en hun speciale eiwitversies
Bij muizen ontstaan de meeste AA-amyloïde fibrillen uit één versie van SAA die SAA1.1 wordt genoemd en sterk aan de ziekte gekoppeld is. Sommige muizenstammen produceren echter voornamelijk licht afwijkende versies, aangeduid als SAA1.5 en SAA2.2, en deze stammen ontwikkelen zelden systemische AA-amyloïdose. De eiwitten verschillen slechts door enkele bouwstenen (aminozuren), maar die verschillen concentreren zich in een dicht gepakte regio die de inwendige kern van de ziekteveroorzakende vezels vormt. De onderzoekers stelden voor dat deze kleine verschillen de eiwitten niet volledig verhinderen te klonteren, maar wel voorkomen dat ze precies de schadelijke vezelvorm aannemen.
De eiwitten aan de tand voelen in het laboratorium
Om dit idee te onderzoeken, produceerde het team alle drie muis-SAA-varianten in bacteriën en volgde hun gedrag in reageerbuisexperimenten. Ze monitoren vezelvorming met een fluorescerende kleurstof die oplicht wanneer amyloïde ontstaat, en verifieerden structuren met elektronenmicroscopie. De ziektegerelateerde SAA1.1 vormde gemakkelijk lange, rechte vezels. SAA2.2 kon ook vezels vormen, maar deze waren dikker, meer gedraaid en structureel gevarieerder, en ze gaven niet hetzelfde sterke kleurstofsignaal. SAA1.5 vormde daarentegen bij de geteste condities geen vezels. Toen de onderzoekers kleine monsters van echte ziektevezels uit zieke muizenmilt toevoegden als “zaden”, groeide SAA1.1 snel nieuwe vezels die de structuur van het origineel nauw kopieerden, vergelijkbaar met een prion. Opmerkelijk genoeg groeiden SAA1.5 en SAA2.2 helemaal niet op deze zaden; de ex vivo vezels konden hen niet rekruteren in de pathogene vorm.
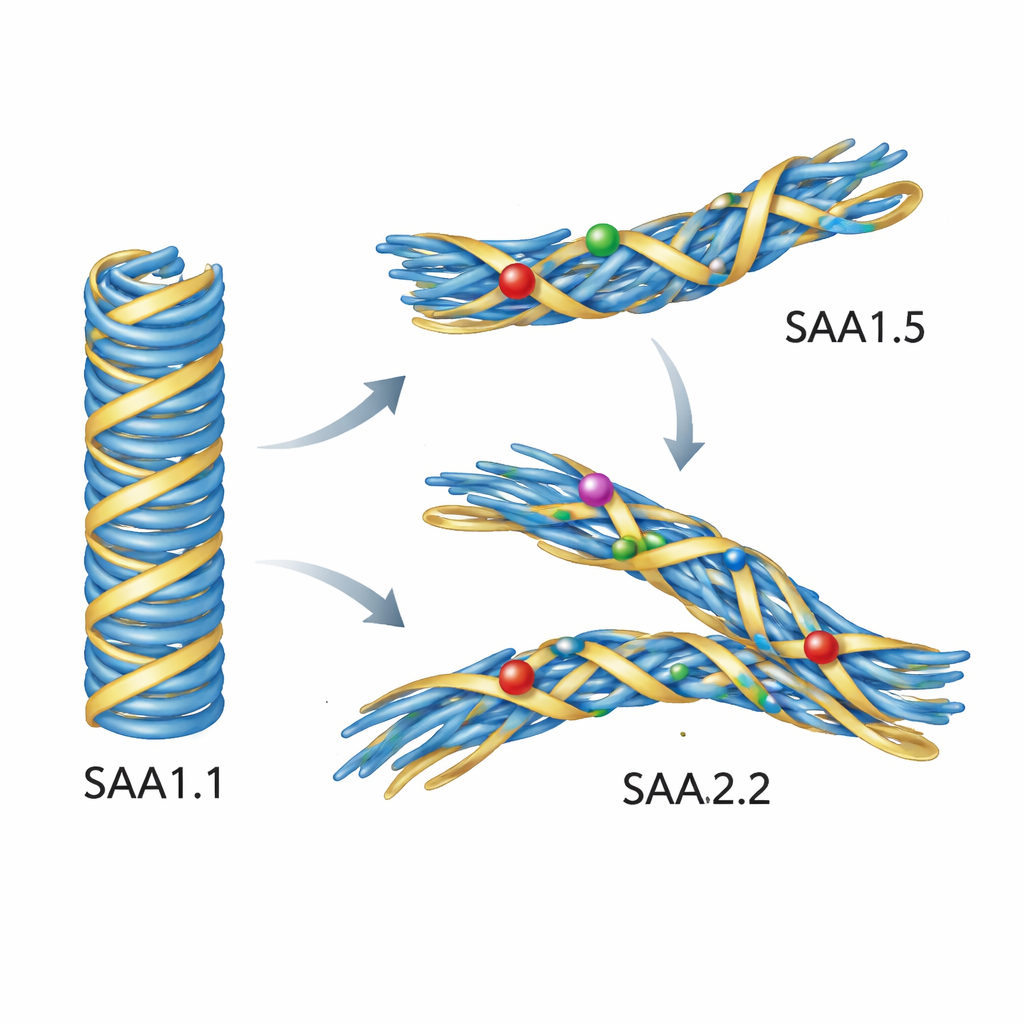
Simulaties tonen waarom gemuteerde eiwitten de schadelijke vorm weigeren
Experimenten alleen konden niet precies laten zien wat er op atomair niveau misgaat, dus deden de auteurs gedetailleerde computersimulaties. Ze startten van een hoge-resolutie-structuur van een pathogene muizen-AA-fibril opgebouwd uit SAA1.1, en vervingen vervolgens computationeel de sequenties door SAA1.5 en SAA2.2. Toen ze deze fibrillen in water bij lichaamstemperatuur simuleerden, bleef het SAA1.1-gebaseerde model opmerkelijk stabiel. Fibrillen opgebouwd uit SAA1.5 of SAA2.2 daarentegen verschoven en raakten vervormd. Een sleutel-lusregio in de kern schoof naar buiten en verloor zijn nauwe contact met het beginsegment van het eiwit, en verschillende zijketens draaiden naar nieuwe orientaties. Deze subtiele herschikkingen verstoorden de dichte verpakking die het ziektegerelateerde vouwwerk definieert. Met andere woorden: de varianten hadden geen bezwaar tegen het vormen van vezels in het algemeen — maar ze konden zich niet comfortabel voegen naar het sjabloon van de pathogene AA-fibril.
Wat de natuurontwerp ons wijst voor toekomstige therapieën
Samengevat toont het werk aan dat "amyloïde-resistente" muizenstammen niet beschermd zijn omdat hun SAA zich helemaal niet kan aggregeren. In plaats daarvan zijn hun SAA-versies structureel incompatibel met precies die ene vezelvorm die systemische AA-amyloïdose veroorzaakt. De eiwitten kunnen nog steeds samenklonteren, maar doen dat in alternatieve, naar het lijkt goedaardige vormen. Vergelijkbare beschermende mutaties zijn bekend bij andere eiwitmisvouwingziekten, inclusief sommige prion- en Alzheimer‑gevallen. Dit suggereert een breder principe: het zodanig aanpassen van een ziektegevoelig eiwit dat het zijn toxische architectuur niet kan aannemen — terwijl het nog steeds normaal functioneert — kan afdoende zijn om ziekte te voorkomen. Op termijn zouden therapieën geïnspireerd door deze natuurlijke “resistente” varianten, of door korte fragmenten afgeleid van hen, eiwitten kunnen helpen wegsturen van schadelijke vouwen en naar ongevaarlijke vormen leiden.
Bronvermelding: Moderer, T., Schnell, A.F., Scheurmann, N.J. et al. Assessment of the biochemical basis underlying the resistance against systemic amyloidosis. Sci Rep 16, 1313 (2026). https://doi.org/10.1038/s41598-026-35297-9
Trefwoorden: AA-amyloïdose, serum amyloïd A, eiwitmisvouwing, amyloïde resistentie, muismodellen