Clear Sky Science · nl
Modellering en experimentele verificatie van neerslag van polycaprolacton-nanodeeltjes
Waarom piepkleine plastic bolletjes belangrijk zijn voor de geneeskunde
Stel je voor dat je een krachtig geneesmiddel inpakt in een vlekje zo klein dat het door bloedvaten kan glippen en zijn lading precies aflevert waar dat nodig is. Zulke vlekjes, polymerenanodeeltjes genoemd, liggen aan de basis van veel opkomende behandelingen en beeldvormingsmiddelen. Ze met de juiste en reproduceerbare grootte maken is echter verrassend moeilijk. Deze studie laat zien hoe een eenvoudig, op natuurkunde gebaseerd computermodel de grootte van een veelgebruikt biologisch afbreekbaar nanodeeltje kan voorspellen en bijsturen, en daarmee mogelijk jaren van proef‑en‑fout kan besparen bij de ontwikkeling van nieuwe nanogeneesmiddelen.
Van keukengerei mengen naar laboratoriumprecisie
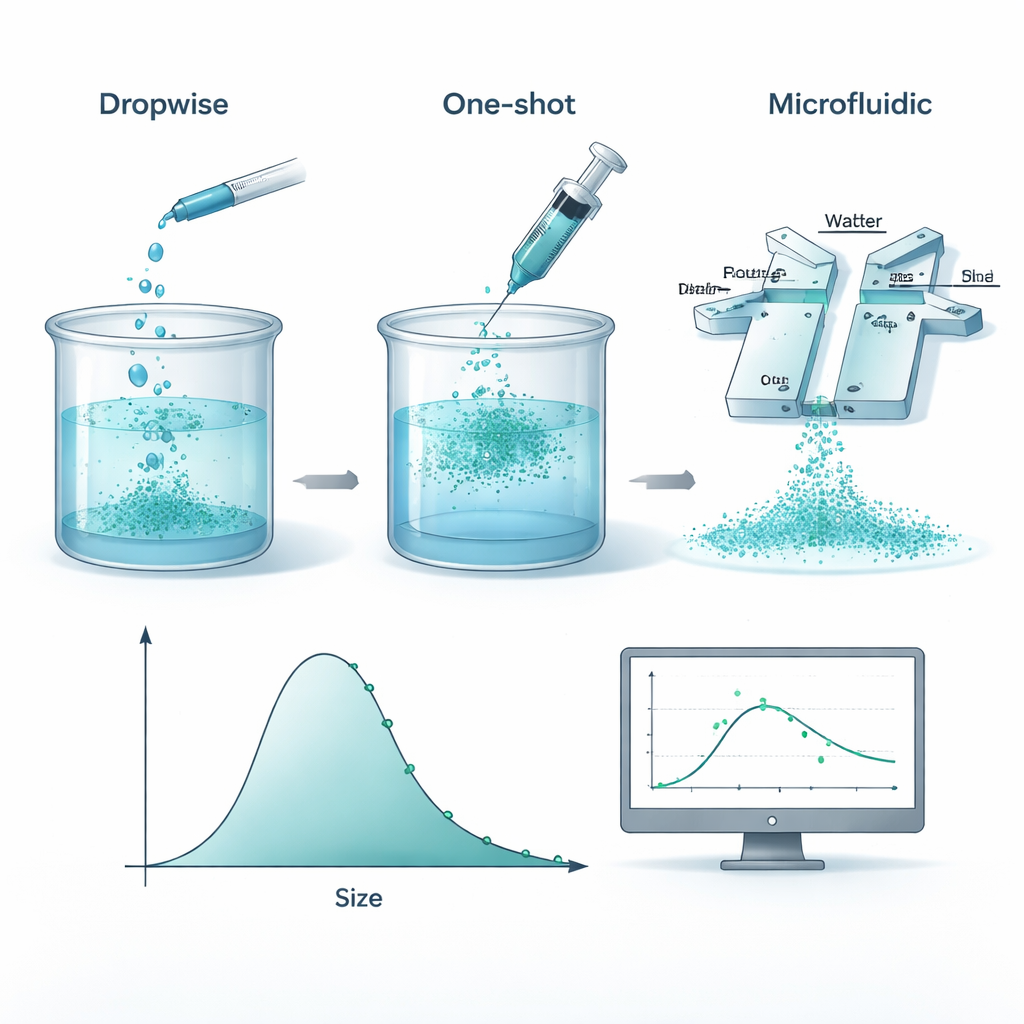
Om deze nanodeeltjes te maken lossen onderzoekers een biologisch afbreekbare kunststof genaamd polycaprolacton (PCL) op in een organisch oplosmiddel en mengen dat vervolgens met water, waardoor de polymeer uit de oplossing ‘valt’ en kleine bolletjes vormt. Het team vergeleek drie praktische manieren om dit te doen: de polymeeroplossing druppelsgewijs heel langzaam toevoegen, alles in één keer erin gooien, en beide vloeistoffen door een kleine microfluïdische chip duwen waar ze elkaar in smalle kanaaltjes ontmoeten. Onder zorgvuldig gecontroleerde omstandigheden leverden alle drie benaderingen deeltjes met zeer vergelijkbare gemiddelde groottes en spreidingen op. Dit betekent dat, althans in de bestudeerde reeksen, belangrijker is wat je erin stopt — hoeveelheden polymeer en stabilisator — dan welk mengapparaat je gebruikt.
Hoe viscositeit en hulpstoffen de deeltjes vormen
De onderzoekers onderzochten vervolgens hoe de receptingrediënten de uiteindelijke deeltjesgrootte bepalen. Het vergroten van de hoeveelheid PCL in de organische fase maakt die vloeistof dikker, oftewel viskeuzer. Denk aan het mengen van siroop in water in plaats van sap: dikkere siroop breekt in grotere druppels. Hier leidden dikker wordende polymeeroplossingen tot grotere nanodeeltjes en iets bredere grootteverdelingen. Het toevoegen van een tweede oplosmiddel, ethanol, hielp het proces stabiel te houden zelfs bij zeer hoge polymeerconcentraties, maar had als nadeel dat de deeltjes in het hogere concentratiegebied groter werden. Een tweede ingrediënt, een oppervlakteactieve stof genaamd Pluronic F‑127, werkt als een moleculaire anti‑klonteraar. Bij lage concentraties van de surfactant hebben deeltjes de neiging tegen elkaar te botsen en aan elkaar te kleven, waardoor ze groter en minder uniform worden. Naarmate de surfactantconcentratie toeneemt, bedekt deze de deeltjesoppervlakken, voorkomt samensmelting en levert kleinere, stabielere nanodeeltjes op — tot op zekere hoogte; daarboven nemen de voordelen af en kan de grootteverdeling weer gemengd raken.
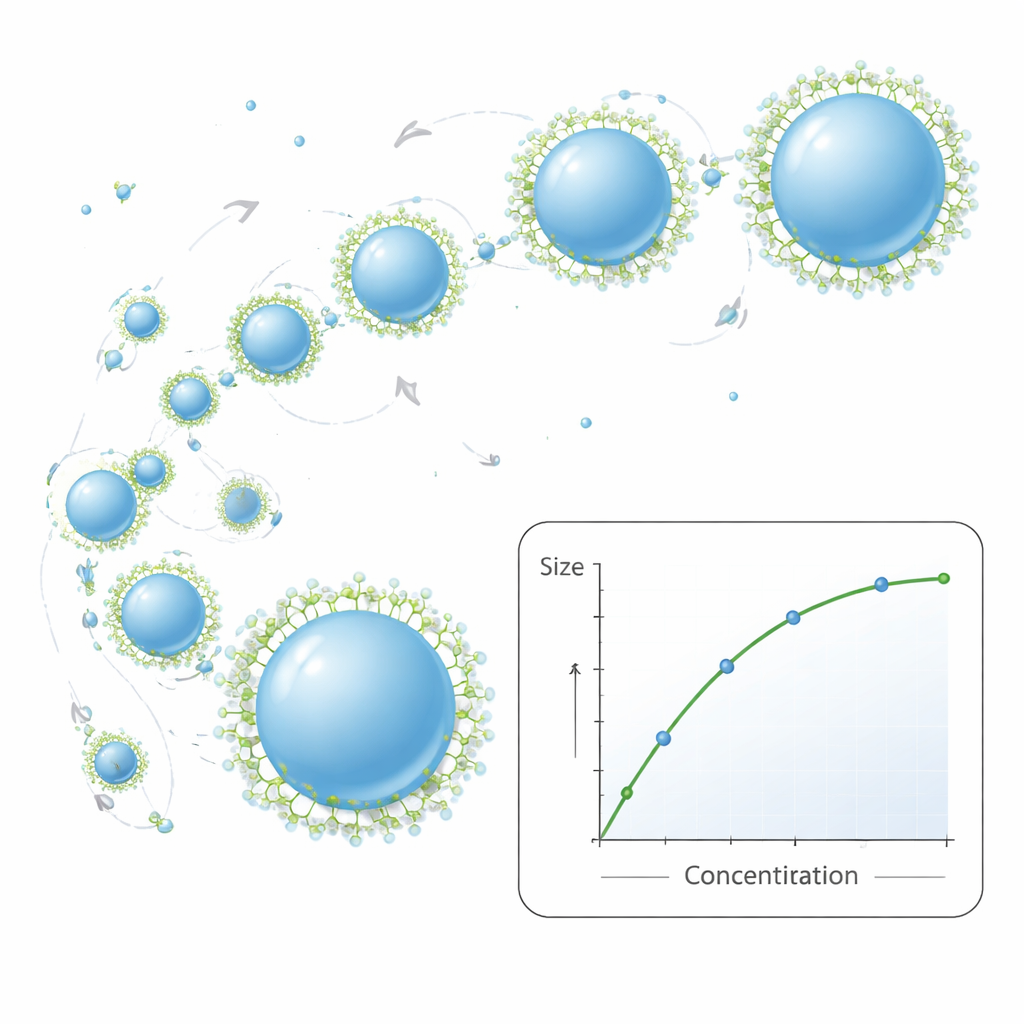
Een eenvoudige groeiregel die de werkelijkheid benadert
Het hart van het werk is een compact wiskundig model dat beschrijft hoe nanodeeltjes groeien nadat ze voor het eerst verschijnen. Het behandelt hun beweging als willekeurig gespring in vloeistof, waarbij botsingen soms leiden tot het samensmelten van twee deeltjes tot een groter exemplaar. Eerdere modellen gingen ervan uit dat deeltjes die elkaar ontmoetten onmiddellijk samensmolten en perfecte sferen vormden. Het nieuwe model voegt twee realistische wendingen toe: ten eerste staat het een eindige tijd toe waarin twee aangrenzende deeltjes van een uitgezakte, langgerekte vorm ontspannen naar één enkele bol; ten tweede laat het surfactantmoleculen geleidelijk het oppervlak 'blokkeren', waardoor verder samensmelten vertraagd of gestopt wordt. Met slechts een paar meetbare invoerwaarden — zoals temperatuur, vloeistofviscositeit en initiële polymeerconcentratie — voorspelt het model hoe de gemiddelde deeltjesgrootte met receptcondities verandert. Over vele experimenten kwamen de voorspelde groottes nauw overeen met die gemeten via lichtverstrooiing, terwijl het model ook de algemene trends in de breedte van de grootteverdeling vastlegde.
Het model als ontwerpgereedschap gebruiken
Om te testen of deze aanpak echt nuttig is, keerde het team het probleem om: in plaats van het model te gebruiken om eerdere data te verklaren, liet men het recepten voorstellen die drie specifieke deeltjesgroottes en uniformiteitsniveaus zouden moeten opleveren. De onderzoekers bereidden deze “ontworpen” formuleringen vervolgens in het laboratorium. De gemeten deeltjesdiameters weekten slechts 1–7 procent af van de doelen — ruim binnen de gebruikelijke experimentele variatie — wat laat zien dat het model formuliekeuzes betrouwbaar kan sturen. Voorspellingen over hoe smal of breed de grootteverdeling zou zijn waren minder precies, maar nog steeds voldoende om relatief nauwe van meer verspreide populaties te onderscheiden. Vergeleken met zware simulatietechnieken die elk molecuul of elke stroomwerveling volgen, draait dit gestroomlijnde model snel op bescheiden computers en is het eenvoudig aan te passen aan andere polymeren en procesopstellingen.
Wat dit betekent voor de toekomst van nanomedicatie
Voor niet‑specialisten is de kernboodschap dat het maken van bruikbare nanodeeltjes niet langer uitsluitend hoeft te steunen op zorgvuldig proef‑en‑foutwerk in het laboratorium. Door de essentiële fysica vast te leggen van hoe kleine plastic druppels bewegen, botsen en door surfactanten worden beschermd, levert dit werk een praktisch “kaartje” van formuliekeuzes — hoeveel polymeer, welke oplosmiddelmix, hoeveel stabilisator — naar de uiteindelijke deeltjesgrootte. Omdat PCL een veelgebruikt biologisch afbreekbaar materiaal is in medicijnafgifte, implantaten en beeldvormingsmiddelen, kan dit model onderzoekers helpen veiliger, effectievere nanogeneesmiddelen sneller en met minder verspild materiaal te ontwerpen. Dezelfde principes zijn toepasbaar op andere polymeren, wat meer voorspelbaarheid en efficiëntie kan brengen in de wereld van nanoschaaltherapieën.
Bronvermelding: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
Trefwoorden: polymeer-nanodeeltjes, nanoneerslag, medicijnafgifte, numerieke modellering, polycaprolacton