Clear Sky Science · nl
Nicorandil verbetert neuropathische en ontstekingspijn via TNF-α, IL6/MAPKERK1/2 en NO/cGMP‑signaalroutes
Waarom het verlichten van zenuwpijn belangrijk is
Miljoenen mensen leven met brandende, schietende of tintelende pijn die lang aanhoudt nadat een verwonding genezen is. Deze “neuropathische” pijn is vaak lastig te behandelen met gangbare pijnstillers en gaat vaak gepaard met bijwerkingen bij langdurig gebruik van medicatie. De hier samengevatte studie onderzoekt of nicorandil — een hartmiddel dat al aan patiënten met hartpijn wordt gegeven — ook overdreven actieve pijnbanen in het zenuwstelsel kan kalmeren, en hoe dit op cellulair niveau werkt.
Een hartmedicijn in pijnonderzoek
Nicorandil wordt routinematig voorgeschreven bij angina omdat het de bloedvaten ontspant. Het doet dit via twee belangrijke werkingen: het levert kleine hoeveelheden stikstofmonoxide (NO), een signaalmolecuul, en het opent bepaalde kaliumkanalen in cellen. Eerder dieronderzoek suggereerde dat nicorandil ook pijn kan verminderen door in te grijpen op zenuwreceptoren die betrokken zijn bij warmte- en pittige prikkels en door het eigen opioïde systeem van het lichaam te activeren. In de huidige studie wilden de onderzoekers in kaart brengen wat er stroomafwaarts van deze eerste effecten gebeurt, met de nadruk op ontsteking, oxidatieve stress (een soort chemische “roest”) en specifieke signaalroutes binnen zenuwcellen.
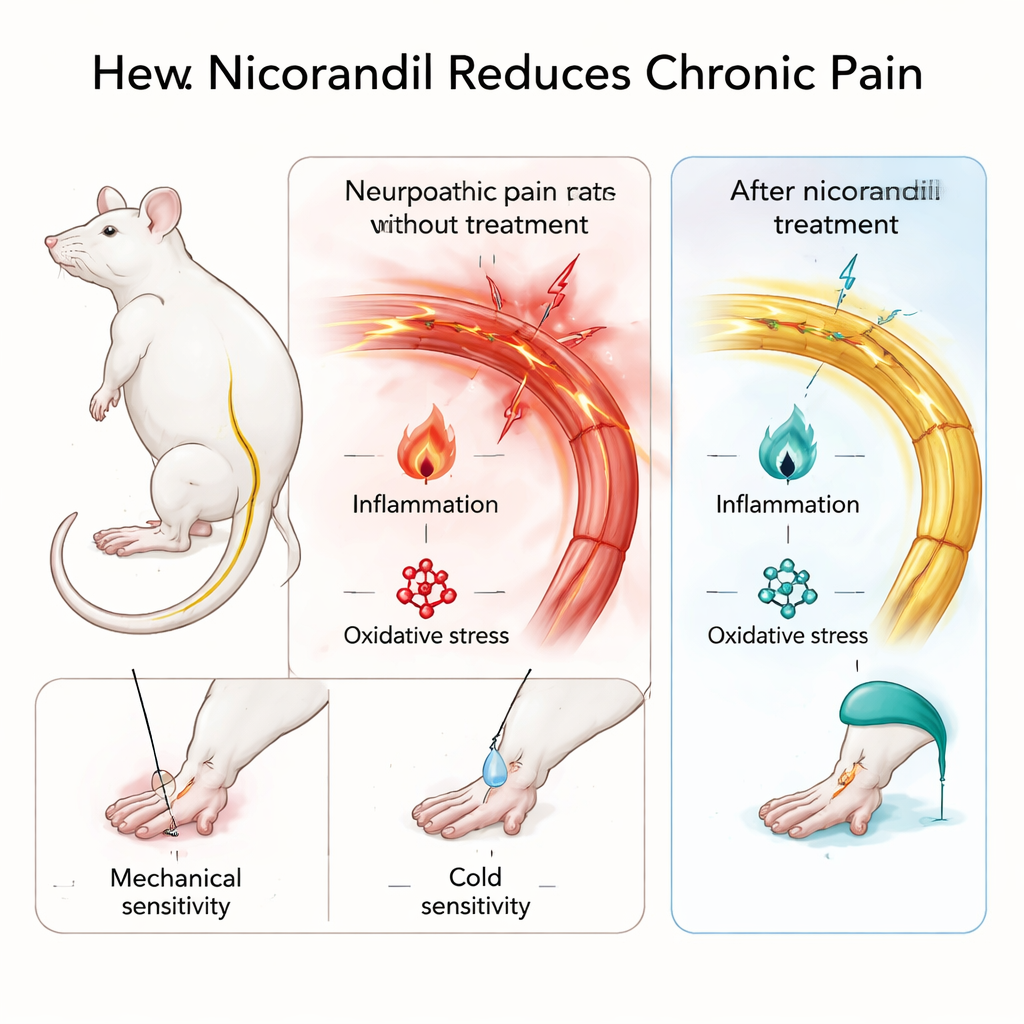
Nicorandil testen in modellen van aanhoudende pijn
Om langdurige zenuwpijn na te bootsen bond het team de nervus ischiadicus losjes samen bij ratten, een klassieke procedure die gevoeligheid voor aanraking en koude produceert vergelijkbaar met menselijke neuropathische pijn. Ze gebruikten ook de formalinetest, waarbij een milde chemische irriterende stof in een pootje wordt geïnjecteerd om goed afgebakende, aanhoudende ontstekingspijn te creëren. Ratten kregen nicorandil via de mond in twee doseringen, en de onderzoekers maten hoe sterk ze reageerden op lichte aanraking en koude van de beschadigde poot, evenals hoe vaak ze likten of wegfladderden na formaline. Belangrijk is dat nicorandil de dieren niet slaperig of ongecoördineerd maakte in een open-veldtest, wat suggereert dat de afname van pijngedrag niet eenvoudigweg door sedatie werd veroorzaakt.
Het terugschakelen van chemische ‘alarmsignalen’
Nicorandil verminderde duidelijk zowel pijn door zenuwbeschadiging als formaline‑geïnduceerde pijn. Behandelde ratten verdroegen aanraking en koude beter en toonden minder wegfladderen en kortere liktijden. Bloedonderzoek toonde aan dat nicorandil de niveaus verlaagde van krachtige ontstekingsboodschappers — tumor necrose factor alfa (TNF-α) en interleukine‑6 (IL‑6) — evenals cyclooxygenase‑2, een enzym dat bijdraagt aan de productie van pijngerelateerde prostaglandinen. Het verminderde ook malondialdehyde, een merker voor oxidatieve stress, wat wijst op minder chemische schade aan celmembranen. Onder de microscoop zagen de zenuwen van nicorandil‑behandelde dieren er gezonder uit: er was minder structurele schade en zwelling in de ischiaszenuw en in de groep sensibele zenuwcellen die de dorsale wortelganglion wordt genoemd.
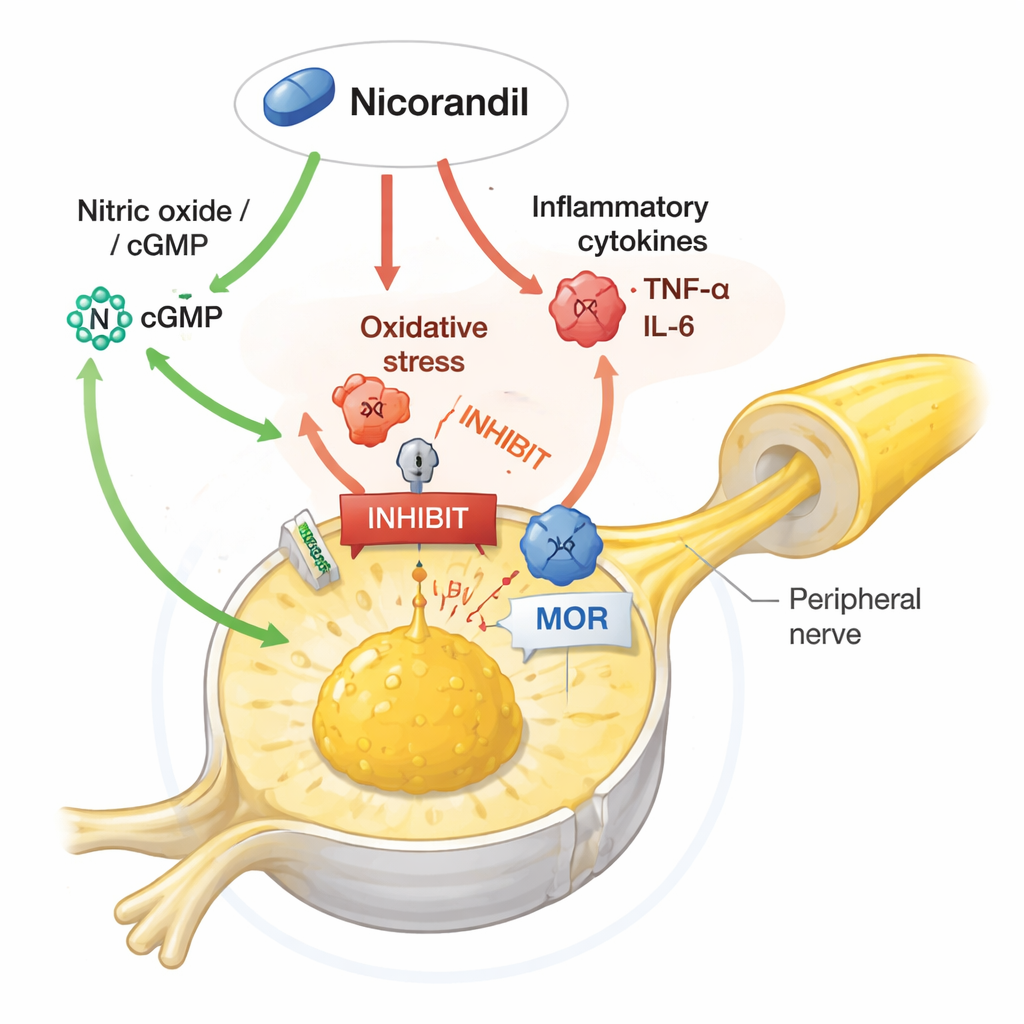
Het ontwarren van het signaalweb binnen pijnzenuwen
De studie ging verder door te onderzoeken welke moleculaire routes nodig waren voor de gunstige effecten van nicorandil. Toen de onderzoekers geneesmiddelen gaven die stikstofmonoxide versterkten of cyclisch GMP (cGMP, een boodschapper gekoppeld aan NO) verhoogden, verzwakte dat gedeeltelijk nicorandil’s vermogen om pijn te verminderen en sleutelproteïnen te normaliseren. Nicorandil voorkwam de gebruikelijke stijging van ERK1/2, een lid van de MAP‑kinasefamilie die pijnsignalen versterkt, en beperkte de niveaus van TRPV1, een kanaal dat zenuwen gevoeliger maakt voor warmte en chemische prikkels. Versterking van NO‑signalisatie of cGMP keerde deze beschermende veranderingen om, terwijl het blokkeren van NO‑vormende enzymen soms de pijnstilling door nicorandil versterkte. Verrassend genoeg maakte het blokkeren van de kaliumkanalen waarvoor nicorandil bekendstaat het niet onmogelijk om pijn te onderdrukken, wat suggereert dat in deze context het pijnstillende vermogen meer afhankelijk is van modulatie van stikstofmonoxide, oxidatieve stress, ontsteking en opioïde gerelateerde signalering dan van de klassieke vasculaire werking.
Wat dit zou kunnen betekenen voor mensen met pijn
Alles bij elkaar schetsen de bevindingen nicorandil als een multitarget pijnmodulator: het kalmeert overactieve zenuwbanen door oxidatieve schade en ontstekingsboodschappers te verminderen, ERK1/2 en TRPV1 in sensorische neuronen tot rust te brengen en te interacteren met stikstofmonoxide en het eigen opioïde systeem van het lichaam. Hoewel deze resultaten afkomstig zijn van rattenmodellen en kortdurende dosering, suggereren ze dat een medicijn dat al in de klinische praktijk voor hartziekten wordt gebruikt, mogelijk op den duur herbestemd of aangepast kan worden om moeilijk behandelbare neuropathische en ontstekingspijn te helpen bestrijden. Toekomstig onderzoek bij mensen is nodig om veilige doseringen, lange termijn‑effecten en of dezelfde beschermende mechanismen in menselijke zenuwen werken vast te stellen.
Bronvermelding: Badr, R.M., Abuiessa, S.A., Elblehi, S.S. et al. Nicorandil ameliorates neuropathic and inflammatory pain via TNF-α, IL6/MAPKERK1/2 and NO/cGMP signaling. Sci Rep 16, 4722 (2026). https://doi.org/10.1038/s41598-026-35272-4
Trefwoorden: neuropathische pijn, nicorandil, ontsteking, oxidatieve stress, stikstofmonoxide‑signaleringsroute