Clear Sky Science · nl
Verstoring van zinkhomeostase verlaagt histonacetyleringsniveaus in normale en tumorcellen
Wanneer een nuttig metaal schadelijk wordt
Zink is vooral bekend als de voedingsstof in multivitaminen die ons immuunsysteem en wondgenezing ondersteunt. Maar binnen onze cellen moet zink binnen een zeer nauwe "precies goed" range gehouden worden. Deze studie laat zien dat wanneer zinkniveaus in cellen te hoog worden, ze belangrijk genen stilletjes kunnen uitschakelen door de manier waarop DNA is verpakt aan te spannen, en zelfs cellen kunnen aanzetten tot een schoonmaakproces genaamd autofagie. Omdat zinksupplementen, anti-roosingrediënten en experimentele kankergeneesmiddelen allemaal zinkniveaus kunnen veranderen, is begrip van dit verborgen regelsysteem van belang voor dagelijkse gezondheid en toekomstige therapieën.
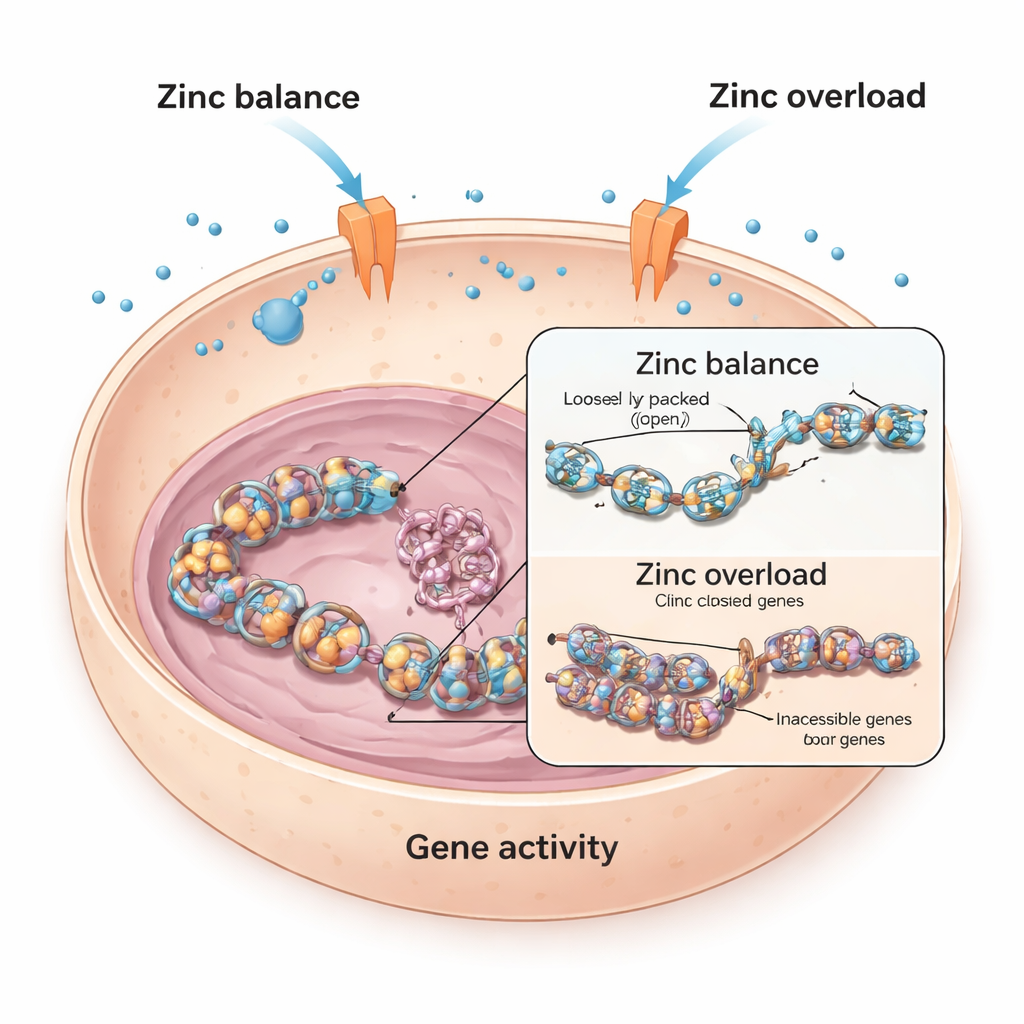
Zink in balans houden binnen levende cellen
Elke cel is afhankelijk van zink, dat duizenden eiwitten helpt hun werk te doen. Om zowel tekort als overmaat te vermijden, gebruiken cellen speciale "poorten" in hun membranen, zogeheten zinktransporters, om zink naar binnen en naar buiten te verplaatsen. De onderzoekers begonnen met hartspiercellen van muizen en mensen en onderzochten wat er gebeurt wanneer deze cellen extra zink krijgen. Ze ontdekten dat in muizencellen hoge zinkniveaus de activiteit van een sleutelgen verbonden met het hart, Bmp4, sterk verminderden; dit gen helpt bij het sturen van hartontwikkeling en functie. In tegenstelling daarmee waren menselijke hartcellen veel minder aangetast, wat erop wijst dat verschillende cellen zich op verschillende manieren verdedigen tegen zinkoverbelasting.
Hoe zink de DNA‑verpakking aanspant
Om te achterhalen hoe zink genen zoals Bmp4 uitschakelt, keek het team naar histonen, de haspelachtige eiwitten waar het DNA omheen gewikkeld zit. Wanneer kleine chemische labels, acetylgroepen genaamd, aan histonen worden toegevoegd, wordt het DNA losser en makkelijker af te lezen; wanneer deze labels worden verwijderd, pakt het DNA strakker en worden genen moeilijker aangezet. De studie toonde aan dat overtollig zink in muizenhartcellen leidde tot een daling van histonacetylering op een specifiek punt (bekend als H3K9), wat nauw overeenkwam met de daling in Bmp4‑activiteit. Geneesmiddelen die histon‑de‑acetylase‑enzymen blokkeren konden het effect van zink terugdraaien en Bmp4 herstellen, wat suggereert dat zink de balans van dit chemische labelingssysteem verstoorde.
Te veel zink binnenin, niet alleen buiten
De cruciale stap bleek zink in het waterige cytoplasma van de cel te zijn, niet alleen in de omringende vloeistof. Met een fluorescentieprobe die oplicht bij vrije zink, zagen de onderzoekers een golf van zink binnenin muizencellen na behandeling. Toen ze een zinkshuttle gebruikten om zink rechtstreeks in cellen te duwen, zagen ze dezelfde daling in histonacetylering en genactiviteit, zelfs bij veel lagere zinkconcentraties in het buitenmilieu. Bij menselijke hartcellen daarentegen pasten de transporters in het celmembraan zich snel aan: sommige zinkinvoerapparaten schakelden uit en uitvoerapparaten werden opgevoerd, waardoor een sterke stijging van intern zink werd voorkomen en de histonacetylering beschermd bleef. Muizenhartcellen toonden een meer "verkeerd aangesloten" transporterrespons, waardoor meer zink naar binnen kon stromen en gencontrole verstoorde.
Van genregulatie tot zelfreiniging in normale en tumorcellen
De onderzoekers vroegen zich vervolgens af of deze zinkgedreven aanscherping van DNA‑verpakking uniek is voor hartcellen. Ze testten verschillende normale menselijke celtypen en kankercellijnen uit maag, baarmoeder en eierstok. Wanneer zink zich met behulp van een shuttle binnenin kon ophopen, toonden bijna al deze cellen een duidelijke daling in histonacetylering. In sommige tumorcellen, zoals maagkankercellen, trad dit zelfs op bij bijzonder lage zinkdoses, wat suggereert dat bepaalde kankers buitengewoon gevoelig zijn voor zinkverstoring. Het team koppelde verlaagde acetylering ook aan autofagie, een proces waarbij cellen versleten onderdelen recyclen. Matige interne zinkstijgingen versterkten autofagie, maar zeer hoge zinkniveaus verzwakten het uiteindelijk, wat wijst op een smal venster waarin zink mogelijk gebruikt kan worden om dit zelfreinigingspad bij te stellen.
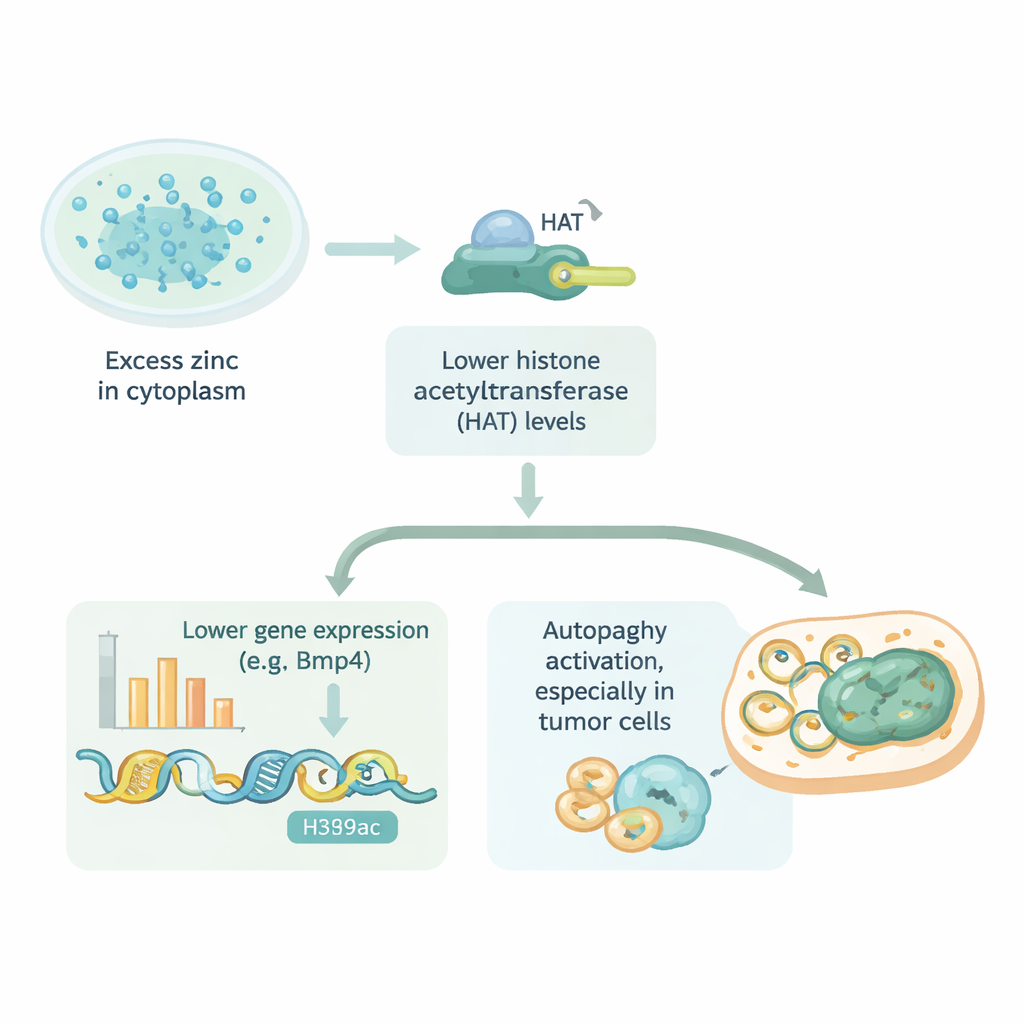
Wat dit betekent voor gezondheid en behandeling
Kort gezegd toont dit werk aan dat te veel zink binnen cellen genen kan terugschakelen door DNA moeilijker toegankelijk te maken, en dat hetzelfde pad kan beïnvloeden hoe actief cellen zichzelf schoonmaken. Het effect beperkt zich niet tot hartcellen; het blijkt te gelden voor verschillende normale en kankercellen, hoewel sommige beter in staat zijn zich te verdedigen tegen zinkoverbelasting dan andere. Deze inzichten suggereren dat de kleine zinktransport"poorten" in celmembranen veelbelovende medicinale aangrijpingspunten zouden kunnen zijn — ofwel om gezond weefsel te beschermen tegen zinkgerelateerde schade ofwel om kwetsbare tumoren richting celdood te duwen. Hoewel de bevindingen uit kweekcelexperimenten komen, bieden ze een nieuw perspectief op hoe een alledaagse voedingsstof genactiviteit en ziekte kan beïnvloeden wanneer haar delicate balans verstoord raakt.
Bronvermelding: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
Trefwoorden: zinkhomeostase, genregulatie, histonacetylering, autofagie, kankercellen