Clear Sky Science · nl
Metabole herprogrammering vergroot de weerstand tegen oxidatieve stress in differentierende cardiomyocyten
Waarom de strijd van hartcellen met zuurstof ertoe doet
Elke hartslag hangt af van gespecialiseerde spiercellen, cardiomyocyten genoemd. Tijdens de ontwikkeling ondergaan deze cellen een ingrijpende overgang: ze gaan van een laag-zuurstof, suikergestuurde omgeving in de baarmoeder naar een zuurstofrijke omgeving na de geboorte. Zuurstof is onmisbaar, maar het levert ook schadelijke bijproducten die DNA kunnen beschadigen en cellen kunnen doden. Deze studie onderzoekt hoe rijpende hartcellen hun metabolisme herschakelen zodat ze meer zuurstof aankunnen, meer energie produceren en zich tegelijk tegen oxidatieve schade beschermen — inzichten die toekomstige behandelingen voor hartziekten en regeneratie kunnen informeren.
Van eenvoudige bouwers naar krachtpatsers
Onrijpe hartcellen, cardiomyoblasten genoemd, zijn kleine, delende cellen die voornamelijk afhankelijk zijn van afbraak van glucose voor energie. Terwijl ze differentiëren tot volwassen cardiomyocyten stoppen ze met delen en groeien ze, vaak samensmeltend tot polynucleaire, langgerekte cellen die beter geschikt zijn voor krachtige contractie. Met behulp van hoogresolutiemicroscopie volgden de onderzoekers deze transformatie over tien dagen in een laboratoriummodel. Markers voor celproliferatie namen af, terwijl de cellen uitrekken en zich reorganiseren tot vezelige, hartachtige structuren, wat bevestigt dat ze een meer volwassen, contractiele toestand zijn binnengestapt. 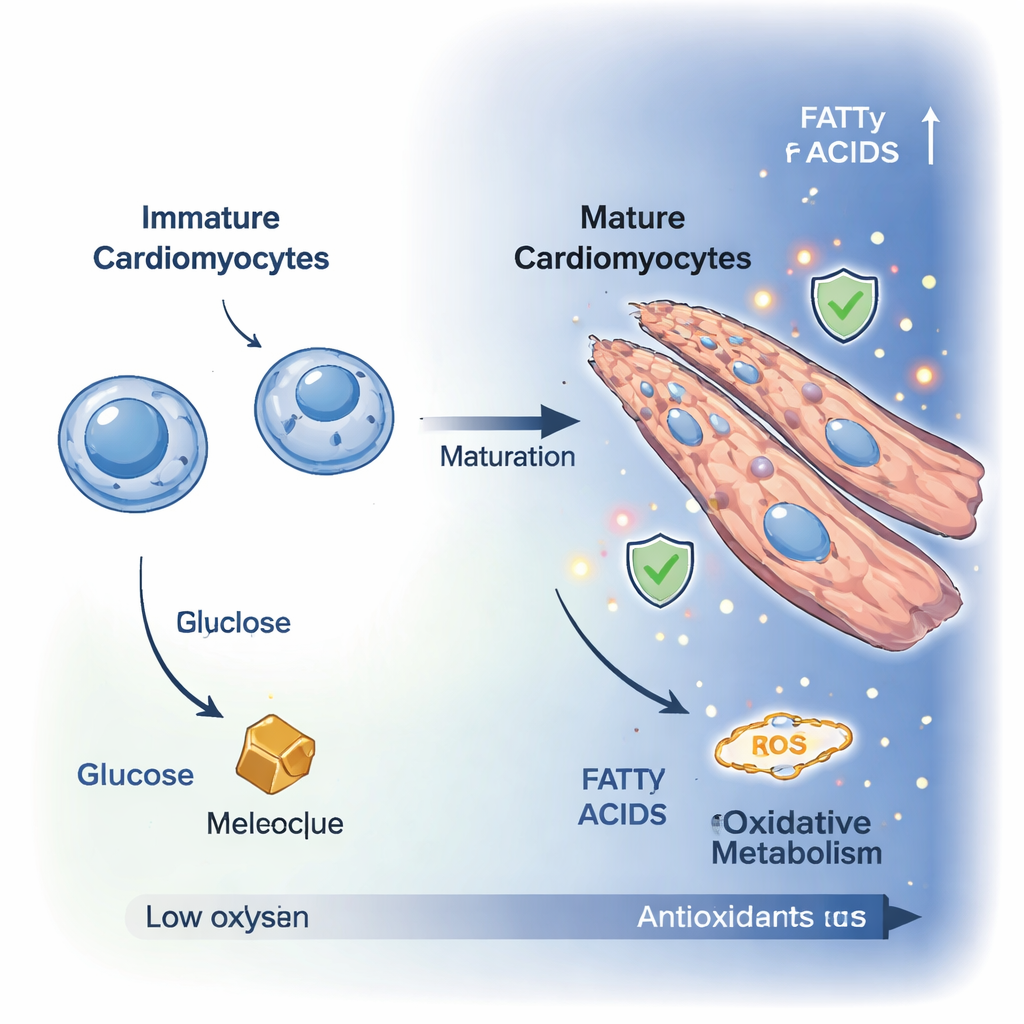
Brandstoffen verwisselen en nieuwe energieroutes aanleggen
Om te begrijpen wat er intern verandert, maten de onderzoekers honderden kleine moleculen in de cellen en gebruikten geavanceerde beeldvorming van natuurlijke celfluorescentie om energieverbruik in realtime te volgen. Gezamenlijk lieten deze technieken een duidelijke verschuiving zien van een glycolytische toestand, waarin cellen voornamelijk glucose verbranden, naar een oxidatieve toestand gedomineerd door mitochondriale respiratie. De niveaus van glucose en fructose daalden, terwijl tussenproducten van de tricarbonzuurcyclus (TCA) — zoals citroenzuur, malaat en oxoglutarraat — toenamen. Weganalyse toonde sterkere activiteit in routes die brandstof naar de mitochondriën voeren, waaronder de malaat–aspartaatshuttle en de afbraak van aminozuren, wat aangeeft dat rijpe cardiomyocyten hun brandstofopties verbreden en energie efficiënter naar hun energiecentrales leiden.
Leven met meer zuurstof — en meer stress
Efficiënter branden in de mitochondriën heeft een prijs: verhoogde productie van reactieve zuurstofsoorten (ROS), chemisch agressieve moleculen die lipiden, eiwitten en DNA kunnen beschadigen. De onderzoekers vonden dat naarmate cardiomyocyten rijpten, hun mitochondriën groter en meer uitgerekt werden, en markers voor oxidatieve stress toenamen. Fluorescentiebeeldvorming toonde meer lipofuscine-achtige korrels, een kenmerk van geoxideerde lipiden, en een nucleaire probe liet hogere ROS-niveaus zien in gedifferentieerde cellen. Metabolomics wees op veranderingen in glutathionmetabolisme, een centraal antioxiderend systeem dat het molecuul glutathion — opgebouwd uit aminozuren zoals glutamaat en glycine — gebruikt om ROS te neutraliseren. Deze bevindingen suggereren dat terwijl hartcellen hun oxidatieve metabolisme opvoeren, ze ook hun antioxiderende routes bijstellen om schade onder controle te houden. 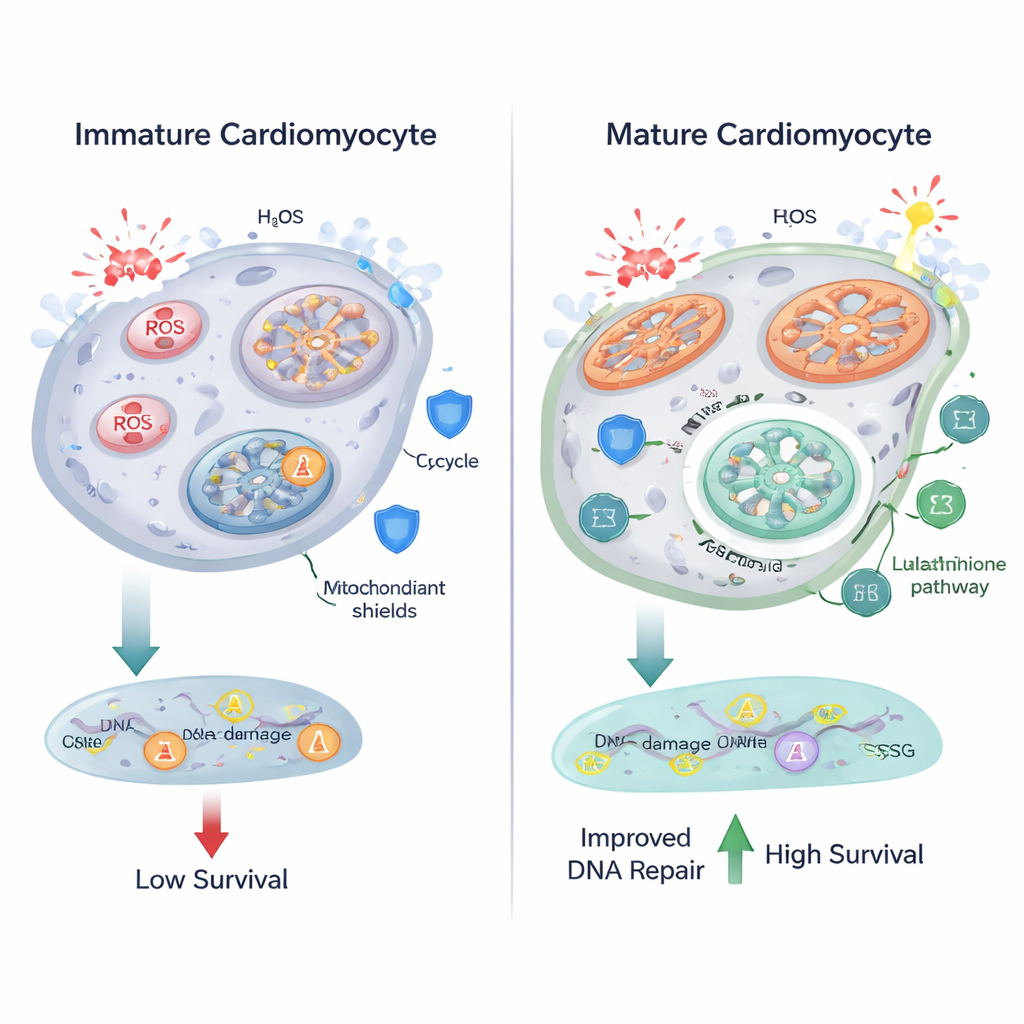
Schade ingeperkt, verdediging versterkt
Verrassend genoeg lieten gedifferentieerde cardiomyocyten, ondanks hogere ROS, niet meer DNA-breuken zien dan hun onrijpe tegenhangers wanneer gemeten met γ-H2AX-foci, een gevoelige marker voor DNA-schade. Toen het team de cellen uitdaagde met waterstofperoxide, een sterke oxidator, stapelden zowel onrijpe als rijpe cellen ROS en DNA-breuken op — maar de rijpe cellen hielden het beter. Zij vertoonden relatief minder DNA-letsel ten opzichte van hun hogere ROS-niveaus, waren minder geneigd om celdoodsgemedieerde signalen zoals PUMA te activeren, en toonden aanzienlijk hogere overlevingspercentages. Deze resultaten wijzen erop dat differentierende cardiomyocyten niet alleen hun metabolisme aanpassen maar ook hun DNA-reparatie- en overlevingsmechanismen upgraden, waardoor ze stevigere oxidatieve omstandigheden kunnen doorstaan.
Wat dit betekent voor het beschermen van het hart
Kort gezegd toont deze studie aan dat hartcellen tijdens hun volwassenwording leren harder te werken zonder zichzelf te vernietigen. Ze schakelen van een suikerrijk, laag-zuurstofleven naar een zuurstofintensief, mitochondriën-gedreven bestaan en bouwen tegelijk betere schilden en reparatieteams om met oxidatieve stress om te gaan. Inzicht in dit fijn afgestemde evenwicht tussen energieproductie en zelfbescherming kan onderzoekers helpen strategieën te ontwikkelen om beschadigd volwassen hartweefsel veerkrachtiger te maken of om stamcellen te sturen naar veiligere, duurzamere cardiomyocyten voor regeneratieve therapieën.
Bronvermelding: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Trefwoorden: cardiomyocyt-differentiatie, oxiderende stress, mitochondriën, celmetabolisme, hartaandoening